Com 7- Equilibrio Quimico.ppt
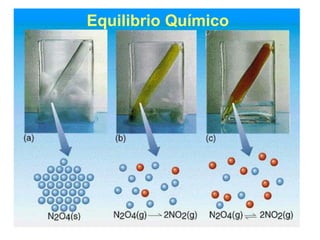
- 2. Equilibrio Químico 2NO2(g) N2O4(g) •Una reacción química ha alcanzado el equilibrio cuando las concentraciones de todos los reactivos y productos permanece constante, a una cierta temperatura. •Las velocidades de las reacciones directa e inversa son iguales al alcanzar el estado de equilibrio.
- 3. A ↔ B Equilibrio Químico
- 4. N2(g) + 3 H2 (g)→ 2 NH3(g) Equilibrio Químico
- 5. 3 2 2 2 3 H N NH c K Constante de Equilibrio N2(g) + 3 H2 (g)→ 2 NH3(g)
- 6. b a q p c K B A Q P a A(g) + b B(g) ↔ p P(g) + q Q(q) b a q p P P P P P K B A Q P Kp = Kc (RT)∆n Constante de Equilibrio
- 7. • Si todos los reactivos y productos están en una sola fase, el equilibrio es homogéneo. • Si uno o más reactivos o productos están en una fase diferente, el equilibrio es heterogéneo. CaCO3(s) CaO(s) + CO2(g) Constante de Equilibrios Heterogéneos ) ( 2 ) ( 2 ) ( 2 ) ( 3 ) ( CO constante CO constante CO CaCO CaO g c c g g s s c K K K
- 8. N2O4(g) 2NO2(g) 0,212 O N NO K 4 2 2 2 c N2(g) + 3H2(g) 2NH3(g) 0,5 H N NH K 3 2 2 2 3 c CaCO3(s) CaO(s) + CO2(g) 2 c CO K Constante de Equilibrio La concentración de los líquidos y de los sólidos puros no se incluye en la constante de equilibrio.
- 9. Magnitud de las constantes de equilibrio
- 10. aA + bB(g) pP + qQ b a q p Q B A Q P Predicción del sentido de una reacción b a q p c K B A Q P Cociente de Reacción (Q) Q > K Q < K Q = K Equilibrio
- 11. Principio de Le Châtelier Si un sistema que ha alcanzado el equilibrio químico es perturbado (cambio de concentración, T, P, V), reacciona oponiéndose a la perturbación, de modo de volver a la condición de equilibrio. N2(g) + 3H2(g) 2NH3(g)
- 12. Principio de Le Châtelier: Efecto de la concentración
- 13. Principio de Le Châtelier N2(g) + 3H2(g) 2NH3(g)
- 14. Principio de Le Châtelier: Proceso Haber N2(g) + 3H2(g) 2NH3(g)
- 15. T= cte Relación entre K y G (1)
- 16. Relación entre K y G (2)
- 17. Relación entre K y G (3)
- 18. En el equilibrio, ∆G = 0 Relación entre K y G (4)
- 19. G = Gº + RT ln (P/Pº) G = Gº + RT ln (C/Cº) Relación entre K y G (5) ∆Gº = ∆Hº - T ∆Sº ∆Gº = -RT lnK = ∆Hº - T ∆Sº K = e (-∆Hº/RT + ∆Sº/R)
- 20. ∆Gº = ∆Hº - T ∆Sº ∆Gº = -RT lnK = ∆Hº - T ∆Sº ∆H> 0 ∆H< 0 Relación entre K y T
- 22. Diferencia entre estabilidad cinética y termodinámica