Análisis Gravimétrico - Clase 03
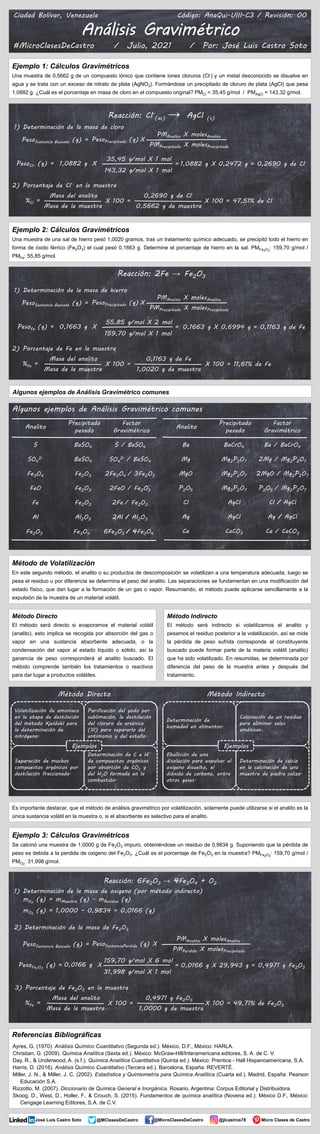
- 1. Determinación de humedad en alimentos. Calcinación de un residuo para eliminar sales amónicas. Ebullición de una disolución para expulsar el oxígeno disuelto, el dióxido de carbono, entre otros gases. Determinación de calcio en la calcinación de una muestra de piedra caliza. Ejemplos Volatilización de amoniaco en la etapa de destilación del método Kjeldahl para la determinación de nitrógeno. Purificación del yodo por sublimación, le destilación del cloruro de arsénico (III) para separarlo del antimonio y del estaño. Separación de muchos compuestos orgánicos por destilación fraccionada. Determinación de C e H de compuestos orgánicos por absorción de CO2 y del H2O formada en la combustión. Ejemplos Método Indirecto Método Directo Ciudad Bolívar, Venezuela Código: AnaQui-UIII-C3 / Revisión: 00 Análisis Gravimétrico #MicroClasesDeCastro / Julio, 2021 / Por: José Luis Castro Soto Referencias Bibliográficas Ayres, G. (1970). Análisis Químico Cuantitativo (Segunda ed.). México, D.F., México: HARLA. Christian, G. (2009). Química Analítica (Sexta ed.). México: McGraw-Hill/Interamericana editores, S. A. de C. V. Day, R., & Underwood, A. (s.f.). Química Analítica Cuantitativa (Quinta ed.). México: Prentice - Hall Hispanoamericana, S.A. Harris, D. (2016). Análisis Químico Cuantitativo (Tercera ed.). Barcelona, España: REVERTÉ. Miller, J. N., & Miller, J. C. (2002). Estadística y Quimiometría para Química Analítica (Cuarta ed.). Madrid, España: Pearson Educación S.A. Rizzotto, M. (2007). Diccionario de Química General e Inorgánica. Rosario, Argentina: Corpus Editorial y Distribuidora. Skoog, D., West, D., Holler, F., & Crouch, S. (2015). Fundamentos de química analítica (Novena ed.). México D.F., México: Cengage Learning Editores, S.A. de C.V. @jlcastros78 Micro Clases de Castro José Luis Castro Soto @MicroClasesDeCastro @MClasesDeCastro Ejemplo 1: Cálculos Gravimétricos Una muestra de 0,5662 g de un compuesto iónico que contiene iones cloruros (Cl-) y un metal desconocido se disuelve en agua y se trata con un exceso de nitrato de plata (AgNO3). Formándose un precipitado de cloruro de plata (AgCl) que pesa 1,0882 g. ¿Cuál es el porcentaje en masa de cloro en el compuesto original? PMCl = 35,45 g/mol / PMAgCl = 143,32 g/mol. Reacción: Cl- (ac) → AgCl (s) 1) Determinación de la masa de cloro 2) Porcentaje de Cl- en la muestra PesoSustancia Buscada (g) = PesoPrecipitado (g) X PMAnalito X molesAnalito PMPrecipitado X molesPrecipitado PesoCl- (g) = 1,0882 g X 143,32 g/mol X 1 mol 35,45 g/mol X 1 mol 1,0882 g X 0,2472 g = 0,2690 g de Cl− = %Cl = Masa del analito Masa de la muestra X 100 = 0,2690 g de Cl− 0,5662 g de muestra X 100 = 47,51% de Cl Algunos ejemplos de Análisis Gravimétrico comunes Método de Volatilización En este segundo método, el analito o su productos de descomposición se volatilizan a una temperatura adecuada, luego se pesa el residuo u por diferencia se determina el peso del analito. Las separaciones se fundamentan en una modificación del estado físico, que dan lugar a la formación de un gas o vapor. Resumiendo, el método puede aplicarse sencillamente a la expulsión de la muestra de un material volátil. Ejemplo 2: Cálculos Gravimétricos Una muestra de una sal de hierro pesó 1,0020 gramos, tras un tratamiento químico adecuado, se precipitó todo el hierro en forma de óxido férrico (Fe2O3) el cual pesó 0,1663 g. Determine el porcentaje de hierro en la sal. PMFe2O3 : 159,70 g/mol / PMFe: 55,85 g/mol. Reacción: 2Fe → Fe2O3 1) Determinación de la masa de hierro 2) Porcentaje de Fe en la muestra PesoSustancia Buscada (g) = PesoPrecipitado (g) X PMAnalito X molesAnalito PMPrecipitado X molesPrecipitado PesoFe (g) = 0,1663 g X 159,70 g/mol X 1 mol 55,85 g/mol X 2 mol 0,1663 g X 0,6994 g = 0,1163 g de Fe = %Fe = Masa del analito Masa de la muestra X 100 = 0,1163 g de Fe 1,0020 g de muestra X 100 = 11,61% de Fe Ejemplo 3: Cálculos Gravimétricos Se calcinó una muestra de 1,0000 g de Fe2O3 impuro, obteniéndose un residuo de 0,9834 g. Suponiendo que la pérdida de peso es debida a la perdida de oxigeno del Fe2O3. ¿Cuál es el porcentaje de Fe2O3 en la muestra? PMFe2O3 : 159,70 g/mol / PMO2 : 31,998 g/mol. Reacción: 6Fe2O3 → 4Fe3O4 + O2 3) Porcentaje de Fe2O3 en la muestra %Fe = Masa del analito Masa de la muestra X 100 = 0,4971 g Fe2O3 1,0000 g de muestra X 100 = 49,71% de Fe2O3 1) Determinación de la masa de oxigeno (por método indirecto) m02 (g) = mMuestra (g) - mResiduo (g) m02 (g) = 1,0000 – 0,9834 = 0,0166 (g) PesoSustancia Buscada (g) = PesoSustanciaPerdida (g) X PMAnalito X molesAnalito PMPerdido X molesPrecipitado PesoFe2O3 (g) = 0,0166 g X 31,998 g/mol X 1 mol 159,70 g/mol X 6 mol 0,0166 g X 29,943 g = 0,4971 g Fe2O3 = 2) Determinación de la masa de Fe2O3 Método Directo El método será directo si evaporamos el material volátil (analito), esto implica se recogida por absorción del gas o vapor en una sustancia absorbente adecuada, o la condensación del vapor al estado líquido o sólido, así la ganancia de peso corresponderá al analito buscado. El método comprende también los tratamientos o reactivos para dar lugar a productos volátiles. Método Indirecto El método será indirecto si volatilizamos el analito y pesamos el residuo posterior a la volatilización, así se mide la pérdida de peso sufrida corresponde al constituyente buscado puede formar parte de la materia volátil (analito) que ha sido volatilizado. En resumidas, se determinada por diferencia del peso de la muestra antes y después del tratamiento. Es importante destacar, que el método de análisis gravimétrico por volatilización, solamente puede utilizarse si el analito es la única sustancia volátil en la muestra o, si el absorbente es selectivo para el analito. Algunos ejemplos de Análisis Gravimétrico comunes Analito Precipitado pesado Factor Gravimétrico S / BaSO4 BaSO4 S SO4 2- / BaSO4 BaSO4 SO4 2- 2FeO / Fe2O3 Fe2O3 FeO 2Fe / Fe2O3 Fe2O3 Fe 2MgO / Mg2P2O7 Mg2P2O7 MgO P2O5 / Mg2P2O7 Mg2P2O7 P2O5 2Fe3O4 / 3Fe2O3 Fe2O3 Fe3O4 Fe2O3 Fe3O4 6Fe2O3 / 4Fe3O4 Cl AgCl Cl / AgCl Ca CaCO3 Ca / CaCO3 BaCrO4 Ba Ba / BaCrO4 2Mg / Mg2P2O7 Mg2P2O7 Mg Analito Precipitado pesado Factor Gravimétrico Al Al2O3 2Al / Al2O3 Ag AgCl Ag / AgCl
