FENÓMENOS DE TRANSPORTE EN INGENIERÍA QUIMICA
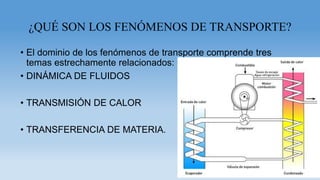
- 1. ¿QUÉ SON LOS FENÓMENOS DE TRANSPORTE? • El dominio de los fenómenos de transporte comprende tres temas estrechamente relacionados: • DINÁMICA DE FLUIDOS • TRANSMISIÓN DE CALOR • TRANSFERENCIA DE MATERIA.
- 2. RAZONES DEL ESTUDIO DE LOS FENOMENOS DE TRANSPORTE A menudo se presentan de manera simúltanea en problemas industriales, biológicos, agrícolas y metereológicos; de hecho, el desarrollo de cualquier proceso de transporte en forma individual es la excepción, más que la regla. Las Ecuaciones básicas que describen los tres fenómenos de transporte están bastante relacionadas entre sí. La semenjanza de las ecuaciones es la base para resolver problemas “por analogía”.
- 3. Los mecanismos moleculares que constituyen la base de los diversos fenómenos de transporte tienen una estrecha relación entre sí. Toda la materia está hecha de moléculas, y los mismos movimientos e interacciones moleculares son responsables de la viscosidad, conductividad térmica y la difusión.
- 4. FENOMENOS DE TRANSPORTE INGENIERIA QUIMICA. Transporte - Difusión 4 TRANSPORTE DE ENERGIA TRANSPORTE DE MATERIA TRANSPORTE DE CANTIDAD DE MOVIMIENTO TRANSFERENCIA DE MASA--------------------------------------Gradiente de concentración TRANSFERENCIA DE CALOR-------------------------------------Gradiente de temperatura TRANSFERENCIA DE CANTIDAD DE MOVIMIENTO-------Gradiente de velocidad
- 5. INGENIERIA QUIMICA. Transporte - Difusión 5 SISTEMA A1 A2 A4 A3 Estado Estacionario
- 6. INGENIERIA QUIMICA. Transporte - Difusión 6
- 7. INGENIERIA QUIMICA. Transporte - Difusión 7
- 8. INGENIERIA QUIMICA. Transporte - Difusión 8
- 9. INGENIERIA QUIMICA. Transporte - Difusión 9
- 10. PRIMERA LEY DE FICK Adolf Eugen Fick (1829-1901) FUNDAMENTO: Describe el movimiento de una especie química A através de una mezcla binaria de A y B debido a un gradiente de concentración de A. EJEMPLO: Al dejar caer un pequeño cristal de permanganato de potasio en un vaso de precipitado que contenga agua. El KMnO4 empieza a disolverse en el agua, y muy cerca del cristal hay una solución concentrada púrpura oscura de KMnO4 se difunde lejos del cristal. El avance de la difusión puede seguirse entonces al observar el crecimiento de la región purpura oscura.
- 11. DIFUSIVIDAD DEL PERMANGANATO DE POTASIO
- 12. EJERCICIO• Calcular la densidad de flujo de masa j(ay) en estado estacionario del helio para el sistema siguiente a 500°c. La presión parcial del helio es 1 atm a y=0 y cero en la superficie superior de la lámina. el espesor y de la lámina de cristal de Pyrex es 10ˉ² mm, y su densidad 𝜌(𝐵) = 2,6𝑔/𝑐𝑚3 Se ha reportado que la solubilidad y la difusividad del helio en cristal Pyrex es de 0.0084 volúmenes de helio gaseoso por volumen de cristal y 𝔇 𝐴𝐵 = 0.2𝑋10−7 𝑐𝑚2 /𝑠, respectivamente. Demostrar que es razonable despreciar la velocidad media de masa. • Solución • 𝜌𝐴0 = 0.0084 𝜌 𝐴0 𝑀 𝐴 𝑅𝑇 • = (0.0084) (1.0 𝑎𝑡𝑚)(4.00𝑔/𝑚𝑜𝑙) 82.05𝑐𝑚3 𝑎𝑡𝑚/𝑚𝑜𝑙 𝐾)(773𝐾) • 𝜌𝐴0 = 5.3𝑥10−7 𝑔/𝑐𝑚3
- 13. • Así, la fracción de masa del helio en la fase sólida en la superficie inferior es • 𝜔𝐴0 = 𝜌𝐴0 𝜌𝐴0+𝜌𝐵0 = 5.3∗10−7 5.3∗10−7+2.6 = 2.04 ∗ 10−7 • Ahora podemos calcular la densidad de flujo del helio a partir de la ecuación: • 𝜔 𝐴𝑦 𝐴 = 𝜌𝐷 𝐴𝐵 𝜔 𝐴0−0 𝑌 • 𝐽 𝐴𝑦 = (2.6𝑔/𝑐𝑚3 )(2.0 ∗ 10−8 𝑐𝑚2 /𝑠) 2.04∗10−7 10−3 𝑐𝑚 • = 1.05 ∗ 10−11 𝑔/𝑐𝑚2 𝑠 • Luego la velocidad del helio puede obtenerse a partir de la ecuación: • 𝑣 𝐴𝑦 = 𝐽 𝐴𝑦 𝜌𝐴 + 𝑣𝑦 ∴ 𝑣 𝐴𝑦/ 𝑦=0= 1.05∗10−11 𝑔/𝑐𝑚2 𝑠 5.3∗10−7 𝑔/𝑐𝑚3 + 𝑣𝑦0 = 1.98 ∗ 10−5 𝑐𝑚/𝑠 + 𝑣𝑦0 • Entonces, el valor correspondiente 𝒗𝒚 𝟎 de la velocidad media de masa del sistema cristal-helio en y=0 se obtiene a partir de la ecuación: • 𝑉𝑦 = 𝜔 𝐴 𝑣 𝐴𝑦 + 𝜔 𝐵 𝑣 𝐵𝑦 • 𝑉𝑦0 = (2.04 ∗ 10−7 )(1.98 ∗ 10−5 𝑐𝑚/𝑠 + 𝑉𝑦0) + (1 − 2.04 ∗ 10−7 )(0) • 𝑉𝑦0 = (2.04∗10−7)(1.98∗10−5 𝑐𝑚/𝑠 ) 1−2.04∗10−7 • 𝑉𝑦0 = 4.04 ∗ 10−12 𝑐𝑚/𝑠
- 14. VIDEO PRIMERA LEY DE FICK
- 15. INGENEIRIA QUIMICA. Transporte - Difusión 15 LEY DE DIFUSION DE FICK Es la rapidez de difusión por unidad de area de sección transversal en una dirección determinada es proporcional al cambio de la concentración del soluto en esa dirección. La ecuación para esta ley es:
- 16. INGENIERIA QUIMICA. Transporte - Difusión 16 Difusión (visión estática)Movimiento molecular en la difusión mayorno.demoléculas→ Difusión en una superficie sólida
- 17. FACTORES QUE INFLUYEN EN LA DIFUSION INGENIERIA QUIMICA. Transporte - Difusión 17 TEMPERATURA DIFERENCIA DE CONCENTRACION DISTANCIA DE DIFUSION DIFUSION Y MATERIALES HUESPEDES