Estereoisomeria
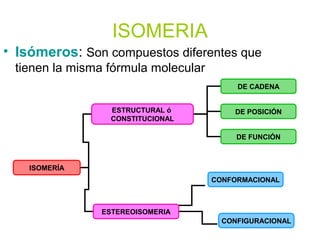
- 1. ISOMERIA • Isómeros: Son compuestos diferentes que tienen la misma fórmula molecular ISOMERÍA ESTRUCTURAL ó CONSTITUCIONAL ESTEREOISOMERIA DE CADENA DE POSICIÓN DE FUNCIÓN CONFORMACIONAL CONFIGURACIONAL
- 2. QUIRALIDAD Las manos derecha e izquierda son entre si imágenes especulares no superponibles Cuando un objeto tiene una imagen especular no superponible se dice que es QUIRAL
- 3. QUIRALIDAD Los objetos que tienen imágenes especulares superponibles son aquirales
- 13. COMPAREMOS…………… AQUIRAL TIENE PLANO DE SIMETRIA
- 14. Las moléculas también pueden ser quirales Cuando una molécula no tiene plano de simetría existe una imagen especular no superponible de la misma. Cuando esto ocurre se dice que la molécula es quiral y ópticamente activa, Una molécula ópticamente activa desvía el plano de polarización de la luz polarizada
- 15. POLARIMETRO Desviación hacia laDesviación hacia la derechaderecha dextrorrotatoria (+) Desviación hacia laDesviación hacia la izquierdaizquierda levorrotatoria (-)
- 16. ROTACION ESPECIFICA El ángulo de rotación observado depende de la estructura del compuesto pero también de la longitud de la celda, de la concentración de la muestra, de la temperatura y de la longitud de onda de la luz irradiada [α] = α (observed) c • l Rotación específica c es la concentración en g/mL y l es la longitud de la celda en decímetros.
- 17. Qué características estructurales tiene que tener una molécula para tener actividad óptica? No tiene que tener plano de simetría y esto en muchos casos se debe a la presencia de carbonos asimétricos. Un carbono asimétrico es un carbono con hibridación sp3 que está unido a 4 sustituyentes distintos.
- 19. ENANTIOMEROS • Se llama enantiómeros a dos isómeros que se relacionan entre si por ser imágenes especulares no superponibles Los dos enantiómeros tienen todas las propiedades físicas idénticas (Punto de fusión, punto de ebullición, solubilidad, etc) La única propiedad en la que difieren es en el sentido de rotación del plano de la luz polarizada Cada uno de los enantiómeros gira el plano de polarización de la luz el mismo ángulo pero en direcciones opuestas. Uno es dextrorrotatorio y el otro levorrotatorio.
- 20. NOMENCLATURA (R,S) • Cada una de las moléculas que conforman el par de enantiómeros debe recibir algún nombre adicional para distinguirlas entre si. El sistema más aceptado para nombrar la configuración de un centro estereogénico es la denominada convención de Cahn, Ingold y Prelog, que asigna una letra R o S a cada centro estereogénico de una molécula quiral. :
- 21. NOMENCLATURA (R,S) Las reglas que hay que seguir para asignar una configuración R o S son las siguientes: 1º. Cada átomo unido al carbono asimétrico recibe un número 1, 2, 3 ó 4. El 1 se asigna al grupo de mayor prioridad y el 4 al de menor prioridad. La prioridad se establece según el número atómico: el átomo de mayor prioridad es el de mayor número atómico.
- 22. 2º. Una vez asignado el orden de prioridad se mira el carbono estereogénico desde el lado opuesto al grupo de menor prioridad. Si el orden de prioridades decreciente de los restantes grupos representa una secuencia en el sentido de las agujas del reloj se asigna al estereocentro la configuración R (rectus, derecha). Si la secuencia gira en el sentido opuesto a las agujas del reloj la configuración del estereocentro es S (sinister, izquierda). NOMENCLATURA (R,S)
- 23. NOMENCLATURA (R,S) Ejemplo 1: Asignación de la configuración R o S de los dos enantiómeros del 1- cloro-1-fluoroetano. La representación tridimensional de los dos enantiómeros del 1- cloro-1- fluoroetano es la siguiente:
- 24. NOMENCLATURA (R,S) 1º. El orden de prioridad de los grupos unidos al carbono estereogénico en base al número atómico es, de mayor a menor, Cl > F > C > H. Por tanto, el orden de prioridad será Cl (1º), F (2º), C (3º) y H (4º).
- 26. NOMENCLATURA (R,S) • IMPORTANTE!!!!!!! El sentido de rotación de la luz polarizada no tiene ninguna relación con la nomenclatura (R,S). El valor del ángulo de rotación y su sentido es experimental. No se puede predecir. Una molécula con configuración R podría ser levógira ó dextrógira y no se puede conocer ese dato si no se analiza la muestra en un polarímetro.
- 27. PROYECCIONES DE FISHER La proyección de Fischer es una forma de representar una molécula tridimensional en una superficie bidimensional. Para transformar la representación tridimensional de una molécula con un estereocentro en una proyección de Fischer se siguen los siguientes pasos: 1. Se orienta la estructura de manera que el carbono del esterocentro quede contenido en el plano del papel, dos de los sustituyentes se dirijan hacia el observador y los otros dos sustituyentes se alejen del observador:
- 28. PROYECCIONES DE FISHER 2. Con la orientación correcta se proyectan los dos enlaces que se acercan al observador en la horizontal y los dos enlaces que se alejan del observador en la vertical:
- 30. PROYECCIONES DE FISHER Si el grupo de menor prioridad está en la horizontal, esto significa que espacialmente se está dirigiendo al observador. Como las reglas de Cahn –Ingold y Prelog dicen que debe estar alejándose, la configuración real es la opuesta a la obtenida
- 32. COMPUESTOS CON MAS DE UN CARBONO ASIMETRICO Es decir que si un compuesto tiene dos carbonos asimétricos tiene un máximo de 4 esteroisómeros
- 33. DIASTEREOMEROS Se denomina diastereómeros a todos los estereoisómeros que no son enantiómeros Los diastereómeros tienen todas sus propiedades físicas diferentes.
- 34. COMPUESTOS CON MAS DE UN CARBONO ASIMETRICO
- 35. COMPUESTOS MESO Se llaman compuestos meso a aquellos compuestos que teniendo carbonos asimétricos tienen una imagen especular superponible, es decir que no tienen enantiómero ni presentan actividad óptica. Esto se debe a que tienen un plano interno de simetría
- 36. MEZCLAS RACÉMICAS Una mezcla racémica contiene igual cantidad de los dos enantiómeros de una molécula. Por lo tanto la mezcla no presentará Actividad Optica. Sus propiedades fisicas (P. de fusión, ebullición, etc, pueden ser diferentes a las de los enantiómeros)
- 37. SEPARACION DE ENANTIOMEROS RCOOH + H2N-R' R-COONH3-R' (+) RCOOH (+) R-COONH3-R' (+) + (+) H2N-R' (-) RCOOH (-) R-COONH3-R' (+) enantiómeros diastereoisómeros Se hace reaccionar la mezcla con un reactivo ópticamente activo y puro. Se genera así una mezcla de diastereoisómeros, que tienen distintas propiedades físicas y se los pueden separar por medios físicos como cristalización, destilación fraccionada, cromatografía, etc.. Existen también fases quirales para cromatografía
- 38. ISOMERÍA cis-trans La isomería cis-trans se puede observar en moléculas cíclicas o en moléculas que presenten dobles enlaces. • Isomería cis-trans en ciclos Los cicloalcanos tienen dos “caras” o lados debido al plano que contiene el esqueleto carbonado; cuando en el ciclo hay dos sustituyentes en átomos de carbono distintos, existen dos isómeros. Si los sustituyentes se encuentran del mismo lado del plano es el isómero cis, y si están en lados opuestos es el isómero trans. trans-1,2-dimetilciclopropano H H CH3 H H CH3 Los grupos metilo en lados opuestos del plano cis-1,2-dimetilciclopropano H H CH3 H CH3 H Los grupos metilo en el mismo lado del plano
- 39. • Isomería cis-trans en alquenos Una característica del doble enlace es su rigidez que impide la libre rotación, por lo que se reduce los posibles intercambios de posición que pueden sufrir los átomos de una molécula y surge así un nuevo tipo de isomería. La isomería cis-trans en los alquenos se da cuando los sustituyentes en cada uno de los carbonos del doble enlace son distintos. C C H H H CH3 C C H CH3 H CH3 Dos sustituyentes distintos: H y CH3 Dos sustituyentes distintos: H y CH3 En este compuesto hay isomería geométrica, pues se cumple la condición en ambos carbonos. En este carbono hay dos sustituyentes iguales, por lo tanto, en este compuesto no hay isomería geométrica.
- 40. Un estereoisómero es cis cuando los dos hidrógenos están del mismo lado del doble enlace. Un estereoisómero es trans cuando los dos hidrógenos están en lados opuestos del doble enlace C C H CH3 H CH3 Del mismo lado del plano C C H CH3 CH3 H De lados opuestos del plano cis-2-buteno trans-2-buteno
- 41. MOLECULAS DISIMÉTRICAS • Poseen actividad óptica porque no tienen plano de simetría pero no tienen carbonos asimétricos. Ejemplos: alenos y bifenilos
- 42. ALENOS . El átomo de carbono central de un aleno tiene hibridación sp y es lineal, mientras que los átomos de carbono de los extremos tienen hibridación sp2 y son trigonales. Los alenos son quirales cuando cada uno de los átomos de carbono tienen al final dos sustituyentes diferentes Alenos: Cuando los dos sustituyentes sobre cada átomo de carbono sp2 es distinto. La molécula no tiene plano de simetría porque los sustituyentes quedan en planos perpendiculares.
- 44. BIFENILOS
- 45. BIFENILOS Estas dos conformaciones, que carecen de plano de simetría, son entre sí imágenes especulares no son superponibles