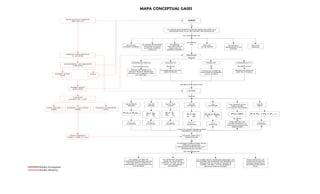
Mapa conceptual gases
- 1. MAPA CONCEPTUAL GASES EDAD ANTIGUA GRIEGOS (600-300 A.C) GAS Es Un estado de la materia donde las partículas están muy separadas entre sí por las fuerzas intermoleculares Se caracterizan por Se definen Su fuerza de repulsión El espacio por Su forma y Son muy Se difunden Son muy volumen variables molecular es mayor intermolecular es compresibles elásticos rápidamente y con que la de cohesión mayor que en facilidad molecular líquidos y sólidos PERÍODO RENACENTISTA Magnitudes (s. XVI-XVII) Que son Cantidad de Gas (n) Volumen (V) Presión (P) Temperatura (T°) JAN BAPTISTA VAN HELMONT (1580-1644) Se da por Es Se define como Se expresa como Número de moles (n) ó El recipiente en el cual Medida del grado de Fuerza por unidad de Número Real de Moléculas está contenido calor de un cuerpo Área sobre el recipiente (Número de Avogadro), dado ROBERT FLUDD FILÓN que lo contiene en masa (g). (1617) Se relacionan entre sí por ROBERT BOYLE (1627-1691) LEYES Que son FLOGISTO principios del s. XVIII Ley de Boyle- Ley de Ley de Gay- Ley de Ley Ley General de los Ley de Mariotte Charles Lussac Avogadro Combinada Gases Ideales Dalton JHON DALTON CHARLES Y GAY-LUSSAC AMADEO AVOGADRO o Ecuación de Estado (1808) (1809) (1811) P1V1= P2V2 V 1= V 2 P1= T1 V 1= V 2 P1V1= P2V2 PV= nRT PT= PA + PB + PC +… T1 T2 P2 T2 n1 n2 T1 T2 Se utiliza A T° y n A P y n A V y n Para calcular una A V y T° A P y T° A n constantes constantes constantes muestra de gas en un constantes constantes constante conjunto de condiciones determinado Todos los Gases Ideales pueden estudiarse a través de EDAD MODERNA TEORÍA CINÉTICO- Finales s. XVIII- y s. XIX MOLECULAR Es La energía cinética media de las moléculas gaseosas, directamente proporcional a la T° absoluta de la muestra Se caracteriza por Los gases constan de Las moléculas de gases La colisión de las moléculas gaseosas con Entre colisiones, las moléculas individuales que son están en movimiento las paredes del recipiente son elásticas; la moléculas no ejercen muy pequeñas y están muy contínuo, al azar, en línea energía total se conserva durante la fuerzas repulsivas ni separadas en comparación con recta con velocidades colisión; es decir, no hay pérdida ni atractivas unas sobre Núcleo Conceptual sus tamaños cambiantes ganancia neta de energía otras. Núcleo Histórico
