Formación y representación de reacciones químicas
•Descargar como DOCX, PDF•
0 recomendaciones•2,809 vistas
Mapa conceptual
Denunciar
Compartir
Denunciar
Compartir
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Similar a Formación y representación de reacciones químicas
Similar a Formación y representación de reacciones químicas (20)
REACCIONES QUIMICAS COTIDIANAS - MODULO TP INICIO.PPT

REACCIONES QUIMICAS COTIDIANAS - MODULO TP INICIO.PPT
tiposdereaccionesqumicas-150503194707-conversion-gate02.pdf

tiposdereaccionesqumicas-150503194707-conversion-gate02.pdf
Último
Último (20)
Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...

Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...
SELECCIÓN DE LA MUESTRA Y MUESTREO EN INVESTIGACIÓN CUALITATIVA.pdf

SELECCIÓN DE LA MUESTRA Y MUESTREO EN INVESTIGACIÓN CUALITATIVA.pdf
Planificacion Anual 2do Grado Educacion Primaria 2024 Ccesa007.pdf

Planificacion Anual 2do Grado Educacion Primaria 2024 Ccesa007.pdf
TECNOLOGÍA FARMACEUTICA OPERACIONES UNITARIAS.pptx

TECNOLOGÍA FARMACEUTICA OPERACIONES UNITARIAS.pptx
Planificacion Anual 4to Grado Educacion Primaria 2024 Ccesa007.pdf

Planificacion Anual 4to Grado Educacion Primaria 2024 Ccesa007.pdf
cortes de luz abril 2024 en la provincia de tungurahua

cortes de luz abril 2024 en la provincia de tungurahua
MAYO 1 PROYECTO día de la madre el amor más grande

MAYO 1 PROYECTO día de la madre el amor más grande
texto argumentativo, ejemplos y ejercicios prácticos

texto argumentativo, ejemplos y ejercicios prácticos
Caja de herramientas de inteligencia artificial para la academia y la investi...

Caja de herramientas de inteligencia artificial para la academia y la investi...
Formación y representación de reacciones químicas
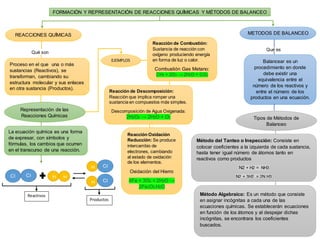
- 1. FORMACIÓN Y REPRESENTACIÓN DE REACCIONES QUÍMICAS Y MÉTODOS DE BALANCEO REACCIONES QUÍMICAS Qué son Proceso en el que una o más sustancias (Reactivos), se transforman, cambiando su estructura molecular y sus enlaces en otra sustancia (Productos). Representación de las Reacciones Químicas La ecuación química es una forma de expresar, con símbolos y fórmulas, los cambios que ocurren en el transcurso de una reacción. CI CI H H H H CI CI Reactivos Productos EJEMPLOS Reacción de Combustión: Sustancia de reacción con oxígeno produciendo energía en forma de luz o calor. Combustión Gas Metano: CH4 + 2O2 → 2H2O + CO2 Reacción de Descomposición: Reacción que implica romper una sustancia en compuestos más simples. Descomposición de Agua Oxigenada: 2H2O2 → 2H2O + O2 Reacción Oxidación Reducción: Se produce intercambio de electrones, cambiando al estado de oxidación de los elementos. Oxidación del Hierro 4Fe + 3O2 + 2H2O → 2Fe2O3.H2O METODOS DE BALANCEO Qué es Balancear es un procedimiento en donde debe existir una equivalencia entre el número de los reactivos y entre el número de los productos en una ecuación. Tipos de Métodos de Balanceo Método del Tanteo o Inspección: Consiste en colocar coeficientes a la izquierda de cada sustancia, hasta tener igual número de átomos tanto en reactivos como productos N2 + H2 = NH3 N2 + 3H2 = 2N H3 Método Algebraico: Es un método que consiste en asignar incógnitas a cada una de las ecuaciones químicas. Se establecerán ecuaciones en función de los átomos y al despejar dichas incógnitas, se encontrara los coeficientes buscados.