Clase termo 10
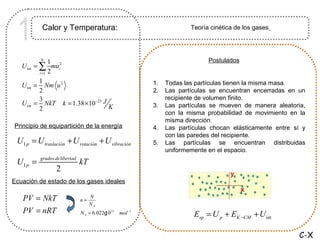
- 1. 1 Calor y Temperatura: Teoría cinética de los gases N 1 Postulados U int = ∑ mui2 i =1 2 1 1. Todas las partículas tienen la misma masa. U int = Nm u 2 2 2. Las partículas se encuentran encerradas en un 3 recipiente de volumen finito. U int = NkT k = 1.38 ×10 −23 J 3. Las partículas se mueven de manera aleatoria, 2 K con la misma probabilidad de movimiento en la misma dirección. Principio de equipartición de la energía 4. Las partículas chocan elásticamente entre sí y con las paredes del recipiente. U1 p = U traslación + U rotación + U vibración 5. Las partículas se encuentran distribuidas uniformemente en el espacio. grados delibertad U1 p = kT 2 Ecuación de estado de los gases ideales PV = NkT n= N NA PV = nRT N A = 6.022g 23 10 mol −1 Esp = U p + EK −CM + U int C-X
- 2. 2 Calor y Temperatura: Teoría cinética de los gases 1. Fuerza ejercida por una partícula r r ∆p 2mu x F1 p = = ∆t ∆t 2. Fuerza total sobre la pared r r N FT = n p F1 p = mA u x 2 V 3. Presión ejercida por el gas r F N 1N p = = m ux = 2 m u2 A V 3V Ecuación de estado de los gases ideales 4. De la energía interna (diapositiva anterior) pV = NKT NK = nR m u 2 = 3 NkT pV = nRT C-X
- 3. 3 Calor y Temperatura: Procesos y Trabajo 1. Trabajo realizado por el sistema W = ∫ Fdx = ∫ pAdx = ∫ pdV 2. Trabajo realizado sobre el sistema W = − ∫ Fdx = − ∫ pAdx = − ∫ pdV C-X
- 4. 4 Calor y Temperatura: 1era Ley de la Termodinámica Energía térmica: Está asociada al movimiento ∆U = ∆Q + ∆W aleatorio de las partículas. dU = δ Q − pdV (Mecanismos de intercambio Calor y Trabajo) La variación de energía interna del sistema = al calor cedido al sistema + el trabajo realizado sobre el sistema ∆Q Capacidad calorífica C= Fracaso de la equipartición de la energía ∆T C 1 ∆Q Capacidad calorífica molar c= = n n ∆T dU dU dV CV = Cp = +p dT dT dT C p = CV + nR pdV = nRdT C-X
- 5. 4 Calor y Temperatura: Resumen Expansión adiabática ∆U = ∆Q + ∆W CV dT 0 − pdV dU = δ Q − pdV dU = δ Q + dW 3 Cp γ= Gas monoatómico CV = nR 2 γ −1 CV TV = cte Gas diatómico C = 5 nR V 2 pV γ = cte Procesos ∆U ( J ) W (J ) Q( J ) V2 V2 Isotérmico CV ∆T −nRT ln nRT ln V1 V1 Isobárico CV ∆T − p∆V C p ∆T Isocórico CV ∆T 0J CV ∆T Adiabático CV ∆T CV ∆T 0J C-X
- 6. 4 Calor y Temperatura: Resumen Expansión adiabática ∆U = ∆Q + ∆W CV dT 0 − pdV dU = δ Q − pdV dU = δ Q + dW 3 Cp γ= Gas monoatómico CV = nR 2 γ −1 CV TV = cte Gas diatómico C = 5 nR V 2 pV γ = cte Procesos ∆U ( J ) W (J ) Q( J ) V2 V2 Isotérmico CV ∆T −nRT ln nRT ln V1 V1 Isobárico CV ∆T − p∆V C p ∆T Isocórico CV ∆T 0J CV ∆T Adiabático CV ∆T CV ∆T 0J C-X