Contenidos a dictar entre agosto y septiembre
•Descargar como DOCX, PDF•
0 recomendaciones•163 vistas
Contenidos conceptuales y procedimentales a evaluar en revisión septiembre 2014
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Más contenido relacionado
Destacado
Destacado (20)
Planificacion del san josé 4° año a y d iii lapso académico 2014

Planificacion del san josé 4° año a y d iii lapso académico 2014
Guia de reactivos impuros y rendimiento de reacción

Guia de reactivos impuros y rendimiento de reacción
Guia de unidades físicas y químicas de concentración de soluciones

Guia de unidades físicas y químicas de concentración de soluciones
Guia de unidades físicas y químicas de concentración de soluciones

Guia de unidades físicas y químicas de concentración de soluciones
Guia de unidades físicas y químicas de concentración de soluciones

Guia de unidades físicas y químicas de concentración de soluciones
Mapa conceptual de concentración de soluciones químicas

Mapa conceptual de concentración de soluciones químicas
Guia de unidades físicas y químicas de concentración de soluciones

Guia de unidades físicas y químicas de concentración de soluciones
Planificacion del área de química 4° año a y d. Primer lapso académico

Planificacion del área de química 4° año a y d. Primer lapso académico
Más de U.E.N "14 de Febrero"
Cronograma del I momento ETA Osmar Uridan Sánchez ParedesCronograma I momento Escuela Técnica Asistencial Dr. Osmar Uridan Sánchez Par...

Cronograma I momento Escuela Técnica Asistencial Dr. Osmar Uridan Sánchez Par...U.E.N "14 de Febrero"
Más de U.E.N "14 de Febrero" (20)
Formato para planificar orientación y convivencia. 

Formato para planificar orientación y convivencia.
instrumento para evaluar orientación y convivencia...P.C.R.P

instrumento para evaluar orientación y convivencia...P.C.R.P
Cronograma I momento Escuela Técnica Asistencial Dr. Osmar Uridan Sánchez Par...

Cronograma I momento Escuela Técnica Asistencial Dr. Osmar Uridan Sánchez Par...
Último
Centros Multigrados Procedimientos para la planificación en los Centros Educativos tipo V ( multi...

Procedimientos para la planificación en los Centros Educativos tipo V ( multi...Katherine Concepcion Gonzalez
Último (20)
🦄💫4° SEM32 WORD PLANEACIÓN PROYECTOS DARUKEL 23-24.docx

🦄💫4° SEM32 WORD PLANEACIÓN PROYECTOS DARUKEL 23-24.docx
RESOLUCIÓN VICEMINISTERIAL 00048 - 2024 EVALUACION

RESOLUCIÓN VICEMINISTERIAL 00048 - 2024 EVALUACION
PINTURA DEL RENACIMIENTO EN ESPAÑA (SIGLO XVI).ppt

PINTURA DEL RENACIMIENTO EN ESPAÑA (SIGLO XVI).ppt
Procedimientos para la planificación en los Centros Educativos tipo V ( multi...

Procedimientos para la planificación en los Centros Educativos tipo V ( multi...
Código Civil de la República Bolivariana de Venezuela

Código Civil de la República Bolivariana de Venezuela
PP_Comunicacion en Salud: Objetivación de signos y síntomas

PP_Comunicacion en Salud: Objetivación de signos y síntomas
Los avatares para el juego dramático en entornos virtuales

Los avatares para el juego dramático en entornos virtuales
Prueba de evaluación Geografía e Historia Comunidad de Madrid 2º de la ESO

Prueba de evaluación Geografía e Historia Comunidad de Madrid 2º de la ESO
Novena de Pentecostés con textos de san Juan Eudes

Novena de Pentecostés con textos de san Juan Eudes
Prueba de evaluación Geografía e Historia Comunidad de Madrid 4ºESO

Prueba de evaluación Geografía e Historia Comunidad de Madrid 4ºESO
Contenidos a dictar entre agosto y septiembre
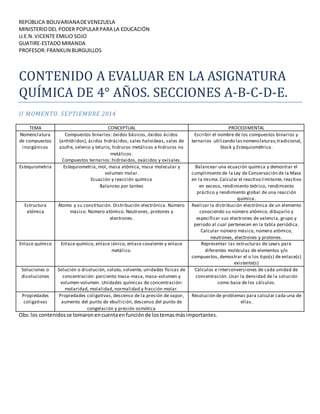
- 1. REPÚBLICA BOLIVARIANADEVENEZUELA MINISTERIODEL PODER POPULARPARA LA EDUCACIÓN U.E.N.VICENTE EMILIO SOJO GUATIRE-ESTADOMIRANDA PROFESOR:FRANKLIN BURGUILLOS CONTENIDO A EVALUAR EN LA ASIGNATURA QUÍMICA DE 4° AÑOS. SECCIONES A-B-C-D-E. II MOMENTO. SEPTIEMBRE 2014 TEMA CONCEPTUAL PROCEDIMENTAL Nomenclatura de compuestos inorgánicos Compuestos binarios: óxidos básicos, óxidos ácidos (anhídridos), ácidos hidrácidos, sales haloideas, sales de azufre, selenio y telurio, hidruros metálicos e hidruros no metálicos. Compuestos ternarios: hidróxidos, oxácidos y oxisales. Escribir el nombre de los compuestos binarios y ternarios utilizando lasnomenclaturas;tradicional, Stock y Estequiométrica. Estequiometria Estequiometria, mol, masa atómica, masa molecular y volumen molar. Ecuación y reacción química Balanceo por tanteo Balancear una ecuación química y demostrar el cumplimiento de la Ley de Conservación de la Masa en la misma.Calcular el reactivo limitante, reactivo en exceso, rendimiento teórico, rendimiento práctico y rendimiento global de una reacción química. Estructura atómica Átomo y su constitución. Distribución electrónica. Número másico. Número atómico. Neutrones, protones y electrones. Realizar la distribución electrónica de un elemento conociendo su número atómico, dibujarlo y especificar sus electrones de valencia, grupo y periodo al cual pertenecen en la tabla periódica. Calcular número másico, número atómico, neutrones, electrones y protones. Enlace químico Enlace químico, enlace iónico, enlace covalente y enlace metálico. Representar las estructuras de Lewis para diferentes moléculas de elementos y/o compuestos, demostrar el o los tipo(s) de enlace(s) existente(s) Soluciones o disoluciones Solución o disolución, soluto, solvente, unidades físicas de concentración: porciento masa-masa, masa-volumen y volumen-volumen. Unidades químicas de concentración: molaridad, molalidad, normalidad y fracción molar. Cálculos e interconversiones de cada unidad de concentración. Usar la densidad de la solución como base de los cálculos. Propiedades coligativas Propiedades coligativas, descenso de la presión de vapor, aumento del punto de ebullición, descenso del punto de congelación y presión osmótica Resolución de problemas para calcular cada una de ellas. Obs:los contenidosse tomaronencuentaenfunciónde lostemasmásimportantes.
