Sndrome de donohue
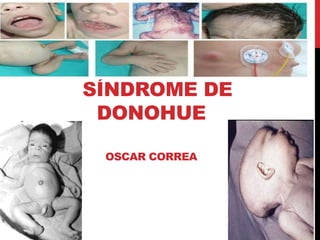
- 1. SÍNDROME DE DONOHUE OSCAR CORREA
- 2. SÍNDROME DE DONOHUE Raro síndrome de extrema resistencia a la insulina recesivo autosomal debido a mutaciones en el dominio de unión del RECEPTOR DE INSULINA. Las características clínicas incluyen grave restricción del crecimiento intrauterino y postnatal, rasgos faciales caracterizados por orejas alargadas de lóbulo ensanchado, labios delgados, alteraciones genitales y muerte prematura. Un trastorno autosómico recesivo significa que deben estar presentes dos copias de un gen anormal para que se desarrolle la enfermedad o el rasgo. Biblioteca Virtual en Salud, Cuba. http://www.bvscuba.sld.cu/php/decsws.php?lang=es&tree_id=C16.320.215&page=info
- 3. SÍNDROME DE DONOHUE ASPECTOS MOLECULARES El síndrome de Donohue, está causado por mutaciones recesivas en el gen receptor de insulina (INSR) que se localiza en el cromosoma 19p13.2 El receptor de insulina se localiza en la membrana plasmática y pertenece a la familia de los receptores de factores de crecimiento, siendo activado por la insulina. Por tanto, las mutaciones del gen INSR producen resistencia a la insulina. Biblioteca Virtual en Salud, Cuba. http://www.bvscuba.sld.cu/php/decsws.php?lang=es&tree_id=C16.320.215&page=info
- 4. ANTECEDENTES CLÍNICOS Donohue describió en 1948 un niños que tenia En el año 1954, se describió un cuadro unas características clínico en dos hermanos consistente en un faciales particulares y un grave retraso del crecimiento intrauterino, conjunto de alteraciones muerte temprana (los hermanos vivieron fenotípicas, lo que 46 y 66 días), y un aspecto facial que les denomino recordaba al de un gnomo, y por ello lo "disendocrinia” denominaron síndrome de Leprechaunismo. Paciente a las 2 semanas de vida. Fenotipo característico con macrogenitalismo, distensión abdominal, manos y pies grandes.
- 5. CARACTERÍSTICAS FÍSICAS (FENOTIPO) Crecimiento Grave retraso crecimiento prenatal y postnatal Cráneo y cara Dismorfias faciales; ojos, orejas y boca grandes -Extremidades Pies y manos relativamente grandes -Abdomen Distendido -Mamilas Agrandadas y protuberantes -Genitales Relativamente grandes -Piel Reducción de grasa subcutánea (lipoatrofia) Pelo abundante (hipertricosis), y acantosis nigricans Por Anatomía Anomalías de gónadas patológica Otras Hiperinsulinemia e hipoglucemia
- 6. EPIDEMIOLOGÍA DEL S. DE DONOHUE Se considera que este síndrome es extremadamente poco frecuente, habiéndose estimado que se presenta en 1 niño por cada 4 millones. En el ECEMC, se ha observado en 1 niño por cada 1.231.567 de nacimientos.
- 7. CARACTERÍSTICAS CLÍNICAS
- 8. Insulinemia Síndrome. De Donohue Hipoglicemia Resistencia a la Insulina hiperandrogenismo *El síndrome se ha considerado dentro del grupo de endocrinopatías llamados HAIR-AN (acrónimo de Hyperandrogenism, Insulin Resistence, Acanthosis Nigricans),
- 9. INSR Glicoproteína 2 Sub-Unidades Alfa tetramérica y 2 Sub-unidades transmembrana Beta Permite la translocación Produce la activación Consta de 1.355 de las proteínas intracelular de la aminoácidos transportadoras de tirosincinasa glucosa
- 10. La insulina inicia su Induce un péptido El receptor insulínico acción metabólica transportador es un tetrámero con uniéndose a desde un pool dos subunidades alfa intracelular hacia la receptores de y dos beta membrana celular.( membrana celular. GLUT-4 ).
- 13. DEFINICIÓN DE INSULINO- RESISTENCIA Es un estado metabólico en el cual las concentraciones fisiológicas de insulina producen respuesta biológica anormal. Se traduce en concentraciones plasmáticas de insulina más elevadas que las de una población control, para niveles similares de glicemia. La respuesta fisiológica a una menor entrada de glucosa a las células se traduce en aumento de secreción de insulina
- 14. Efectos Finales de la Insulina Síntesis de glicógeno Síntesis de Lípidos Síntesis de proteínas Factores de Transcripción Síntesis de Proteínas
- 16. 1 MATGGRRGAAAAPLLVAVAALLLGAAGHLY G GEVCPGMDIRNNL Amino ácido 46 TRLHELENCSVIEGHLQILLMFKTRPEDFRDLSFPKLIMIT R YLLLFRVYGLESLKDL abreviaturas 103 FPNLTVIRGSRLFFNYALVIFEMVHLKELGLYNLMNITRGSVRIEKNNELCYLATIDW 163 SRILDSVEDNYIVLNKDDNEECGDICPGTAKGKTNCPATVINGQFVE CWTHSHCQKV H Un alanina 220 CPTICKSHGCTAEGLCCHSECLGNCSQPDDPTKCVACRNFYLDGRCVETCPPPYYHFQ Arginina R 277 DWRCVNFSFCQDLHHKCKNSRRQGCHQYVIHNNKCIPECPSGYTMNSSNLLCTPCLGP Asparagina N 334 CPKVCHLLEGEKTIDSVTSAQELRGCTVINGSLIINIR R GNNLAAELEANLGLIEEIS Aspártico ácido D 391 GYLKIRRSYALVSLSFFRKLRLIRGETLEIGNYSFYALDNQNLRQLWDWSKHNLTITQ Cisteína C 448 GKLFFHYNPKLCLSEIHKMEEVSGTKGRQERNDIALKTNGDQASCENELLKFSYIRTS Ácido glutámico E 505 FDKILLRWEPYWPPDFRDLLGFMLFYKEAPYQNVTEFDGQDACGSNSWTVVDIDPPLR Glutamina Q 562 SNDPKSQNHPGWLMRGLKPWTQYAIFVKTLVTFSDERRTYGAKSDIIYVQTDATNPSV Glicina G 619 PLDPISVSNSSSQIILKWKPPSDPNGNITHYLVFWERQAEDSELFELDYCLKGLKLPS Histidina H 676 RTWSPPFESEDSQKHNQSEYEDSAGECCSCPKTDSQILKELEESSFRKTFEDYLHNVV Isoleucina L ILeucine 733 FVPRPSRKRRSLGDVGNVTVAVPTVAAFPNTSSTSVPTSPEEHRPFEKVVNKESLVIS Lisina K 790 GLRHFTGYRIELQACNQDTPEERCSVAAYVSARTMPEAKADDIVGPVTHEIFENNVVH Metionina M 847 LMWQEPKEPNGLIVLYEVSYRRYGDEELHLCVSRKHFALERGCRLRGLSPGNYSVRIR Fenilalanina F 904 ATSLAGNGSWTEPTYFYVTDYLDVPSNIAKIIIGPLIFVFLFSVVIGSIYLFLRKRQP Prolina P 961 DGPLGPLYASSNPEYLSASDVFPCSVYVPDEWEVSREKITLLRELGQGSFGMVYEGNA Serina S 1018 RDIIKGEAETRVAVKTVNESASLRERIEFLNEASVMKGFTCHHVVRLLGVVSKGQPTL Treonina T 1075 VVMELMAHGDLKSYLRSLRPEAENNPGRPPPTLQEMIQMAAEIADGMAYLNAKKFVHR Triptófano W 1132 DLAARNCMVAHDFTVKIGDFGMTRDIYETDYYRKGGKGLLPVRWMAPESLKDGVFTTS Y tirosina 1189 SDMWSFGVVLWEITSLAEQPYQGLSNEQVLKFVMDGGYLDQPDNCPERVTDLMRMCWQ Valina V 1246 FNPKMRPTFLEIVNLLKDDLHPSFPEVSFFHSEENKAPESEELEMEFEDMENVPLDRS 1303 SHCQREEAGGRDGGSSLGFKRSYEEHIPYTHMNGGKKNGRILTLPRSNPS número de variantes alélicas Cambio de la secuencia de aminoácidos .0014 H-209-a-R .0020 G-31 a una .0022 R-372 a codón de parada .0025 R-86 a P Fuente: http://www.ncbi.nlm.nih.gov/nuccore/NM_001079817.1?ordinalpos=2&itool=EntrezSystem2.PEntrez.Sequence.Sequence_ResultsPanel.Sequence_R VDocSum
- 17. 1 gagaaggacg gggtggccgc agcgcctctt ctcggagcat cgcggccccc gacccccgcg 61 gcgcgctctg ggccagcgcc atccgaggag GGA ca cccgcagcca gcgct tggccaccgg 121 gggccggcgg ccgcgccgct ggggcggcgg gctggtggcg tgctactggg gtggccgcgc 181 cgccgcgggc ccggagaggt cacctgtacc gtgtcccggc ggaacaacct atggatatcc 241 cactaggttg catgagctgg agaattgctc tgtcatcgaa agatactctt ggacacttgc 301 gatgttcaaa acgaggcccg aagatttccg tcatcatgat ttccccaaac agacctcagt 361 ttgctgctct cactgattac tgggctcgag tccgggtcta agcctgaagg acctgttccc 421 caacctcacg gtcatccggg gatcacgact gttctttaac tcatc TCGA g tacgcgctgg 481 ctcaaggaac tcggcctcta gatggttcac caacctgatg ggggttctgt aacatcaccc 541 aagaacaatg agctctgtta ccgcatcgag cttggccact cccgtatcct atcgactggt 601 ggattccgtg gaacaaagat acatcgtgtt gaggataatt gacaacgagg agtgtggaga 661 catctgtccg g cac ccgcga agggcaagac caactgcccc gccaccgtca tcaacgggca 721 gtttgtcgaa cgatgttgga ctcatagtca ctgccagaaa gtttgcccga ccatctgtaa 781 tgcaccgccg gtcacacggc aaggcctctg gagtgcctgg ttgccacagc gcaactgttc 841 tcagcccgac gaccccacca agtgcgtggc ctgccgcaac acggcaggtg ttctacctgg 901 tgtggagacc tgcccgcccc cgtactacca cttccaggac tgaacttcag tggcgctgtg 961 cttctgccag acaaatgcaa gacctgcacc gaactcgcgg gccaccagta aggcagggct 1021 cgtcattcac aacaacaagt gcatccctga gtgtccctcc gggtacacga tgaattccag 1081 gcctgggtcc tgcaccccat caacttgctg ctgtcccaag tcctagaagg gtgtgccacc 1141 atcgactcgg cgagaagacc tgacgtctgc ccaggagctc cgaggatgca ccgtcatcaa 1201 atcatcaaca cgggagtctg ttcgaggagg tagaagccaa gcagctgagc caacaatctg 1261 cctcggcctc attgaagaaa tttcagggta tctaaaaatc acgctctggt cgccgatcct 1321 tt gtcactttcc c ttccgga agttacgtct aaattgggaa gagaccttgg gattcgag número de variantes alélicas Cambio de la secuencia de ADN .0014 CAC-a-CGC sustitución en 672 pares de bases .0020 GGA a la AGA de sustitución en 93 pares de bases .0022 C-para-T sustitución de pares de bases en 1333 .0025 G a C sustitución en 476 pares de bases Fuente: http://www.ncbi.nlm.nih.gov/nuccore/NM_001079817.1?ordinalpos=2&itool=EntrezSystem2.PEntrez.Sequence.Sequence_Re
- 18. TRATAMIENTO Existen algunos casos que han sobrevivido tras ser tratados con: • factor de crecimiento de insulina-1 (IGF-1, siglas del inglés: insulin-like growth factor- 1), aunque se necesitan dosis relativamente altas para mantener suficientes niveles de IGF-1 en suero.
- 19. GRACIAS! :D
