Fuerzas intermoleculares original!
- 1. FUERZAS INTERMOLECULARES Grupo Nº: 5 Introducción a la Química
- 2. FUERZAS INTERMOLECULARES Las fuerzas intermoleculares son las fuerzas de atracción entre las moléculas que componen una sustancia molecular. Sus características son: -Se ponen de manifiesto cuando las moléculas están cerca unas de otras. Esto ocurre cuando la temperatura es suficientemente baja o la presión alta. -Cuanto mayor es la intensidad de estas fuerzas, mas energía se requiere para producir la fusión o la vaporización de las sustancias. – Cuanto mayor es la intensidad de las fuerzas de atracción que se ejercen entre las moléculas de una sustancia, mas elevados son su punto de función y de ebullición. Se clasifican en 3 tipos de fuerzas: 1-La fuerza de London que están presentes en todas las sustancias moleculares 2- Las fuerzas dipolares que solo existen en sustancias cuyas moléculas son polares 3- El enlace de hidrogeno que se presenta entre moléculas que contienen un átomo de hidrógenos unido a otro muy electronegativo.
- 3. FUERZAS DE LONDON Cuando una molécula se aproxima a otra se acercan sus nubes electrónicas, por lo tanto, como las cargas de igual signo se repelen los electrones se distribuyen en ambas, de manera de disminuir esta repulsión y originan así dipolos transitorios. Dependen de la facilidad con que se puede distorsionar la nube electrónica de una molécula. Esta facilidad de distorsión se denomina polarizabilidad, debido a que la deformación de la nube electrónica polariza la molécula, generando un dipolo transitorio. La intensidad de las fuerzas de London depende del tamaño de la nube electrónica y también de la geometría de las moleculas. Por Ej: La sustancia H2O que sus moleculas interaccionan por fuerzas de London, ya que es una sustancia molecular y todas estas sustancias contienen fuerzas de London.
- 4. FUERZAS DIPOLO DIPOLO Estas interacciones se producen solo entre moleculas polares. En este caso el dipolo es permanente. Esto permite que las moleculas interactúen entre si, además la intensidad de estas fuerzas es directamente proporcional a la polaridad de las moléculas. Por ej: Dióxido de Azufre que es una sustancia cuyas moléculas son polares ya que su diferencia de electronegatividad es mayor a 0,4 y por lo tanto tiene fuerzas de Dipolo-dipolo.
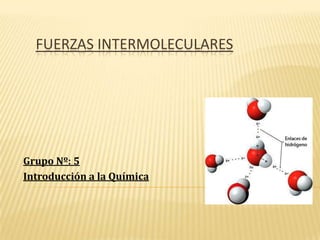
- 5. PUENTE DE HIDROGENO Este tipo de fuerza se da cuando en las moleculas existe un átomo de hidrogeno unido a un átomo de un elemento muy electronegativo (con el F, el O o el N). La diferencia tan marcada de electronegatividad hace que el par de electrones compartidos en el enlace sea mas intensamente atraído por el átomo mas electronegativo. Los puentes de Hidrogeno se producen en moléculas polares. Por Ej: El agua que tiene un átomo de hidrogeno y un átomo de oxigeno.
- 6. FUERZAS INTERMOLECULARES Y SOLUBILIDAD Una sustancia se disuelve en un disolvente cuando la polaridad de sus moléculas es similar a la de las moléculas del disolvente, por lo tanto las sustancias polares se disuelven en disolventes polares y la no polares en disolventes no polares. Algunos hidrocarburos no son solubles en agua, esto se debe a las fuerza de atracción intermoleculares. Las moléculas de agua son polares y las fuerzas por puente de hidrogeno son interacciones fuertes; mientras que las interacciones entre las moléculas de hidrocarburos son débiles. Las moléculas de hidrocarburos no polares y las moléculas de agua polares no se atraen y por lo tanto no son solubles.
- 7. Fuerzas intermoleculares y solubilidad CL4 Es una molécula no polar por lo tanto: • Tiene fuerzas de London ya que todas las sustancias moleculares la tienen •No tiene fuerza Dipolo-dipolo •No tiene puentes de Hidrogeno, porque no hay ningún hidrogeno unido a un elemento muy electronegativo. No es soluble en agua porque sus moléculas son no polares y las del agua son polares por lo tanto no pueden disolverse CH3Cl Es una molécula polar por lo tanto: •Tiene fuerzas de London ya que todas las sustancias moleculares la tienen •Tienen fuerzas Dipolo-dipolo. •No tiene puentes de hidrogeno. Es soluble en agua porque es una molécula polar al igual que las moléculas de agua por lo tanto puede diluirse. NH3 Es una molécula polar por lo tanto: •Tiene fuerzas de London ya que todas las sustancias moleculares la tienen. •Tienen fuerzas Dipolo-dipolo. •Tiene puente de hidrogeno ya que tiene un átomo de hidrogeno unido a un elemento muy electronegativo como es el N. Es soluble en agua porque es una molécula polar al igual que las moléculas de agua por lo tanto puede diluirse.