balanceo de ecuaciones por inspección
•
0 recomendaciones•1,580 vistas
aqui se genera un procedimiento para explicar como se balancea una ecuación por simple inspección o tanteo
Denunciar
Compartir
Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
Tutorial para comprender y ejercitar el método por tanteo para el balanceo de ecuaciones químicas.Balanceo de ecuaciones químicas por método de tanteo

Balanceo de ecuaciones químicas por método de tanteoEscuela Normal Superior Nro. 11 ¨Ricardo Levene¨
Recomendados
Tutorial para comprender y ejercitar el método por tanteo para el balanceo de ecuaciones químicas.Balanceo de ecuaciones químicas por método de tanteo

Balanceo de ecuaciones químicas por método de tanteoEscuela Normal Superior Nro. 11 ¨Ricardo Levene¨
Más contenido relacionado
La actualidad más candente
La actualidad más candente (19)
Balanceo De Ecuaciones QuíMicas Martha Delia RamíRez TéLlez

Balanceo De Ecuaciones QuíMicas Martha Delia RamíRez TéLlez
Hidrocarburos aromáticos (trabajo segundo periodo)

Hidrocarburos aromáticos (trabajo segundo periodo)
Guía práctica para Balanceo de ecuaciones químicas

Guía práctica para Balanceo de ecuaciones químicas
Similar a balanceo de ecuaciones por inspección
Similar a balanceo de ecuaciones por inspección (20)
Guía de apoyo nº1 q2 m 2013 estequiometría y leyes ponderales

Guía de apoyo nº1 q2 m 2013 estequiometría y leyes ponderales
Guía de apoyo nº1 q2 m 2013 estequiometría y leyes ponderales

Guía de apoyo nº1 q2 m 2013 estequiometría y leyes ponderales
Conservación de la masa en las transformaciones químicas

Conservación de la masa en las transformaciones químicas
Material complementario de ciencias naturales (la materia). docente..nomar a...

Material complementario de ciencias naturales (la materia). docente..nomar a...
Actividades de ajuste de reacciones quimicas resueltas

Actividades de ajuste de reacciones quimicas resueltas
balanceo de ecuaciones por inspección
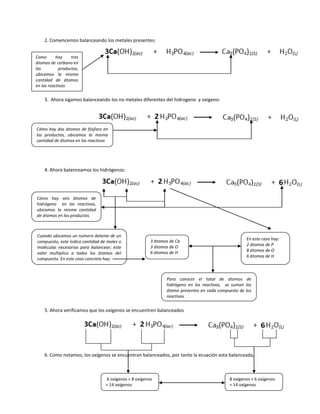
- 1. 2. Comencemos balanceando los metales presentes: Como hay tres átomos de carbono en los productos, ubicamos la misma cantidad de átomos en los reactivos 3. Ahora sigamos balanceando los no metales diferentes del hidrogeno y oxígeno: Cómo hay dos átomos de fósforo en los productos, ubicamos la misma cantidad de átomos en los reactivos 4. Ahora balanceamos los hidrógenos: Cómo hay seis átomos de hidrógeno en los reactivos, ubicamos la misma cantidad de átomos en los productos Cuando ubicamos un número delante de un 3 átomos de Ca En este caso hay: compuesto, este indica cantidad de moles o 3 átomos de O 2 átomos de P moléculas necesarias para balancear; este 6 átomos de H 8 átomos de O valor multiplica a todos los átomos del 6 átomos de H compuesto. En este caso concreto hay: Para conocer el total de átomos de hidrógeno en los reactivos, se suman los átomo presentes en cada compuesto de los reactivos. 5. Ahora verificamos que los oxígenos se encuentren balanceados 6. Como notamos, los oxígenos se encuentran balanceados, por tanto la ecuación esta balanceada. 6 oxígenos + 8 oxígenos 8 oxígenos + 6 oxígenos = 14 oxígenos = 14 oxígenos