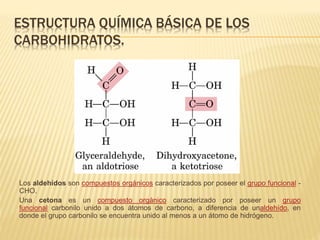
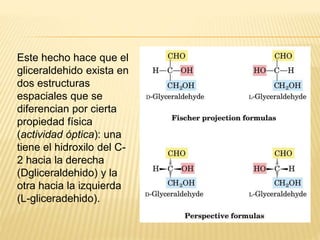
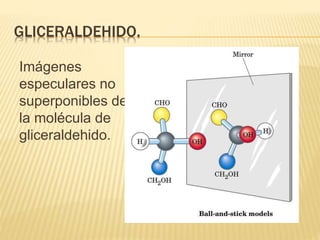
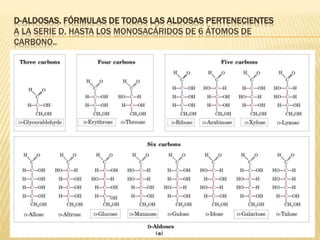
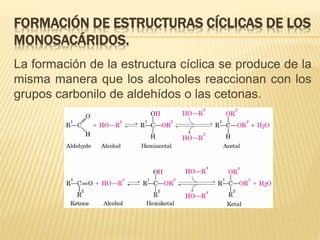
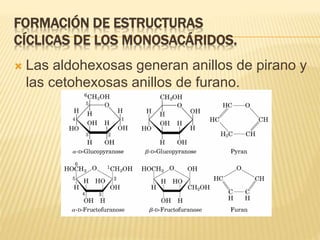
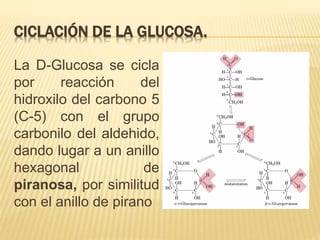
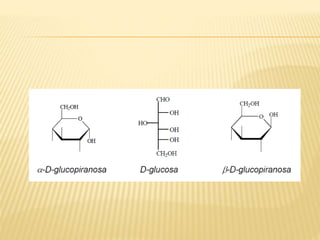
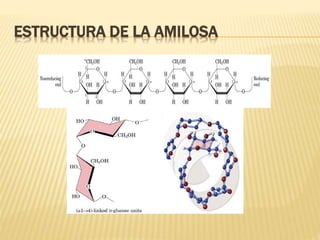
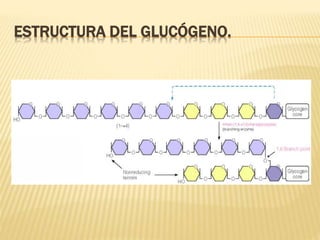
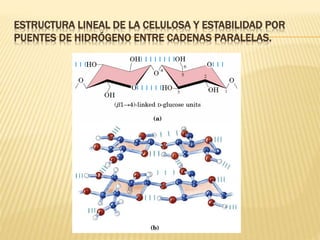
Este documento describe los carbohidratos o sacáridos, que son los compuestos orgánicos más abundantes en la naturaleza. Explica que existen monosacáridos, oligosacáridos y polisacáridos, siendo la glucosa el monosacárido más común. Los polisacáridos más importantes son el almidón, el glucógeno y la celulosa, los cuales almacenan energía o dan estructura a las células y están formados por cadenas de glucosa unidas por enlaces glucos