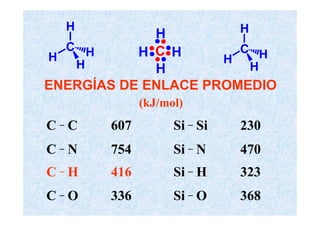
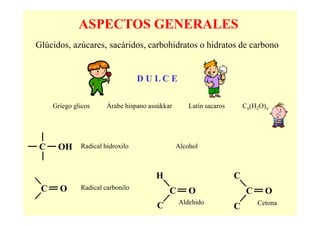
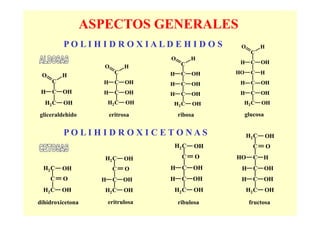
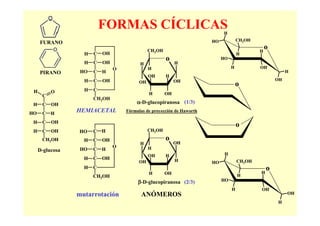
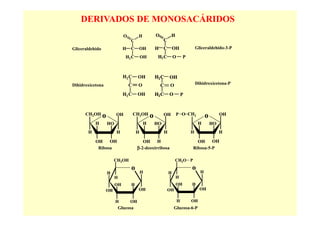
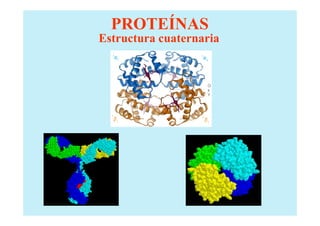
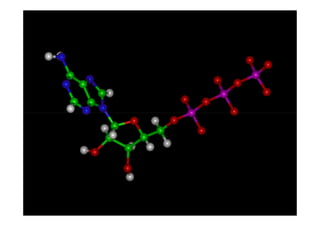
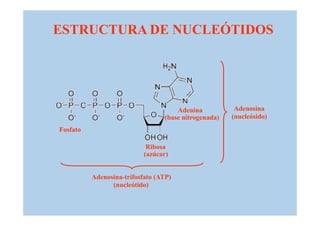
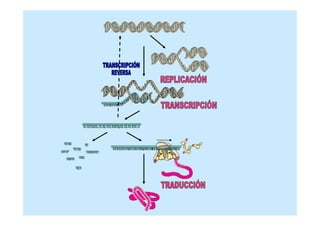
El documento proporciona información sobre los carbohidratos o glúcidos. Explica que existen monosacáridos, oligosacáridos y polisacáridos. También describe la isomería en carbohidratos, incluyendo estereoisomería, isomería óptica y formas cíclicas como la piranosa y la furanosa. Además, menciona algunos derivados de monosacáridos como fosfato-azúcares.




![Si se incuba una solución 0,1 M de glucosa-1-fosfato con una cantidad catalítica de
fosfoglucomutasa, la glucosa-1-fosfato (G-1-P) se transforma en glucosa-6-fosfato (G-6-P)
hasta que se establece el equilibrio. Las concentraciones en el equilibrio son:
glucosa-1-fosfato glucosa-6-fosfato
4,5 x 10-3 M 9,6 x 10-2 M
Calcular K’eq y ∆Gº’ para esta reacción a 25ºC.
[glucosa-6-fosfato]
K’eq = [glucosa-1-fosfato]
9,6 x 10-2 M
K’eq = 4,5 x 10-3 M
K’eq = 2,13 x 101
K’eq = 21,3
∆Gº’ = - RT ln K’eq ln = 2,3 log
∆Gº’ = - 2,3 RT log K’eq R = 8,315 J/mol . ºK
T = 298ºK
∆Gº’ = - 2,3 x 8,315 J/mol . 298ºK x log 21,3
∆Gº’ = 7579,8 J/mol = 7,6 kJ/mol](https://image.slidesharecdn.com/clasebiomolculas2010-100509174844-phpapp01/85/Clase-biomoleculas-2010-5-320.jpg)