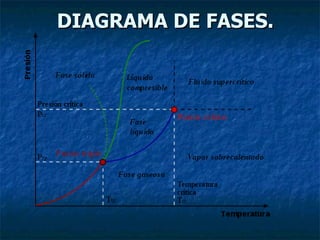
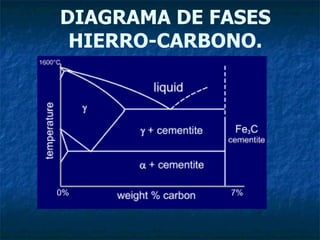
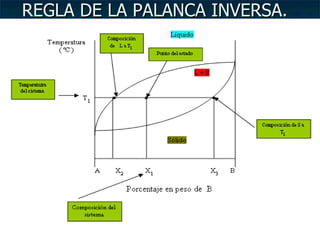
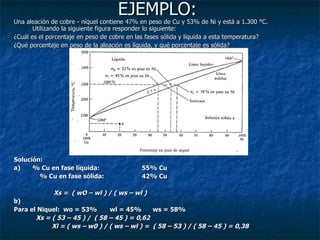
El documento describe los diferentes estados de la materia (sólido, líquido y gaseoso) y cómo cambian dependiendo de la presión y temperatura. Explica que los diagramas de fases muestran las fronteras entre los estados de la materia para un sistema dado en función de variables como la temperatura o la composición química. Además, incluye un ejemplo de cómo usar la regla de la palanca inversa para determinar la composición química y las cantidades relativas de las fases sólida y líquida en una aleación a una temperatura d