Embarazo ectópico con cicatriz de cesárea SEPTIEMBRE 2023.docx
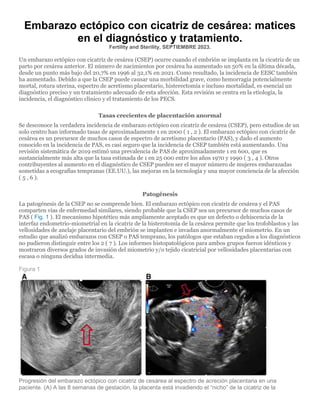
- 1. Embarazo ectópico con cicatriz de cesárea: matices en el diagnóstico y tratamiento. Fertility and Sterility, SEPTIEMBRE 2023. Un embarazo ectópico con cicatriz de cesárea (CSEP) ocurre cuando el embrión se implanta en la cicatriz de un parto por cesárea anterior. El número de nacimientos por cesárea ha aumentado un 50% en la última década, desde un punto más bajo del 20,7% en 1996 al 32,1% en 2021. Como resultado, la incidencia de EESC también ha aumentado. Debido a que la CSEP puede causar una morbilidad grave, como hemorragia potencialmente mortal, rotura uterina, espectro de acretismo placentario, histerectomía e incluso mortalidad, es esencial un diagnóstico preciso y un tratamiento adecuado de esta afección. Esta revisión se centra en la etiología, la incidencia, el diagnóstico clínico y el tratamiento de los PECS. Tasas crecientes de placentación anormal Se desconoce la verdadera incidencia de embarazo ectópico con cicatriz de cesárea (CSEP), pero estudios de un solo centro han informado tasas de aproximadamente 1 en 2000 ( 1 , 2 ). El embarazo ectópico con cicatriz de cesárea es un precursor de muchos casos de espectro de acretismo placentario (PAS), y dado el aumento conocido en la incidencia de PAS, es casi seguro que la incidencia de CSEP también está aumentando. Una revisión sistemática de 2019 estimó una prevalencia de PAS de aproximadamente 1 en 600, que es sustancialmente más alta que la tasa estimada de 1 en 25 000 entre los años 1970 y 1990 ( 3 , 4 ). Otros contribuyentes al aumento en el diagnóstico de CSEP pueden ser el mayor número de mujeres embarazadas sometidas a ecografías tempranas (EE.UU.), las mejoras en la tecnología y una mayor conciencia de la afección ( 5 , 6 ). Patogénesis La patogénesis de la CSEP no se comprende bien. El embarazo ectópico con cicatriz de cesárea y el PAS comparten vías de enfermedad similares, siendo probable que la CSEP sea un precursor de muchos casos de PAS ( Fig. 1 ). El mecanismo hipotético más ampliamente aceptado es que un defecto o dehiscencia de la interfaz endometrio-miometrial en la cicatriz de la histerotomía de la cesárea permite que los trofoblastos y las vellosidades de anclaje placentario del embrión se implanten e invadan anormalmente el miometrio. En un estudio que analizó embarazos con CSEP o PAS temprano, los patólogos que estaban cegados a los diagnósticos no pudieron distinguir entre los 2 ( 7 ). Los informes histopatológicos para ambos grupos fueron idénticos y mostraron diversos grados de invasión del miometrio y/o tejido cicatricial por vellosidades placentarias con escasa o ninguna decidua intermedia. Figura 1 Progresión del embarazo ectópico con cicatriz de cesárea al espectro de acreción placentaria en una paciente. (A) A las 8 semanas de gestación, la placenta está invadiendo el “nicho” de la cicatriz de la
- 2. cesárea. (B) A las 20 semanas de gestación, no hay una interfaz úteroplacentaria clara, con adelgazamiento del miometrio y vasos puente de la placenta que se extienden más allá de la serosa uterina. Debido a que el embrión temprano requiere un ambiente hipóxico para la implantación, puede implantarse preferentemente en una cicatriz de cesárea, que tiende a tener niveles de oxígeno más bajos que el miometrio normal. Para CSEP y PAS, las células trofoblásticas que se implantan sobre una cicatriz avascular necesitan invadir más profundamente la pared uterina para alcanzar la vasculatura materna, que es necesaria para sustentar el embarazo en desarrollo. 8 , 9 ). Diagnóstico Los embarazos ectópicos con cicatriz de cesárea se diagnostican principalmente mediante ecografía en el primer trimestre del embarazo. El uso de la ecografía transvaginal mejora en gran medida la precisión del diagnóstico y el Doppler color es un complemento útil. Las personas embarazadas con CSEP pueden presentarse de diversas formas. En una revisión de 57 pacientes con PESE, el 39% tenía sangrado vaginal indoloro, el 37% era asintomática y el 25% tenía dolor abdominal con o sin sangrado. 10 ). Para una paciente con antecedentes de cesárea que acude temprano en el embarazo para recibir atención, la mejor práctica puede ser realizar una ecografía para excluir un PECS. Alentamos a las pacientes que han tenido tres o más cesáreas o que han tenido un CSEP previo a que se presenten entre las 5 y 7 semanas de su próximo embarazo para una ecografía transvaginal inicial para evaluar la ubicación del embarazo. Un saco gestacional bajo por encima del orificio cervical interno en una paciente con antecedentes de cesárea debe hacer sospechar de EESC y esto debe desencadenar un estudio diagnóstico adecuado. El diagnóstico de un PECS se realiza mejor antes de las 8 semanas de gestación, antes de que el saco gestacional crezca hacia el fondo de ojo. Para identificar un embarazo en posición baja, se puede trazar una línea imaginaria en la mitad del útero, perpendicular al revestimiento del endometrio. Figura 2 ). Figura 2 Embarazo ectópico con cicatriz de cesárea “en el nicho”. Un embarazo bajo es inferior a la línea transversal imaginaria que corta la mitad del útero perpendicular al canal endometrial. Se han propuesto varios criterios para el diagnóstico de CSEP, siendo necesario un estudio futuro de su utilidad clínica. Timor-Tritsch et al. ( 11 ) propuso que cuando se presente cualquiera de los siguientes hallazgos, se pueda realizar un CSEP: • Visualización de una cavidad uterina vacía y un canal endocervical vacío. • Detección de placenta y/o saco gestacional incrustado en la cicatriz de histerotomía. • En las gestaciones tempranas (≤8 semanas), un saco gestacional triangular llena el nicho de la cicatriz; a las ≥8 semanas de gestación, esta forma puede volverse redondeada o incluso ovalada. • Una capa de miometrio delgada (1 a 3 mm) o ausente entre el saco gestacional y la vejiga.
- 3. • Un canal cervical cerrado y vacío. • La presencia de polo embrionario/fetal y/o saco vitelino con o sin actividad cardíaca. • La presencia de un patrón vascular prominente y a veces rico en o en el área de la cicatriz de la cesárea en presencia de una prueba de embarazo positiva. Es de destacar que Timor-Tritsch se ha opuesto a clasificar tales embarazos como ectópicos porque más de la mitad de estos embarazos progresarán hasta el tercer trimestre si se manejan con expectación. Ha escrito que prefiere el término embarazo con cicatriz de cesárea ( 12 ). El diagnóstico de un PECS puede ser difícil porque, en la ecografía, puede confundirse con un embarazo ectópico cervical, un aborto incompleto o un embarazo intrauterino (IU) bajo. En un artículo de revisión, el 13,5% (107/751) de los casos de CSEP fueron diagnosticados erróneamente ( 13 ). Un embarazo ectópico cervical, a diferencia de un PECS, se implantaría en el cuello uterino por debajo del nivel del orificio interno. Los abortos incompletos no deben tener actividad cardíaca, a diferencia de un embarazo ectópico cervical o un PESE, que pueden tener actividad cardíaca. Otros signos que respaldan un aborto incompleto son un saco gestacional irregular o aplanado y un signo positivo del saco deslizante, lo que significa que el saco gestacional se mueve con los cambios de presión sobre el transductor transvaginal. El saco gestacional de un embarazo intrauterino bajo no debe estar dentro o sobre el nicho de la cicatriz, y el Doppler no debe revelar la presencia de un patrón vascular alrededor de la cicatriz de la cesárea. La resonancia magnética puede ser un complemento útil para el diagnóstico de CSEP, pero el beneficio diagnóstico adicional que proporciona sobre la ecografía es incierto. En una serie de casos, 14 ). La resonancia magnética puede ser útil cuando el diagnóstico de un PECS en la ecografía transvaginal es incierto y podría ayudar a evitar retrasos en el diagnóstico con el uso de ecografías seriadas. El diagnóstico temprano es ideal porque es más fácil distinguir entre un CSEP y un embarazo implantado normalmente. También da tiempo para asesorar a la paciente sobre las posibles complicaciones del manejo expectante y la vigilancia prenatal requerida cuando continúa el embarazo. Cuando la paciente desea interrumpir el embarazo, la interrupción temprana se asocia con menor morbilidad y reduce el riesgo de histerectomía ( 6 , 10 , 15 ). Asesoramiento al paciente sobre la interrupción del embarazo. Los embarazos ectópicos con cicatriz de cesárea pueden provocar rotura uterina o histerectomía en el segundo trimestre, lo que somete a las pacientes a morbilidad sin un nacido vivo. Sin embargo, en muchos casos, los CSEP resultarán en última instancia en un nacimiento vivo, pero estos casos frecuentemente se complican con el PAS. Es bien sabido que el PAS puede complicarse con una morbilidad grave y el riesgo de muerte materna. En un metanálisis de EESC del primer trimestre con actividad cardíaca embrionaria, manejada expectantemente, se produjo rotura uterina durante el segundo trimestre en casi el 10% de los casos, y se requirió histerectomía en el segundo trimestre en aproximadamente el 15% de estas pacientes. 16 ). Más del 75% de los PESE con actividad cardíaca embrionaria progresaron hasta el tercer trimestre y los 40 resultaron en un nacimiento vivo, pero el 75% tuvo PAS ( 16 ). Se ha informado que el espectro de acreción placentaria de un PESE ocurre en 50%-100% de los PESE entre diferentes series de casos, lo que probablemente refleja diferentes criterios para el diagnóstico en trabajos publicados. 10 , 16171819 ). Dada la grave morbilidad y mortalidad materna asociadas con un CSEP, la Sociedad de Medicina Materno-Fetal (SMFM), con el consentimiento del Colegio Estadounidense de Obstetras y Ginecólogos, la Sociedad de Planificación Familiar y la Sociedad Estadounidense de Medicina Reproductiva, recomienda no manejo expectante de los CSEP ( 6 ). Califican esta evidencia como grado 1B, lo que significa que se trata de una recomendación sólida con evidencia de calidad moderada. Aunque la interrupción de un PESC al comienzo del embarazo se asocia con una morbilidad más baja y una menor probabilidad de histerectomía, la decisión de continuar o interrumpir el embarazo depende en última instancia de la paciente. Diagnosticar y diferenciar adecuadamente las sutilezas de los tipos de PESC con certeza puede proporcionar información adicional para un asesoramiento integral a los pacientes mientras deciden si están dispuestos a correr el riesgo de una amenaza significativa a su propia salud para potencialmente dar a luz a un bebé vivo. Existe un alto riesgo de recurrencia de CSEP, e incluso en casos que
- 4. parecen conllevar un bajo riesgo de histerectomía, este procedimiento podría ser necesario y afectar la fertilidad futura. Cuando una paciente está considerando continuar con el embarazo, se le debe asesorar sobre el alto riesgo de PAS, hemorragia potencialmente mortal y la alta probabilidad de histerectomía cuando dé a luz. Caracterizar el CSEP como “en la cicatriz” ( Fig. 3 ) versus “en el nicho” ( Fig. 2 ) puede ayudar a brindar un asesoramiento más matizado sobre los resultados del manejo expectante. Un CSEP "en la cicatriz" se implanta parcial o totalmente encima de una cicatriz de histerotomía bien curada, mientras que un CSEP "en el nicho" se implanta en la cicatriz de histerotomía. En un estudio retrospectivo, los pacientes con PESE “en el nicho” tuvieron resultados sustancialmente peores ( 19 ). En este estudio, el 94% (16/17) de los pacientes con manejo expectante de CSEP dieron como resultado un recién nacido vivo. Sin embargo, 11 pacientes con PECE “en el nicho” requirieron una histerectomía, una de ellas a las 20 semanas de gestación debido a un sangrado abundante y las otras 10 requirieron una histerectomía por cesárea en el momento del parto. En comparación, sólo 1 de 6 pacientes con un PESC “en la cicatriz” nació mediante histerectomía por cesárea debido al PAS. Las otras cinco nacieron por cesárea pero no necesitaron histerectomía. Estos datos informan al asesoramiento de pacientes con embarazos “en la cicatriz” que los riesgos de morbilidad grave aumentan, pero algunos embarazos pueden tener un resultado normal y los primeros hallazgos podrían representar un embarazo que progresará normalmente. Abrir imagen a tamaño completo figura 3 Embarazo ectópico con cicatriz de cesárea “sobre la cicatriz” a las (A) 6 semanas de gestación y (B) 9 semanas de gestación en la misma paciente. Otro estudio utilizó el "signo cruzado" para predecir la gravedad del PAS ( 20 ). Para el "signo del cruce", se dibuja una línea recta a lo largo del endometrio que conecta el orificio cervical interno y el fondo uterino en una vista sagital y se utiliza para dividir los embarazos en grupos. Aquellas con un saco gestacional CSEP dentro de la cicatriz de la cesárea y al menos dos tercios del diámetro superior-inferior del saco gestacional por encima de la línea endometrial tuvieron PAS más grave en comparación con aquellas con un saco gestacional a menos de dos tercios por encima de la línea. Figura 4 ). Todos los embarazos del primer grupo tuvieron placenta percreta o increta, en comparación con el 62% de los del segundo grupo. Este sistema de clasificación es similar a distinguir entre embarazos “en el nicho” y “en la cicatriz”, y cualquiera de ellos puede usarse para estudiar estos embarazos y así informar el asesoramiento a las pacientes.
- 5. Figura 4 Representación esquemática de la relación entre el saco gestacional ectópico, la cicatriz de cesárea (CS) y la pared uterina anterior, definida como signo de cruce (COS) (A) Embarazo normalmente implantado en el fondo uterino; (B) COS-1, saco gestacional implantado dentro del CS anterior, y al menos dos tercios del diámetro superior-inferior (SI) del saco gestacional está por encima de la línea endometrial, hacia la pared uterina anterior; (C) COS-2+, saco gestacional implantado dentro del CS anterior y menos de dos tercios del diámetro SI del saco gestacional están por encima de la línea endometrial; y (D) COS-2-, saco gestacional implantado dentro del CS anterior, y menos de dos tercios del diámetro SI del saco gestacional está por encima de la línea endometrial, pero no hay intersección entre el diámetro SI del saco ectópico y la línea endometrial. Ultrasonido en Obstetricia y Ginecología , Vol 50.1, D' Antonio F, Minneci J, Palacios-Jaraquemada J, Historia natural del embarazo con cicatriz de cesárea en ultrasonido prenatal: el signo cruzado, 5, Copyright (2017), con permiso de John Wiley and Sons ) Manejo prenatal Aunque las pacientes que eligen un manejo expectante pueden tener un nacido vivo, el aborto les permite evitar una morbilidad materna grave, incluida la hemorragia, la rotura uterina, la morbilidad de la histerectomía y la pérdida de fertilidad futura. Después de que se diagnostica un CSEP en el primer trimestre, se debe asesorar detalladamente a la paciente sobre los signos y síntomas de ruptura uterina y se le deben tomar precauciones sobre cuándo presentarse inmediatamente a la sala de emergencias. Se debe asesorar a la paciente sobre los altos riesgos del PAS y los signos de trabajo de parto prematuro. La SMFM recomienda repetir la cesárea entre las semanas 34 0/7 y 35 6/7 de gestación, dada la alta probabilidad de PAS ( 6 ). Sin embargo, en nuestra opinión, dado que el 25% de los PESC que progresan al tercer trimestre no tienen PAS, el parto puede retrasarse entre 36 0/7 y 37 6/7 semanas cuando solo hay una previa, o más tarde cuando no hay placenta. previa está presente. Opciones de tratamiento Hay varias opciones para finalizar un CSEP ( 1 , 10 , 13 , 15 , 21 ). Las opciones quirúrgicas incluyen histeroscopia, laparoscopia, laparotomía, cirugía transvaginal, legrado con punzocortante y aspiración uterina. Otras intervenciones de procedimiento incluyen embolización de la arteria uterina (EAU), inyección de metotrexato (MTX) en el saco intragestacional, inyección directa de cloruro de potasio, descompresión del saco guiada por aguja, catéteres con balón y ecografía enfocada de alta intensidad guiada por ecografía. El MTX
- 6. sistémico se utiliza a menudo junto con estos métodos. Dada la falta de ensayos controlados aleatorios que comparen las diferentes opciones de tratamiento, no existe una estrategia de manejo recomendada ( 6 ). A menudo, la elección del tratamiento depende de las habilidades especializadas disponibles en una institución, que pueden incluir cirugía ginecológica mínimamente invasiva, un especialista en medicina materno-fetal o un radiólogo intervencionista capaz de realizar procedimientos guiados por imágenes. Revisaremos las diferentes modalidades de tratamiento a continuación. La conducta expectante El único escenario en el que sería razonable un manejo expectante para el tratamiento de un PECS es cuando no hay actividad cardíaca embrionaria en las primeras etapas del embarazo. Inicialmente, se debe realizar una observación estrecha con U seriadas para confirmar el diagnóstico de fracaso temprano del embarazo ( 16 ). El tratamiento expectante incluye β-gonadotropina humana (β-hCG) en serie y ecografía transvaginal. En algunos casos, es posible que el CSEP no resuelva sin intervención. En estos casos, es poco probable que el legrado por succión bajo orientación estadounidense produzca hemorragia. El MTX sistémico se puede utilizar como terapia complementaria en tales casos y tiene el potencial de reducir la pérdida de sangre durante el procedimiento cuando los niveles de β-hCG están elevados de manera persistente. Para obtener más detalles sobre el uso de MTX en el tratamiento CSEP, consulte la información que se proporciona a continuación. Hay riesgos con el manejo expectante. Una revisión sistemática encontró que el 70% de 17 casos sin actividad cardíaca embrionaria no experimentaron complicaciones maternas importantes y tuvieron un aborto espontáneo sin complicaciones ( 16 ). Sin embargo, los cinco casos restantes sí requirieron tratamiento médico o quirúrgico por hemorragia grave y otros síntomas. Hubo un caso de rotura uterina en el primer trimestre, pero esto no resultó en la necesidad de una histerectomía ni causó muerte materna. Se debe advertir a las pacientes que la EESC puede llevar meses porque la placenta se implanta principalmente dentro del tejido fibroso y la absorción del saco gestacional es lenta. El manejo expectante también puede estar asociado con la formación de malformaciones arteriovenosas que causan sangrado vaginal abundante y persistente, que puede requerir EAU. En una serie de casos, 2 de 10 PESE manejados expectantemente desarrollaron una malformación arteriovenosa entre las 7 y 8 semanas de gestación, que finalmente requirió EAU. 22 ). Manejo de metotrexato Para el tratamiento médico de un PECS, la inyección intragestacional de MTX con o sin MTX sistémico tiene altas tasas de éxito con bajas tasas de complicaciones. En una serie de casos, el 74% de 96 PECS fueron tratados con éxito con una inyección de MTX en el saco intragestacional, cifra que aumentó al 88,5% después de una inyección local o intramuscular adicional. 23 ). Los niveles séricos de β-HCG >100.000 UI/L en el momento de la inyección aumentaron el riesgo de fracaso del tratamiento. 23 ). La dosis de inyección intragestacional de MTX en el saco intragestacional típicamente utilizada es de 1 mg/kg de peso materno, con una dosis máxima de 50 mg en 1 ml de solución. 11 , 21 , 23 ). Además, se puede emplear cloruro de potasio intracardíaco para provocar el cese de la actividad cardíaca embrionaria, especialmente en el contexto de un embarazo heterotópico, con una dosis típica de 2 a 4 ml de una solución de 2 mEq/ml. 24 , 25 ). Las inyecciones en el saco intragestacional se pueden realizar por vía transvaginal o transabdominal. El tipo, calibre y longitud de la aguja a menudo se eligen a discreción del proveedor. Se puede realizar una aspiración del saco para confirmar la correcta colocación de la aguja. La asistolia cardíaca del producto de la gestación debe documentarse después del procedimiento y puede confirmarse en un intervalo de 60 minutos después del procedimiento para estar seguro de que el procedimiento tuvo el efecto deseado. Durante el tratamiento médico, se debe aconsejar al paciente que espere un seguimiento prolongado. En una revisión de pacientes que recibieron MTX en saco intragestacional y una dosis de MTX sistémico, la resolución del embarazo tardó 88,6 días (rango: 26 a 177 días) ( 11 ). En general, no se recomienda el tratamiento con MTX sistémico solo, dada su menor eficacia que otras modalidades de tratamiento cuando hay actividad cardíaca embrionaria. En una población no seleccionada, incluidos casos con actividad cardíaca, el MTX sistemático solo tuvo una tasa de complicaciones del 13% al 62% con una eficacia de sólo el 8,7% al 75%. 6 , 13 , 21 , 26 ). En nuestra institución, sólo consideraríamos el tratamiento con MTX sistémico solo para un PESE sin actividad cardíaca y un nivel de β-hCG <5000 mUI/mL, similar a las recomendaciones utilizadas para el tratamiento de las PE tubáricas, dada la alta tasa de fracaso
- 7. cuando el tratamiento cardíaco la actividad está presente. Administrar metotrexato sistémico a una paciente con un PESE sin actividad cardíaca que desea interrumpir este embarazo de alto riesgo tiene el potencial de reducir las complicaciones en comparación con la tasa de complicaciones superior al 30% asociada con el manejo expectante. 17 ). En nuestra práctica clínica administraríamos una segunda dosis de MTX cuando el paciente esté estable y cuando no haya una disminución adecuada de β-hCG >15% entre los días 4 y 7 después de la primera dosis, similar al tratamiento de la tubárica. EP. Cuando hay una respuesta inicial al tratamiento, seguiríamos el nivel de β-hCG semanalmente hasta que llegue a cero. También realizaríamos un seguimiento semanal de los CSEP tratados con MTX sistémico con ecografía para garantizar que la vascularización en el sitio de implantación del CSEP esté disminuyendo. Cuando hay evidencia de un aumento de la vascularización o cuando el paciente tiene un sangrado significativo, a menudo se procede también con la aspiración por vacío. Tratamiento quirúrgico La elección del tratamiento quirúrgico depende, en parte, de las habilidades del equipo directivo. Entre las opciones de tratamiento quirúrgico, la laparoscopia, la histeroscopia, la laparotomía y la aspiración por succión tienen buenos perfiles de seguridad. El legrado cortante tiene el potencial de exponer vasos sanguíneos profundamente invasivos, lo que provoca un sangrado abundante y, por lo tanto, debe evitarse. Sin embargo, en múltiples estudios se ha demostrado que la aspiración por vacío es eficaz y presenta bajas tasas de complicaciones. En un estudio que evaluó la aspiración por vacío en 191 pacientes <14 semanas de gestación, el 4,7% requirió una transfusión de sangre, el 6% necesitó repetir el procedimiento y hubo un solo caso de histerectomía por hemorragia ( 27 ). En esta revisión, el diámetro del saco gestacional fue un predictor de pérdida de sangre. En otra serie de casos reciente de 14 PESE con <50 días de gestación tratados con aspiración por succión, todos ocurrieron sin complicaciones con una pérdida de sangre estimada <10 ml ( 28 ). Para embarazos que duraron más de 50 días, 5 de los 7 tratados con aspiración endouterina no tuvieron complicaciones. Una complicación se debió a peroración uterina y la otra a hemorragia, que requirió un balón intrauterino. Estas series de casos apoyan la idea de que la aspiración por sí sola es segura para el tratamiento CSEP, especialmente para embarazos tempranos en el primer trimestre. Hay un informe escrito que sugiere la colocación profiláctica del doble balón de Cook después de la aspiración por vacío para prevenir el sangrado, y esto puede considerarse una maniobra profiláctica. 29 ). Una ventaja potencial de la escisión laparoscópica o transvaginal del CSEP es la resección y reparación de la cicatriz anormal. La escisión laparoscópica tuvo una tasa de éxito del 97,1% sin complicaciones en una revisión sistemática que incluyó 69 casos ( 21 ). En 118 casos de escisión transvaginal, hubo >99% de eficacia y una tasa de complicaciones del 0,9% ( 21 ). La escisión histeroscópica de un CSEP tiene una eficacia del 83% y una tasa de complicaciones del 3,2% en 95 casos ( 21 ). La laparotomía tuvo una tasa de complicaciones del 5,3% ( 13 ). Estas opciones son más invasivas que las descritas anteriormente y pueden ser más adecuadas para gestaciones más avanzadas. La histerectomía grávida para pacientes con un PECS en el segundo trimestre debe reservarse para aquellas que no desean fertilidad futura y desean un aborto ( Fig. 5 ). ). Al asesorar a la paciente sobre los riesgos maternos de una histerectomía en el segundo trimestre en comparación con una histerectomía por cesárea, se debe advertir a la paciente que una histerectomía en el segundo trimestre tiene menos pérdida de sangre en comparación con una histerectomía por cesárea en la mayoría de los casos, pero que no hay riesgo de pérdida de sangre en comparación con una histerectomía por cesárea. -Estudios principales que comparan la morbilidad y mortalidad de estos 2 procedimientos. Además, dependiendo del grado de invasión del PAS, una histerectomía temprana en el segundo trimestre puede prevenir una mayor invasión o crecimiento de la placenta hacia la vejiga u otros órganos circundantes. Existen estudios de casos limitados sobre el tratamiento de la PECS diagnosticada en el segundo trimestre. El tratamiento abarca desde histerectomía abierta, histerectomía laparoscópica, 30 ).
- 8. Abrir imagen a tamaño completo Figura 5 El útero se divide sagitalmente, mostrando un embarazo ectópico con cicatriz de cesárea a las 9 semanas de gestación con saco gestacional y placenta. (Reimpreso de American Journal of Obstetrics and Gynecology , Vol 228.5, Glassman D, Mohamed N, Sauer M, Treatment of cesarean scar ectopic breast by gravid total abdominal histerectomia, 595–596, Copyright (2023), con autorización de Elsevier). Tratamientos complementarios Los catéteres intrauterinos con balón se han utilizado con éxito para el tratamiento CSEP y, a menudo, como complemento del MTX sistémico o la aspiración por vacío, pero no se han estudiado tan exhaustivamente como otros tratamientos quirúrgicos. 29 , 31 , 32 ). Los informes publicados han evaluado el balón de Cook doble, con el globo superior lleno con 10 a 25 ml de solución salina en el fondo de ojo y el globo inferior lleno con 10 a 20 ml de líquido al nivel del CSEP, lo que produce la compresión del saco gestacional. ( Figura 6 ) ( 32 ). El catéter se coloca bajo guía ecográfica y se ajusta según sea necesario. Una vez inflados los globos, la ecografía confirma el cese de la actividad cardíaca embrionaria y, con mayor frecuencia, el colapso del saco gestacional. En un informe publicado, el balón se dejó colocado durante 1 a 3 días, dependiendo de una ecografía de seguimiento de 24 horas y de la preferencia del proveedor. En esta serie, se administraron antibióticos aunque el balón estaba colocado. Figura 6
- 9. Un balón de Cook doble con el globo superior lleno con 10 a 25 ml de solución salina en el fondo de ojo y el globo inferior lleno con 10 a 20 ml de líquido al nivel de la cicatriz de la cesárea del embarazo ectópico, lo que produce la compresión del saco gestacional. Cuando se retiró el catéter, primero se desinfló el globo inferior mediante ecografía transvaginal para evaluar la actividad cardíaca embrionaria o el sangrado vaginal. En un estudio de pacientes que recibieron tratamiento con MTX sistémico y balón UI, 37 pacientes fueron manejadas exitosamente sin complicaciones, y una paciente requirió una histerectomía 27 días después del procedimiento debido a un sangrado abundante. 31 ). La embolización de la arteria uterina se ha utilizado como terapia complementaria con dilatación y legrado (D y C), histeroscopia y MTX sistémico. Un estudio encontró que los EAU antes del legrado por succión reducen la pérdida de sangre estimada ( 33 ). En una revisión, se encontró que la EAU con MTX sistémico tenía una tasa de éxito de sólo el 68,2%, pero cuando se utilizó la EAU con legrado, histeroscopia o ambos, hubo una tasa de éxito del 93,6% con solo el 3,4% de complicaciones. 21 ). El uso de partículas de esponja de gelatina absorbibles puede reducir el riesgo de infertilidad futura y malos resultados del embarazo. En un estudio que analizó los CSEP tratados con EAU combinados con D y C, 7 de los 16 CSEP tratados que deseaban fertilidad tuvieron un nacimiento vivo posterior ( 34 ). Las técnicas de investigación no quirúrgicas más nuevas incluyen la ecografía enfocada de alta intensidad guiada por ultrasonido y la inyección de lauromacrogol. La ecografía enfocada de alta intensidad, que se ha utilizado para tratar los fibromas sintomáticos, se utilizó para tratar con éxito 16 CSEP ( 35 ). La ecografía enfocada de alta intensidad, cuando se utilizó como complemento de D y C, tuvo resultados de hemorragia y eficacia similares a los de la EAU con D y C ( 36 ). De manera similar, el legrado combinado con una inyección de lauromacrogol guiada por ecografía, un agente esclerosante, produjo resultados clínicos comparables a los del legrado después de la EAU. Al momento de escribir este artículo, estas técnicas probablemente se utilicen mejor bajo un protocolo de estudio de investigación. Elegir la mejor opción de tratamiento Hasta que se puedan realizar más investigaciones que comparen estas diferentes intervenciones, es mejor individualizar el tratamiento elegido para la CSEP. Actualmente, la literatura no ha identificado la mejor opción de tratamiento. Las dos revisiones sistemáticas más grandes que compararon las diferentes opciones de tratamiento llegaron a conclusiones inconsistentes sobre qué opción de tratamiento equilibraba mejor la eficacia con las complicaciones del procedimiento. En Timor-Tritsch y Monteagudo ( 13 ) de 2012, que incluyó 751 casos de PECS, recomendaron la extirpación histeroscópica y la inyección intragestacional local de MTX o cloruro de potasio dado que estas modalidades tuvieron las tasas de complicaciones más bajas (18,4% y 9,6%, respectivamente). Las modalidades con mayor tasa de complicaciones fueron MTX sistemático (62,1%), legrado (61,9%) y EAU (46,9%), por lo que fueron desaconsejadas. Por el contrario, en Birch Petersen et al. En una revisión sistemática, que analizó 2.037 CSEP, se encontró que los enfoques intervencionistas eran superiores a los enfoques médicos ( 21 ). Entre estas terapias, las tasas de éxito más altas con bajas complicaciones incluyen la resección CSEP transvaginal, la laparoscopia, la EAU con legrado, la histeroscopia o ambas, y la EAU sola. Un estudio reciente ha desarrollado un sistema de clasificación que analiza los marcadores ecográficos del CSEP para determinar la mejor opción de tratamiento ( 15 ). Este estudio examinó 995 CSEP y desarrolló clasificaciones basadas en el grosor del miometrio sobre la cicatriz y el diámetro del saco gestacional. Los expertos clínicos recomendaron la opción quirúrgica óptima para cada tipo. Este sistema de clasificación se validó internamente y, cuando se aplicó a un subconjunto separado con PESE, la tasa de éxito general del tratamiento de primera línea recomendado con el nuevo grupo de clasificación fue del 97,5 % y ninguna paciente requirió histerectomía. Los investigadores del estudio recomiendan que los PECS con un espesor miometrial anterior >3 mm puedan someterse a un legrado por succión bajo guía ecográfica con o sin histeroscopia. Cuando el miometrio anterior está entre 1 y 3 mm y el diámetro promedio del saco gestacional es <30 mm, recomiendan legrado por succión con histeroscopia bajo guía ecográfica. Cuando el miometrio anterior mide entre 1 y 3 mm y el diámetro promedio del saco es >30 mm, se sugiere histeroscopia con monitorización laparoscópica, escisión o posiblemente escisión transvaginal. Cuando el miometrio anterior es <1 mm y el diámetro promedio del saco gestacional es <50 mm, se recomienda la escisión laparoscópica o transvaginal. Para los sacos que miden >50 mm o cuando existe la preocupación de una fístula arteriovenosa uterina, recomiendan la escisión laparoscópica después de una EAU o una laparotomía. Se recomienda la
- 10. escisión laparoscópica o la escisión transvaginal. Para los sacos que miden >50 mm o cuando existe la preocupación de una fístula arteriovenosa uterina, recomiendan la escisión laparoscópica después de una EAU o una laparotomía. Se recomienda la escisión laparoscópica o la escisión transvaginal. Para los sacos que miden >50 mm o cuando existe la preocupación de una fístula arteriovenosa uterina, recomiendan la escisión laparoscópica después de una EAU o una laparotomía. En nuestra opinión, cuando el CSEP en la ecografía tiene varios factores que lo colocan en alto riesgo de hemorragia cuando se extrae, como el tamaño del saco gestacional, la edad gestacional, el grosor del miometrio que recubre el embarazo o la vascularidad, la resección quirúrgica sería ideal para una evaluación más directa. control del sangrado y su alta eficacia. Sin embargo, cuando esta experiencia quirúrgica no está disponible o el CSEP es temprano en la gestación y se observa vascularidad mínima, la inyección intragestacional de MTX en el saco gestacional, la aspiración por succión o la resección histeroscópica son modalidades con alta eficacia y tasas de complicaciones relativamente bajas. Cuando el saco gestacional CSEP es >50 mm y el miometrio es delgado, se debe considerar el tratamiento complementario, como taponamiento con balón, MTX sistémico o EAU. El balón de doble UI utilizado junto con MTX sistémico es relativamente novedoso, y no hay tanta experiencia publicada en comparación con otras intervenciones, pero este parece ser un enfoque razonable. La embolización de la arteria uterina se ha utilizado para reducir los riesgos de hemorragia y puede reducir el riesgo de histerectomía. Terminación de un csep en estados con prohibición del aborto Después del fallo en Dobbs vs. Jackson en junio de 2022, está surgiendo una preocupación sobre la interpretación de la legislación restrictiva sobre el aborto en lo que respecta al tratamiento de la EP y otros embarazos localizados anormalmente, incluidos los CSEP. Muchas restricciones al aborto solo incluyen excepciones para “emergencias que ponen en peligro la vida” y no incluyen lenguaje explícito que permita el tratamiento de la PE. Cuando se combina con la posibilidad de nacimientos vivos y la dificultad de diagnosticar y diferenciar los PESC de los embarazos intrauterinos, los médicos pueden dudar en tratar los PESC por temor a que se los interprete como un aborto ilegal que conduzca a cargos penales dentro de su estado. Por ejemplo, un caso de una paciente con un CSEP en un estado con una prohibición total del aborto no pudo acceder a la atención del aborto debido a las preocupaciones del médico sobre la criminalización. 37 , 38 ). Adoptar un lenguaje que se refiera a los embarazos con cicatriz de cesárea como PE y las recomendaciones de la SMFM contra el manejo expectante de los PESC pueden ser herramientas críticas para permitir que los proveedores de abortos en todo Estados Unidos intervengan y traten los PECS en la era post-Dobbs. Por lo tanto, cualquier debate sobre la posibilidad de un manejo expectante de ciertos tipos de PESC debe tener en cuenta las posibles consecuencias negativas para el acceso a la atención del aborto en estados con leyes restrictivas. Embarazos futuros Se debe advertir a la paciente que, en futuros embarazos, debe realizarse una ecografía temprana en el primer trimestre que evalúe la posibilidad de un CSEP. Los pacientes con un CSEP tienen un mayor riesgo de recurrencia. Pequeñas series de casos informaron tasas de recurrencia entre el 5% y el 40% ( 2 , 39404142 ). El estudio más grande de un solo centro para describir el embarazo después de la PESC incluyó 32 embarazos y reportó una tasa de PEPE recurrente del 15,6% ( 42 ). Existen informes de casos y series de reparaciones de nichos de cicatrices de cesárea, pero aún no hay datos que indiquen que la resección y reparación laparoscópica o transvaginal de la cicatriz de cesárea reduzcan el riesgo de recurrencia ( 15 , 43444546 ). Diferentes expertos han recomendado esperar entre 6 y 18 meses antes de intentar otro embarazo después del manejo conservador del útero de un CSEP, pero no hay datos que respalden esta recomendación. 2 , 6 , 18 , 47 ). Un estudio que analizó el intervalo entre el CSEP actual y la cesárea anterior encontró que este oscilaba entre 6 meses y 12 años ( 2 ). Para futuros embarazos concebidos mediante fertilización in vitro (FIV), los datos son limitados sobre si los embarazos de FIV están asociados con un mayor riesgo de PECS. Lo que se sabe es que los embarazos por FIV se asocian con un mayor riesgo de PAS en comparación con las concepciones naturales, independientemente de los antecedentes de parto por cesárea. 48 ). Un centro de FIV informó 12 CSEP de 20,256 embarazos de FIV
- 11. para una incidencia de 1:1,168, que es mayor que la incidencia reportada que incluyó embarazos de FIV y no FIV ( 49 ). En otro estudio que examinó 98 embarazos de FIV con antecedentes de cesárea previa, hubo 2 PESE ( 50 ). Reducir la incidencia de CSEP Aunque diferentes técnicas quirúrgicas pueden mostrar diferencias en la apariencia de la cicatriz de histerotomía en la ecografía posparto, como la formación de un nicho, aún está por verse si estas técnicas quirúrgicas realmente conducen o no a una disminución de las tasas de CSEP o PAS. Dos estudios encontraron que la sutura extradecidual disminuyó el tamaño del nicho en las imágenes posparto ( 51 , 52 ). Una revisión sistemática, que incluyó 20 ensayos controlados aleatorios, encontró que el cierre de una sola capa en comparación con el cierre de dos capas de la histerotomía dio como resultado un espesor miometrial residual significativamente más delgado, lo que potencialmente aumenta la prevalencia de defectos en las cicatrices uterinas. 53 ). También puede haber una asociación entre cesáreas previas de nalgas y CSEP ( 17 ). El segmento uterino inferior no desarrollado puede provocar una cicatriz de histerotomía más gruesa que no cicatriza adecuadamente, provocando dehiscencias microscópicas en la cicatriz donde se implantaría el blastocisto. Durante las cesáreas repetidas, la histerotomía puede ser incluso más alta para evitar lesiones en la vejiga, lo que genera una cicatriz de histerotomía que es más accesible para el embrión que se implanta porque no se encuentra en la porción inaccesible del cuello uterino. Esto puede explicar el mayor riesgo de PAS con el creciente número de cesáreas. Otro factor que puede influir en la incidencia de CSEP y PAS después del parto por cesárea es que la ubicación cervical de la histerotomía, que puede incorporar glándulas productoras de moco, podría dificultar la curación de la histerotomía. 54 ). Aunque los datos sobre si la técnica quirúrgica de la cesárea puede aumentar el riesgo de un PECS o PAS son limitados, aplicar una buena técnica quirúrgica para el cierre de la histerotomía, como evitar el endometrio al suturar la histerotomía y elegir la ubicación más óptima, plantea poco riesgo para el paciente. paciente y ofrece un beneficio potencial al paciente. En última instancia, la mejor manera de prevenir un PECS es prevenir la cesárea primaria. Por lo tanto, se deben realizar esfuerzos continuos para estandarizar las indicaciones de las cesáreas para reducir la incidencia general de partos por cesárea. Por ejemplo, en California, la tasa de parto por cesárea para nulíparas de vértice único a término disminuyó del 26,0 % en 2014 al 22,8 % en 2019 con la implementación de kits de herramientas para proveedores y paquetes de seguridad del paciente a través de California Maternal Quality Care Collaborative ( 55 ). Se ha demostrado que fomentar intervenciones sistémicas que promueven las directrices sobre las indicaciones de cesárea, como las descritas en la declaración de consenso del Colegio Estadounidense de Obstetras y Ginecólogos, "Prevención primaria de la cesárea", disminuye las tasas de cesárea ( 56 ). Conclusión Con las crecientes tasas de cesáreas en todo el mundo, hay una mayor incidencia de PESC. La literatura sobre el pronóstico y tratamiento de la EP de cicatriz de cesárea ha aumentado significativamente en las últimas dos décadas. La ecografía transvaginal temprana del primer trimestre para una paciente con antecedentes de cesárea es el enfoque óptimo para diagnosticar y predecir el pronóstico de un PECS. Queda por determinar el manejo óptimo de un CSEP después del diagnóstico. Se ha establecido un Registro Internacional de CSEP para comprender mejor los criterios de diagnóstico, el tratamiento y el resultado ( 57 ). El tratamiento oportuno antes de que el CSEP crezca e invada más profundamente el miometrio disminuye los riesgos de complicaciones como rotura uterina, hemorragia potencialmente mortal y progresión a PAS. Las recientes prohibiciones estatales sobre el aborto con un lenguaje vago sobre las excepciones médicas, cuando la vida de la mujer embarazada está en peligro, representan una barrera para el tratamiento oportuno de la PESC.