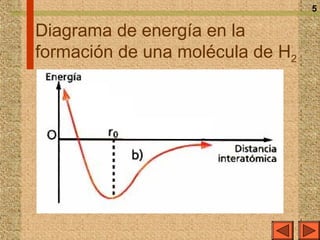
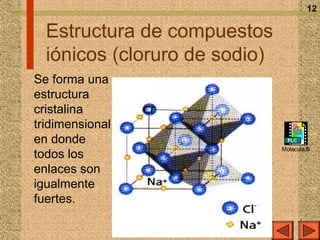
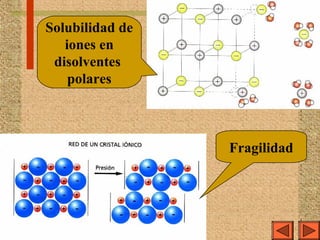
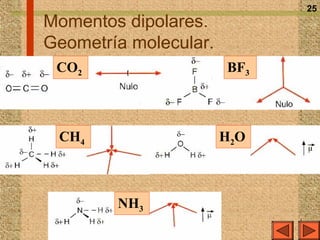
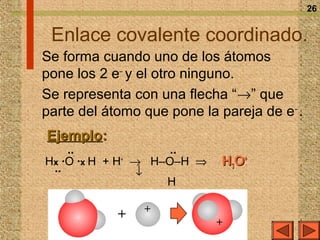
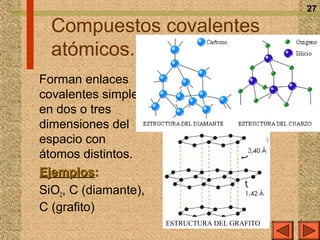
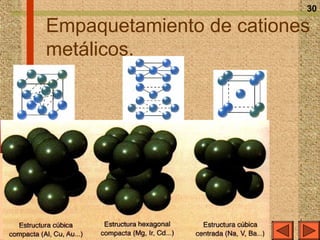
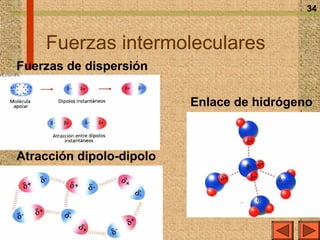
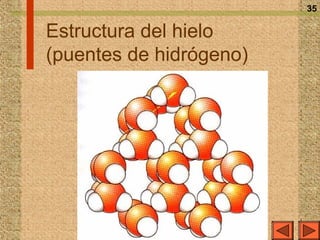
El documento explica los diferentes tipos de enlaces químicos, incluyendo el enlace iónico, covalente y metálico, así como sus propiedades, formación y estructura. Se discuten conceptos como la electronegatividad, el momento dipolar y las fuerzas intermoleculares, además de la regla del octeto y la representación de Lewis. También se presentan ejemplos de reacciones de ionización y se analizan las características de los compuestos iónicos y covalentes.