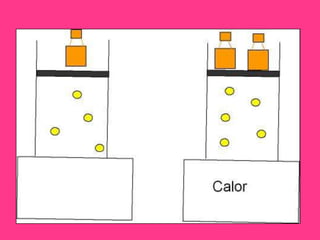
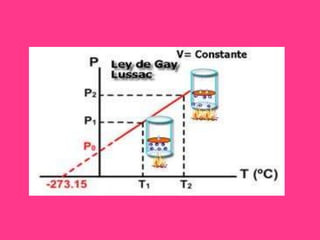
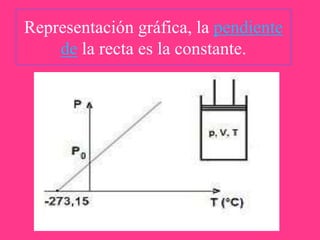
La ley de Gay-Lussac establece que para una cierta cantidad de gas, el cociente entre la presión y la temperatura absoluta tiene un valor constante. Específicamente, si la temperatura de un gas aumenta manteniendo el volumen constante, la presión también aumenta de forma proporcional. Además, la ley se expresa mediante una ecuación en la que el cociente entre la presión final y la temperatura final es igual al cociente entre la presión inicial y la temperatura inicial.