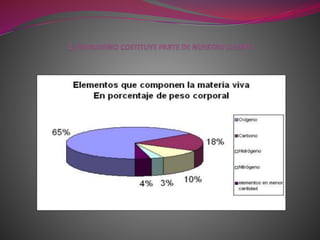
El documento habla sobre el nitrógeno. Explica que el nitrógeno es un elemento químico gaseoso e incoloro que forma parte del aire y es esencial para la vida. Detalla que el nitrógeno se encuentra en las proteínas y ácidos nucleicos de los seres vivos y participa en procesos como la digestión y el crecimiento. También analiza usos del nitrógeno en la industria farmacéutica como la desinfección y conservación.



![CARACTERÍSTICAS GENERALES
Nombre: Nitrógeno Símbolo: N
Número atómico: 7 Masa atómica (uma): 14,0067
Período: 2 Grupo: VA (nitrogenoideos)
Bloque: p (representativo) Valencias: +1, +2, +3, -3, +4, +5
PROPIEDADES PERIÓDICAS
Configuración electrónica: [He] 2s2 2p3 Radio atómico (Å): 0,92
Radio iónico (Å): 1,71 (-3) Radio covalente (Å): 0,92
Energía de ionización (kJ/mol): 1400 Electronegatividad: 3,04
Afinidad electrónica (kJ/mol): 7
PROPIEDADES FÍSICAS
Densidad (g/cm3): 0,0012506 (0 ºC) Color: Incoloro
Punto de fusión (ºC): -210 P. de ebullición (ºC): -196
Volumen atómico (cm3/mol): 13,54](https://image.slidesharecdn.com/monografia-140602220824-phpapp01/85/Monografia-del-nitrogeno-4-320.jpg)