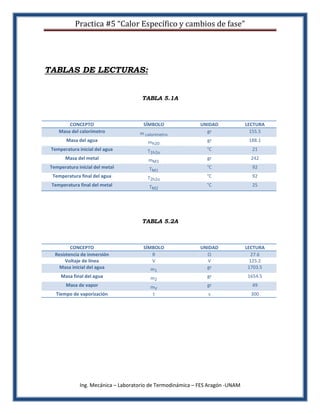
Este documento presenta los objetivos, materiales, aspectos teóricos y desarrollo de una práctica de laboratorio sobre calor específico y cambios de fase. La práctica consiste en tres actividades: 1) determinar el calor específico de un metal, 2) calcular el equivalente mecánico del calor utilizado, y 3) calcular la entalpía de vaporización. Se proporcionan tablas para registrar las lecturas y cálculos realizados durante cada actividad.