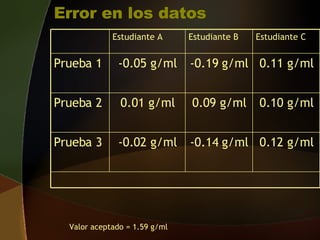
Este documento habla sobre la precisión y exactitud en la medición. Define precisión como la cercanía de una serie de medidas entre sí, dependiendo del observador. Define exactitud como la cercanía de una medida con el valor real, dependiendo del instrumento de medida. Explica cómo calcular el error en una medida y el porcentaje de error para estandarizarlo. Finalmente, recomienda ejercicios de práctica en un libro de texto y en el laboratorio.