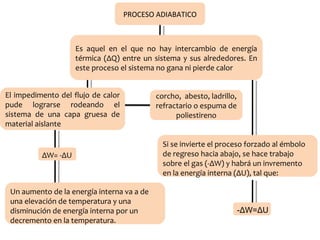
Un proceso adiabático es aquel en el que no hay intercambio de energía térmica entre un sistema y su entorno. Durante un proceso adiabático, el sistema no gana ni pierde calor y todo el trabajo realizado sobre el sistema se traduce en un cambio en su energía interna. Un ejemplo es la expansión adiabática de un gas contenido en un cilindro aislado térmicamente.