Soluciones_1.pptx
- 1. UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
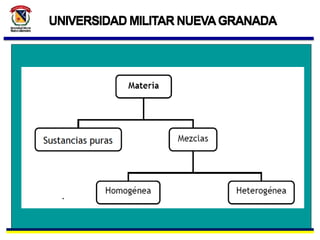
- 2. ¿Qué es una disolución o solución química? Mezcla homogénea, constituida por dos o más componentes. UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 3. COMPONENTES DE UNA SOLUCIÓN SOLUTO: •Se encuentra en menor cantidad. •Se disuelve. •Puede haber uno o varios solutos en una solución. SOLVENTE O DISOLVENTE: •Se encuentra en mayor cantidad. •Disuelve los solutos y determina el estado de la solución. •Solo hay un solvente. UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 4. Solución Solvente Soluto(s) Gaseosa (l) H2O Azúcar, CO2 Aire (g) N2 O2, CH4 Sal de cocina (s) NaCl I, F UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 5. EL AGUA COMO DISOLVENTE El agua es el disolvente universal, es decir, el líquido que más sustancias disuelve y ello hace que sea una de las sustancias más importantes en el ámbito de las disoluciones. Soluto polar: Si se disuelve en agua. Soluto no polar: No se disuelve el agua, pero sí en disolventes no polares. UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 6. Clasificación de soluciones DISOLUCIONES ESTADO Disoluciones sólidas Disoluciones liquidas Disoluciones gaseosas CONCENTRACION Disoluciones diluidas (insaturadas) Disoluciones concentradas (saturadas) Disoluciones supersaturadas UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 7. • Soluciones sólidas: aleaciones de los metales Ejemplos: Bronce (Cu-Sn) Acero (Fe-Cu) Latón (Cu-Zn) Amalgama (Hg – METAL) I) Clasificación de soluciones según su estado: UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 8. • Soluciones líquidas Sólido en liquido Liquido en liquido Gas en liquido Azúcar en agua Sal en agua Alcohol en agua CO2 en agua (Bebidas gaseosas) • Soluciones gaseosas Aire UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 9. Diluidas o insaturadas: Son las que tienen una pequeña cantidad de soluto en un determinado volumen de disolución. Por debajo del máximo de saturación. Concentradas o saturadas: Son aquellas que tienen una cantidad de soluto, próximo a la saturación, en un determinado volumen de disolución. Existe un equilibrio dinámico entre soluto y disolvente. Supersaturadas: Son las que contienen más soluto del que puede disolver el disolvente. Por encima del máximo de saturación. II) Clasificación de soluciones según su concentración: UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 10. Insaturada Saturada Supersaturada UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 11. Departamento de Química, Facultad de Ciencias Básicas y Aplicadas, UMNG Factores que afectan la solubilidad: La temperatura: En la mayoría de los casos la solubilidad de una sustancia sólida aumenta con la temperatura; en los gases la solubilidad disminuye al aumentar la temperatura. La presión: Para fines prácticos, la presión externa no tiene influencias sobre la solubilidad de líquidos y sólidos pero si influye sobre la solubilidad de los gases. Ley de Henry: la solubilidad de un gas en un líquido es proporcional a la presión del gas sobre la disolución. La adición de un ion común (efecto del ion común): Es el efecto que produce agregar determinada concentración de un ion que es común con uno de los iones de la sal cuando ambos se encuentran en la misma solución, dando como resultado la disminución de la solubilidad. UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 12. Departamento de Química, Facultad de Ciencias Básicas y Aplicadas, UMNG UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 13. CONCENTRACIÓN DE LAS SOLUCIONES UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 14. Unidades de Concentración 1) Unidades físicas o porcentuales % m/m = masa del soluto x 100 masa de solución Porcentaje en masa Porcentaje masa/masa ( ó porcentaje peso/peso) Porcentaje volumen a volumen % volumen/volumen ( % v/v ) % v/v = volumen del soluto x 100 volumen solución Porcentaje masa / volumen ó porcentaje peso/volumen ( % m/v ) ó ( % p/v ) % m/v = masa de soluto x 100 volumen de solución UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 15. Partes por millón ppm Es la masa (mg) de soluto que se encuentra en 1 L o 1 kg de solución. ppm = masa del soluto volumen o masa de solución UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 16. 2) Unidades químicas M = moles del soluto litro de solución Molaridad Moles (n) de soluto que esta contenida en ciertas unidades de solución (L). UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA
- 17. Ejercicios: ¿ Cuál es la molaridad de la disolución obtenida al disolver 12 g de K2Cr2O7 en agua destilada hasta obtener 250 mL de disolución? UNIVERSIDAD MILITAR NUEVAGRANADA UNIVERSIDAD MILITAR NUEVAGRANADA