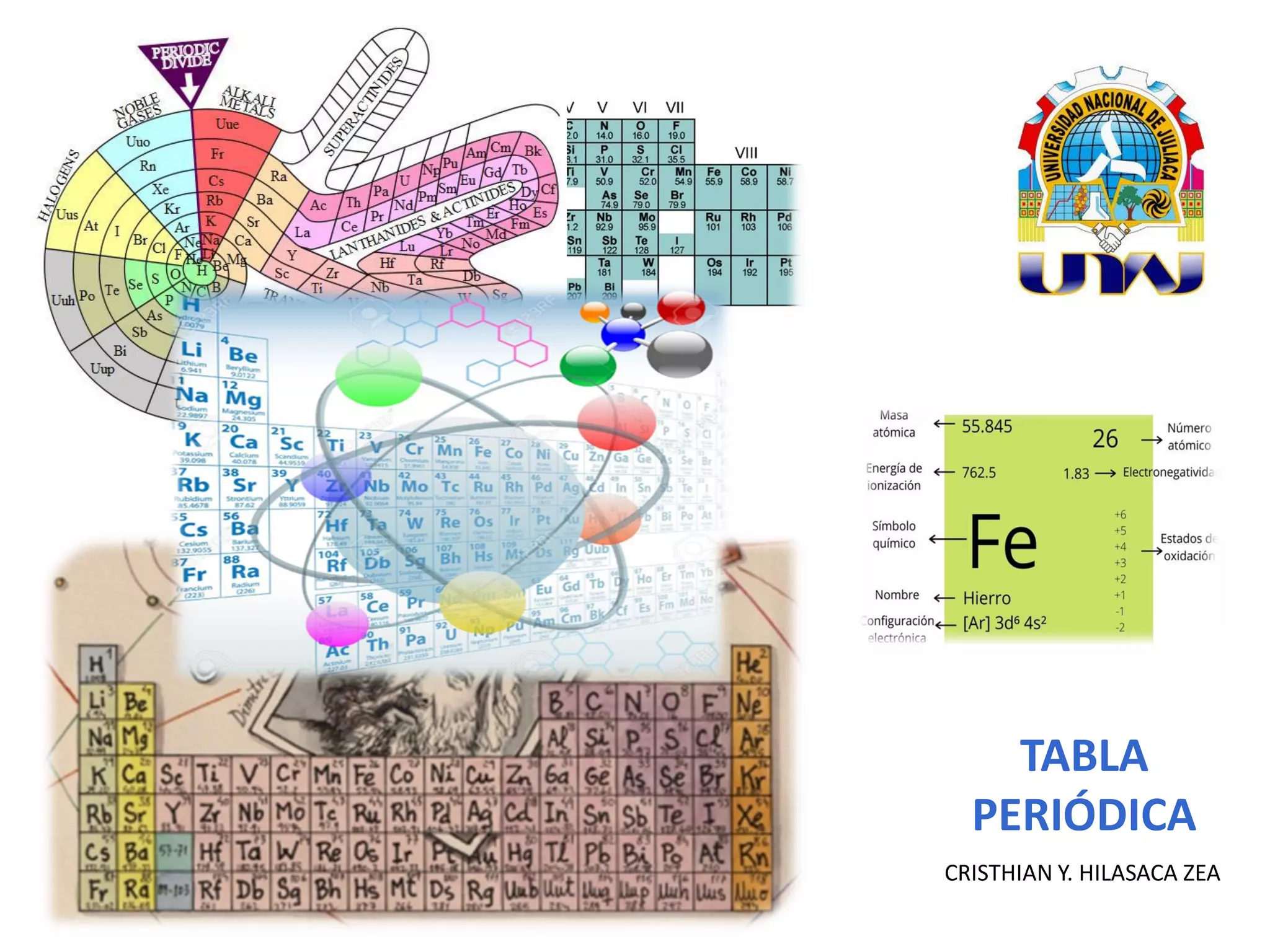
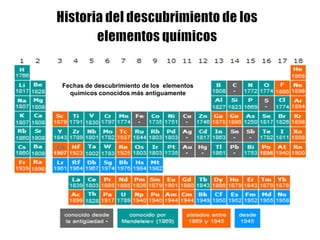
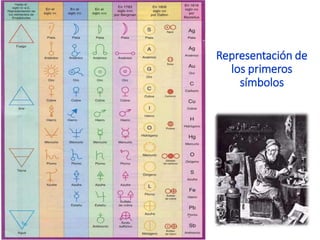
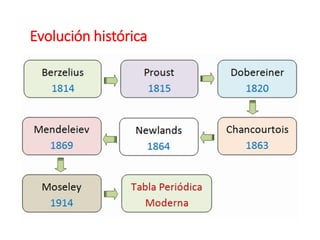
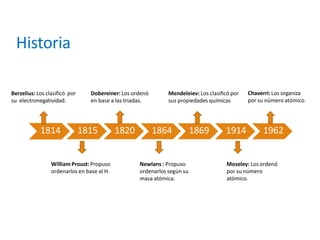
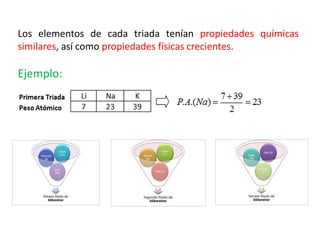
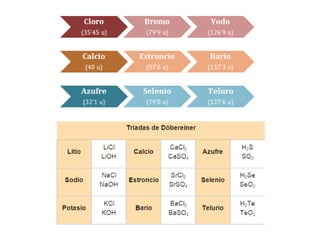
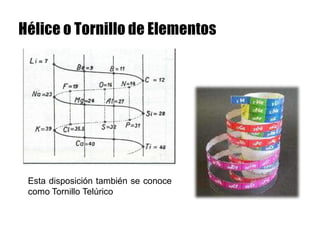
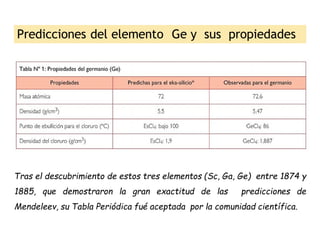
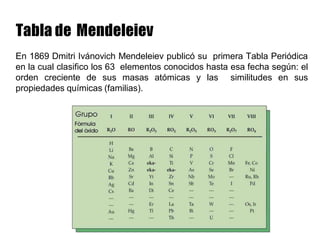
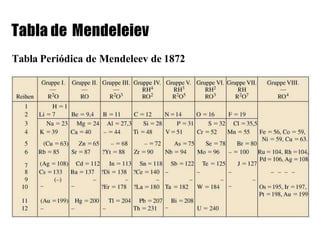
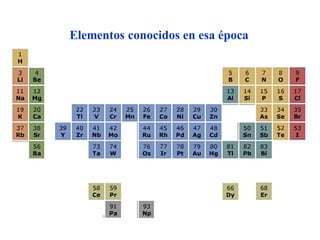
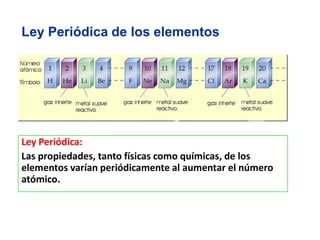
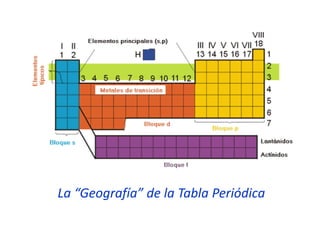
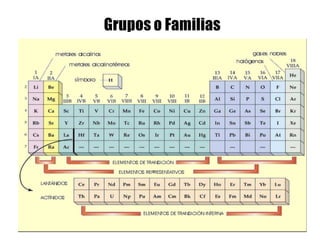
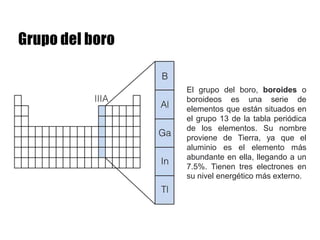
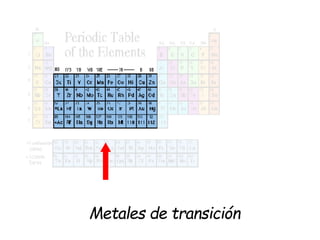
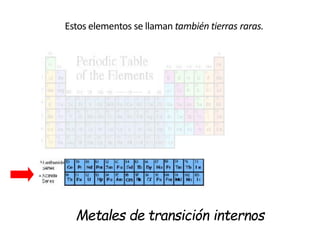
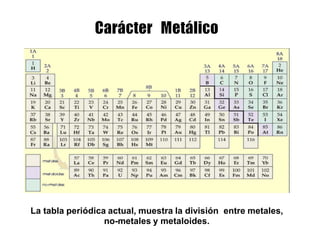
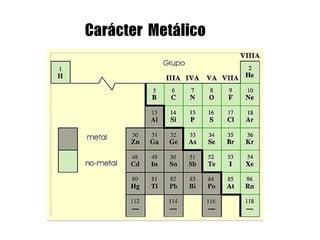
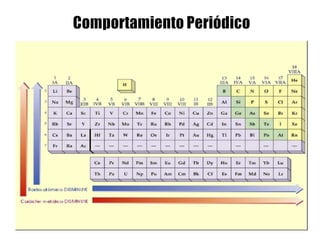
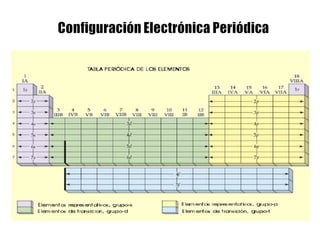
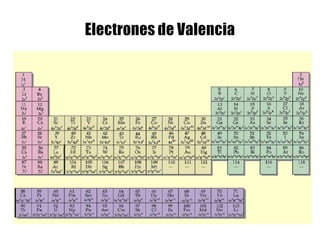
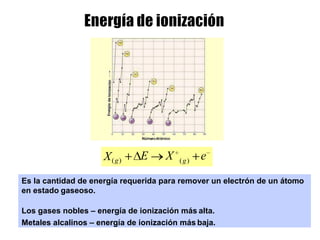
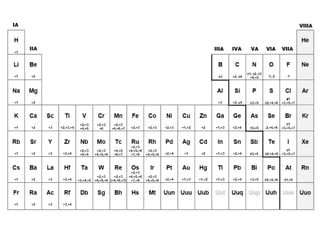
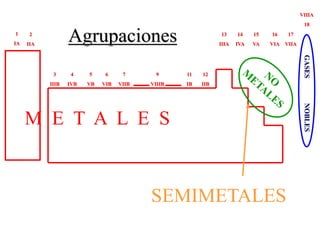
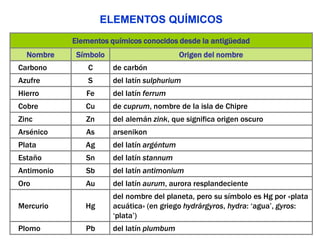
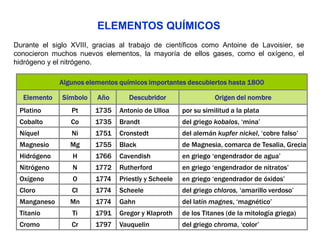
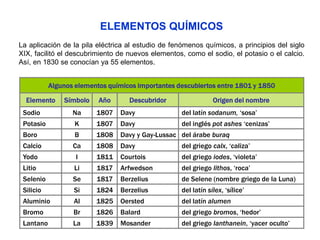
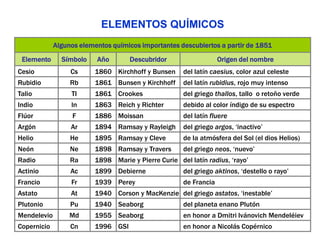
Este documento describe la evolución histórica de la tabla periódica de los elementos, desde sus primeras clasificaciones en el siglo XIX hasta la versión moderna. Explica cómo científicos como Newlands, Meyer, Mendeleiev y Moseley contribuyeron al desarrollo de la tabla ordenando los elementos de diferentes maneras y predijeron la existencia de nuevos elementos. La tabla periódica moderna ordena los 118 elementos conocidos por su número atómico.