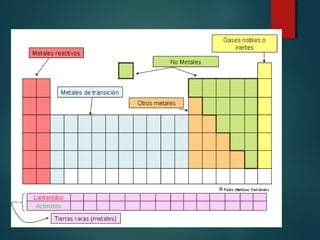
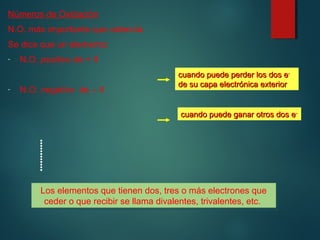
Este documento describe el sistema periódico de Mendeleyev, incluyendo que Mendeleyev ordenó los elementos en una tabla basada en sus masas atómicas y propiedades, con elementos similares en grupos verticales. Explica conceptos clave como número atómico, masa atómica, y valencia, y cómo estos determinan la ubicación de un elemento en la tabla periódica moderna.