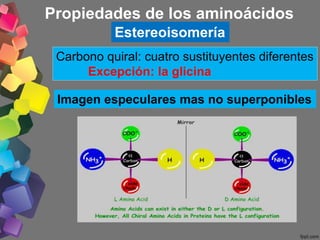
Este documento proporciona información general sobre los aminoácidos. Explica que los aminoácidos son componentes esenciales de las proteínas, son solubles en agua y están compuestos de carbono, oxígeno, hidrógeno y nitrógeno. Además, clasifica los aminoácidos y describe sus propiedades como su carácter anfótero y estereoisomería. Finalmente, menciona algunos péptidos de importancia biológica como la insulina y glucagón.