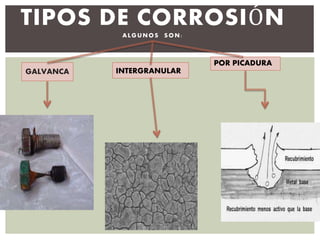
La corrosión es la destrucción de un material por una reacción química o electroquímica con el medio ambiente. Puede ser uniforme, afectando toda la superficie a igual velocidad, o localizada, afectando solo ciertas áreas. La corrosión puede ocurrir por medios químicos o electroquímicos y afecta una variedad de materiales como metales, cerámicas y polímeros. Algunos ejemplos comunes de corrosión incluyen las cañerías de agua, automóviles y electrodom