Denunciar
Compartir
Descargar para leer sin conexión
Más contenido relacionado
Similar a Óxidos Ácidos.pdf
Similar a Óxidos Ácidos.pdf (20)
Semana n° 15 diapositivas: NOMENCLATURA DE ÁCIDOS E HIDRÓXIDOS

Semana n° 15 diapositivas: NOMENCLATURA DE ÁCIDOS E HIDRÓXIDOS
Más de vanesacaiza
Más de vanesacaiza (6)
Último
Realitat o fake news? – Què causa el canvi climàtic? - Modificacions dels pat...

Realitat o fake news? – Què causa el canvi climàtic? - Modificacions dels pat...Pere Miquel Rosselló Espases
Último (20)
tema 6 2eso 2024. Ciencias Sociales. El final de la Edad Media en la Penínsul...

tema 6 2eso 2024. Ciencias Sociales. El final de la Edad Media en la Penínsul...
4. MATERIALES QUE SE EMPLEAN EN LAS ESTRUCTURAS.pptx

4. MATERIALES QUE SE EMPLEAN EN LAS ESTRUCTURAS.pptx
Síndrome piramidal 2024 según alvarez, farrera y wuani

Síndrome piramidal 2024 según alvarez, farrera y wuani
a propósito del estado su relevancia y definiciones

a propósito del estado su relevancia y definiciones
ACERTIJO CÁLCULOS MATEMÁGICOS EN LA CARRERA OLÍMPICA. Por JAVIER SOLIS NOYOLA

ACERTIJO CÁLCULOS MATEMÁGICOS EN LA CARRERA OLÍMPICA. Por JAVIER SOLIS NOYOLA
novelas-cortas--3.pdf Analisis introspectivo y retrospectivo, sintesis

novelas-cortas--3.pdf Analisis introspectivo y retrospectivo, sintesis
FICHA DE LA VIRGEN DE FÁTIMA.pdf educación religiosa primaria de menores

FICHA DE LA VIRGEN DE FÁTIMA.pdf educación religiosa primaria de menores
Estrategia Nacional de Refuerzo Escolar SJA Ccesa007.pdf

Estrategia Nacional de Refuerzo Escolar SJA Ccesa007.pdf
3. ELEMENTOS QUE SE EMPLEAN EN LAS ESTRUCTURAS.pptx

3. ELEMENTOS QUE SE EMPLEAN EN LAS ESTRUCTURAS.pptx
ANTOLOGIA COMPLETA ANITA LA ABEJITA PARA LA LECTOESCRITURA EN PRIMER GRADO.pdf

ANTOLOGIA COMPLETA ANITA LA ABEJITA PARA LA LECTOESCRITURA EN PRIMER GRADO.pdf
Realitat o fake news? – Què causa el canvi climàtic? - Modificacions dels pat...

Realitat o fake news? – Què causa el canvi climàtic? - Modificacions dels pat...
Óxidos Ácidos.pdf
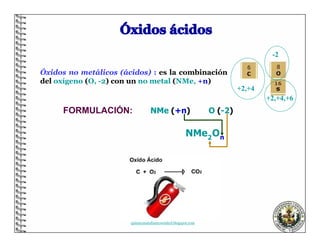
- 1. Óxidos no metálicos (ácidos) : es la combinación del oxígeno (O, -2) con un no metal (NMe, +n) -2 +2,+4 +2,+4,+6 FORMULACIÓN: NMe (+n) O (-2) NMe O 2 n quimicanataliamywendyd.blogspot.com
- 2. Como se llaman por la nomenclatura sistemática: Prefijoóxido + (di)NMe http://www.youtube.com/watch?v=7gpmWF2jWzo
- 3. Como se llaman por la nomenclatura stock: Óxido + NMe (nº romano valencia)
- 4. Como se llaman por la nomenclatura tradicional: hipo- NMe-oso NMe-oso NMe-ico per- NMe-ico Anhídrido + prezi.com http://www.youtube.com/watch?v=F07KMzAHa6Y
- 5. Compuesto Sistemática Stock Tradicional SO Monóxido de azufre Óxido de azufre (II) Anhídrido hiposulfuroso SO2 Dióxido de azufre Óxido de azufre (IV) Anhídrido sulfuroso SO3 Trióxido de azufre Óxido de azufre (VI) Anhídrido sulfúrico CO Monóxido de carbono Óxido de carbono (II) Anhídrido carbonoso CO2 Dióxido de carbono Óxido de carbono (IV) Anhídrido carbónico -2 +2,+4 +2,+4,+6 Comparación de las nomenclaturas
- 6. Los óxidos más importantes son los de carbono, nitrógeno y azufre. Sus átomos están unidos por enlaces covalentes y tienen características ácidas ya que al reaccionar con el agua forman los ácidos oxácidos. Los óxidos no metálicos se caracterizan por: Antiguamente se les llamaba anhídridos Poseen puntos de fusión y ebullición bajos.