E portafolio parte 3 verena
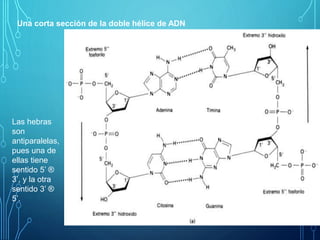
- 1. Las hebras son antiparalelas, pues una de ellas tiene sentido 5’ ® 3’, y la otra sentido 3’ ® 5’. Una corta sección de la doble hélice de ADN
- 2. ARN – ÁCIDO RIBONUCLEÍCO El ácido ribonucleíco se forma por la polimerización de ribonucleótidos. Estos a su vez se forman por la unión de: • a) un grupo fosfato. • b) ribosa, una aldopentosa cíclica y • c) una base nitrogenada unida al carbono 1’ de la ribosa, que puede ser citocina, guanina, adenina y uracilo. Esta última es una base similar a la timina.
- 3. • En general los ribonucleótidos se unen entre sí, formando una cadena simple, excepto en algunos virus, donde se encuentran formando cadenas dobles. • La cadena simple de ARN puede plegarse y presentar regiones con bases apareadas, de este modo se forman estructuras secundarias del ARN, que tienen muchas veces importancia funcional, como por ejemplo en los ARNt (ARN de transferencia).
- 4. Se conocen tres tipos principales de ARN y todos ellos participan de una u otra manera en la síntesis de las proteínas. Ellos son: •ARN mensajero (ARNm) •ARN ribosomal (ARNr) •ARN de transferencia (ARNt).
- 5. ARN MENSAJERO (ARNM) • Consiste en una molécula lineal de nucleótidos (monocatenaria), cuya secuencia de bases es complementaria a una porción de la secuencia de bases del ADN. • El ARNm dicta con exactitud la secuencia de aminoácidos en una cadena polipeptídica en particular. Las instrucciones residen en tripletes de bases a las que llamamos codones. Son los ARN más largos y pueden tener entre 1000 y 10000 nucleótidos
- 6. ARN RIBOSOMAL (ARNR) • Este tipo de ARN una vez transcripto, pasa al nucleolo donde se une a proteínas. De esta manera se forman las subunidades de los ribosomas. Aproximadamente dos terceras partes de los ribosomas corresponde a sus ARNr.
- 7. ARN DE TRANSFERENCIA (ARNT) • Este es el más pequeño de todos, tiene aproximadamente 75 nucleótidos en su cadena, además se pliega adquiriendo lo que se conoce con forma de hoja de trébol plegada. El ARNt se encarga de transportar los aminoácidos libres del citoplasma al lugar de síntesis proteica. En su estructura presenta un triplete de bases complementario de un codón determinado, lo que permitirá al ARNt reconocerlo con exactitud y dejar el aminoácido en el sitio correcto. A este triplete lo llamamos anticodón.
- 10. EL ADN Y EL ARN SE DIFERENCIAN: • el peso molecular del ADN es generalmente mayor que el del ARN • el azúcar del ARN es ribosa, y el del ADN es desoxirribosa • el ARN contiene la base nitrogenada uracilo, mientras que el ADN presenta timina • la configuración espacial del ADN es la de un doble helicoide, mientras que el ARN es un polinucleótido lineal monocatenario, que ocasionalmente puede presentar apareamientos intracatenarios
- 11. Diferencias estructurales entre el DNA y el RNA pentosa bases nitrogenadas estructura DNA RNA
- 12. NUCLEÓTIDOS
- 13. NUCLEÓTIDO Y SU CONTENIDO LA BASE NITROGENADA ESTA UNIDAA LA POSICIÓN 1 DEL ANILLO DE LA PENTOSA POR MEDIO DE UN ENLACE GLUCOSÍDICO A LA POSICIÓN N1 DE LAS PIRIMIDINAS O A LA N9 DE LAS PURINAS.
- 14. • Cuando el ADN o el ARN son rotos en sus nucleótidos constituyentes, la ruptura puede llevarse a cabo en cualquiera de los lados de los enlaces fosfodiester. Dependiendo de las circunstancias, los nucleótidos tienen su grupo fosfato unido a cualquiera de las posiciones 5´ ó 3´ de la pentosa:
- 15. • Todos los nucleótidos pueden existir en una forma en la cual hay más de un grupo fosfato unido a la posición 5´
- 16. NUCLEÓTIDOS • Los nucleótidos son los ésteres fosfóricos de los nucleósidos. Están formados por la unión de un grupo fosfato al carbono 5’ de una pentosa. • A su vez la pentosa lleva unida al carbono 1’ una base nitrogenada. Se forman cuando se une ácido fosfórico a un nucleósido en forma de ión fosfato (PO43-) mediante un enlace éster en alguno de los grupos -OH del monosacárido.
- 17. • Se nombra como el nucleósido del que proceden eliminando la a final y añadiendo la terminación 5´-fosfato, o bien monofosfato; por ejemplo, adenosín-5´-fosfato o adenosín-5´-monofosfato (AMP). • Los nucleótidos pueden formarse con cualquier nucleósido, con una nomenclatura idéntica. • Veamos a continuación, a modo de ejemplo, los nucleótidos de Adenosina:
- 18. ADENOSINA MONOFOSFATOS Nombre sistemático Abreviatura • Adenosina-5'-monofosfato 5'-AMP, AMP • Adenosina-3'-monofosfato 3'-AMP • Adenosina-2'-monofosfato 2'-AMP • Adenosina Polifosfatos Nombre sistemático Abreviatura • Adenosina-5'-monofosfato AMP • Adenosina-5'-difosfato ADP • Adenosina-5'-trifosfato ATP
- 19. • Molécula de ATP (adenosín trifosfato): Es el portador primario de energía de la célula. • El fosfato puede aparecer esterificado a dos grupos simultáneamente. Tal es el caso de los llamados Nucleótidos Cíclicos. • Veremos de ejemplo los nucleótidos de las cuatro bases que forman parte del DNA:
- 20. DESOXINUCLEÓTIDOS Nombre sistemático Abreviatura • Desoxiadenosina-5'-monofosfato dAMP • Desoxiguanosina-5'-monofosfato dGMP • Desoxicitidina-5'-monofosfato dCMP • Timidina-5'-monofosfato TMP
- 21. Aparte de su carácter como monómeros de ácidos nucleicos, la estructura de nucleótido está generalizada entre las biomoléculas, y particularmente como coenzimas. • Niacina adenina dinucleótido (forma reducida, NADH). • Flavina Adenina dinucleótido (FAD). • Coenzima A (forma acetilada, Acetil-CoA). • Uridina difosfato glucosa (UDPG).
- 22. ESTRUCTURA
- 23. • Cada nucleótido es un ensamblado de tres componentes. • Bases nitrogenadas: derivan de los compuestos heterocíclicos aromáticos purina y pirimidina. • Bases nitrogenadas purínicas: son la adenina (A) y la guanina (G). Ambas forman parte del ADN y del ARN. • Bases nitrogenadas pirimidínicas: son la timina (T), la citosina (C) y el uracilo (U). La timina y la citosina intervienen en la formación del ADN. En el ARN aparecen la citosina y el uracilo. • Bases nitrogenadas isoaloxacínicas: la flavina (F). No forma parte del ADN o del ARN, pero sí de algunos compuestos importantes como el FAD.
- 24. • Pentosa: el azúcar de cinco átomos de carbono; puede ser ribosa (ARN) o desoxirribosa (ADN). La diferencia entre ambos es que el ARN sí posee un grupo OH en el segundo carbono. • Ácido fosfórico: de fórmula H3PO4. Cada nucleótido puede contener uno (nucleótidos-monofosfato, como el AMP), dos (nucleótidos-difosfato, como el ADP) o tres (nucleótidos- trifosfato, como el ATP) grupos fosfato.
- 25. COMPOSICIÓN DE LOS ÁCIDOS NUCLEICOS: NUCLEÓTIDOS Existen dos tipos de ácidos nucleicos, el ácido desoxirribonucleico o ADN y el ácido ribonucleico o ARN, que se diferencian en: • El azúcar (pentosa) que contienen: la desoxirribosa en el ADN y la ribosa en el ARN.
- 26. Las bases nitrogenadas que contienen: adenina, guanina, citosina y timina en el ADN; y adenina, guanina, citosina y uraciloen el ARN.
- 27. • La unión formada por la pentosa y la base nitrogenada se denomina "nucleósido" y la unión del nucleósido con un grupo fosfórico se denomina "nucleótido".
- 28. • Los nucleótidos se unen entre sí para formar el polinucleótido por uniones fosfodiester entre el carbono 5' de un nucleótido y el carbono 3' del siguiente:
- 29. FORMACIÓN • Los nucleótidos resultan de la unión mediante enlace éster de la pentosa de un nucleósido con una molécula de ácido fosfórico. Esta unión, en la que se libera una molécula de agua, puede producirse en cualquiera de los grupos hidroxilo libres de la pentosa.
- 30. • También es habitual nombrar a los nucleótidos como fosfatos de los correspondientes nucleósidos; por ejemplo, el ATP es el trifosfato de adenosina o adenosín-trifosfato.
- 31. FUNCIONES DE LOS NUCLEÓTIDOS. • Además de ser los sillares estructurales de los ácidos nucleicos, los nucleótidos desempeñan en las células otras funciones no menos importantes. • En concreto, el trifosfato de adenosina (ATP) actúa universalmente en todas las células transportando energía, en forma de energía de enlace de su grupo fosfato terminal, desde los procesos metabólicos que la liberan hasta aquellos que la requieren.
- 32. • En algunas reacciones del metabolismo, otros nucleótidos trifosfato como el GTP, CTP y UTP, pueden sustituir al ATP en este papel.
- 34. LEYES DE LA TERMODINÁMICA APLICADA A LOS SISTEMAS BIOLÓGICOS • La termodinámica se refiere al estudio de la transferencia de energía que se produce entre moléculas o conjuntos de moléculas, el elemento o conjunto particular de elementos de interés (que podría ser algo tan pequeño como una célula o tan grande como un ecosistema) se llama sistema, mientras que todo lo que no está incluido en el sistema que hemos definido se llama entorno
- 35. LEYES DE LA TERMODINÁMICA APLICADA A LOS SISTEMAS BIOLÓGICOS • Hay tres tipos de sistemas en la termodinámica: • Sistema abierto • Sistema cerrado • Sistema aislado
- 36. SISTEMA ABIERTO: • Puede intercambiar energía y materia con su entorno.
- 37. SISTEMA CERRADO: • Por el contrario, solo puede intercambiar energía con sus alrededores, no materia.
- 38. SISTEMA AISLADO: • Es aquel que no puede intercambiar ni materia ni energía con su entorno. Es difícil encontrarse con sistema aislado perfecto. Los elementos en el interior pueden intercambiar energía entre sí
- 39. LA PRIMERA LEY DE LA TERMODINÁMICA • Se refiere a la cantidad total de energía en el universo, y en particular declara que esta cantidad total no cambia.
- 40. LA SEGUNDA LEY DE LA TERMODINÁMICA • Según la primera ley de la termodinámica la energía no puede ser creada ni destruida, pero puede cambiar de formas más útiles a formas menos útiles.
- 41. LA ENTROPÍA Y LA SEGUNDA LEY DE LA TERMODINÁMICA • El grado de aleatoriedad o desorden en un sistema se llama entropía.
- 42. LA ENTROPÍA EN LOS SISTEMAS BIOLÓGICOS • Una de las implicaciones de la segunda ley de la termodinámica es que, para que el proceso se lleve a cabo, de algún modo debe aumentar la entropía del universo.
- 43. REACCIONES BIOQUÍMICAS COMUNES • Una reacción química es un proceso que forma y rompe enlaces químicos que mantienen unidos a los átomos. • Las reacciones químicas convierten un grupo de sustancias, los cuales son; los reactivos, en otro grupo, los productos. • Las reacciones químicas pueden ser: exergonicas endergónicas
- 44. REACCIÓN EXERGÓNICA • El termino exergónica proviene del griego y significa sale energía, se le llama aquella reacción en la que los reactivos contienen más energía que los productos. • Por ejemplo la glucosa que los cuerpos de los corredores utilizan como combustible, contiene más energía que el dióxido de carbono y el agua que se produce cuando ese azúcar se descompone.
- 45. REACCIÓN ENDERGÓNICAS • El término endergónicas significa entra energía • Es aquella en la que los productos contienen más energía que los reactivos. • Según la segunda ley de la termodinámica las reacciones endergónicas, requieren un aporte de energía, de alguna fuente externa.
- 46. ENTROPÍA • En química hay tres grandes conceptos basados en la idea de la entropía: • Estados Intramoleculares (Grados de libertad) • Estructuras Intermoleculares • Número de posibilidades
- 47. LA ENERGÍA LIBRE GIBBS
- 48. Diagrama A Diagrama B - La energía libre de los productos es menor que la de los reactantes. - Al ser Gproductos menor que Greactivos, ΔG menor que cero (de valor negativo). - El proceso es espontáneo en el sentido directo. - La energía libre de los productos es mayor que la de los reactantes. - Al ser Gproductos mayor que Greactivos, ΔG mayor que cero (de valor positivo). - El proceso no es espontáneo en sentido directo. Pudiendo deducir al analizar los diagramas que:
- 49. COMPUESTOS DE ALTA ENERGÍA CELULAR ATP • Compuestos de alta energía: se caracterizan por tener uno o más enlaces que liberan un gran volumen de energía libre a través del catabolismo. • Adenosintrifosfato: El ATP es uno de los compuestos llamados nucleótidos.
- 50. RAZONES QUÍMICAS DE LA TENDENCIA A LA HIDRÓLISIS DEL ATP • Energía de estabilización por resonancia • Tensión eléctrica entre las cargas negativas vecinas existente en el ATP • Solvatación: la tendencia natural es hacia una mayor solvatación. La energía de solvatación es mayor en los productos de hidrólisis que en el ATP.
- 51. FOSFOENOLPIRUVATO • Posee un enlace fosfato de alta energía implicado en la glucólisis y gluconeogénesis. • En la glicolisis, transfiere su grupo fosfato, por acción de la piruvatokinasa, generando piruvato y adenosíntrifosfato (ATP) mediante el proceso de fosforilación a nivel de sustrato.
- 52. DERIVADOS DE COENZIMA A • El tioéster se forma cuando un sulfhidrilo (cuya forma general se escribe con un grupo orgánico, R, unido con el azufre y el hidrógeno, es decir R-SH) se le añade un ácido carboxílico (R'-COOH).
- 53. 1,3 DI FOSFATOGLICERIDO • Es una molécula que contiene enlaces de altamente energéticos, el 1,3 difosfatoglicerido, es utilizada como fuente de energía en la glicolisis y en el ciclo de krebs.
- 54. FOSFOCREATINA • La fosfocreatina es un compuesto químico con un enlace de fosfato de alta energía, siendo su representación química: Creatina PO3.
- 55. REACCIONES DE ÓXIDO REDUCCIÓN BIOLÓGICA Y ACOPLAMIENTO DE REACCIONES EN LOS SISTEMAS BIOLÓGICOS • “Las reacciones de oxidación-reducción llamadas también redox; son aquellas en las que tienen lugar una transferencia de electrones desde un dador electrónico o agente reductor, hasta un aceptor electrónico o el agente oxidante.
- 57. REACCIONES DE ÓXIDO REDUCCIÓN BIOLÓGICA Y ACOPLAMIENTO DE REACCIONES EN LOS SISTEMAS BIOLÓGICOS Ejemplos de reacciones: • La oxidación del sodio y la reducción del cloro. • Otra reacción de oxidación-reducción; oxidación parcial del metano (CH4).
- 58. QUIMIÓTROFOS • Ejemplos de rutas bioenergéticas, en las que existen reacciones redox: • Glucólisis • Fermentación • Ciclo de Krebs • Cadena respiratoria • Fosforilación oxidativa • Ciclo de Calvin • Fotosíntesis
- 59. RUTAS CATABÓLICAS, ANABÓLICAS Y ANAPLETÓRICAS • Entre los distintos tipos de biomoléculas orgánicas que forman parte de las células vivas hay que distinguir por un lado a las proteínas y los ácidos nucleicos, cuya misión fundamental es el almacenamiento, transmisión y expresión de la información genética ("biomoléculas informativas"), y por otro a los glúcidos y lípidos ("biomoléculas energéticas") cuya principal misión es la de proporcionar energía para los distintos procesos celulares y que por lo tanto están llamados a ser los grandes protagonistas del catabolismo.
- 60. CATABOLISMO DE AZÚCARES • Los monosacáridos diferentes de la glucosa, que en ocasiones pueden proceder de la hidrólisis de distintos tipos de oligosacáridos, se transforman en glucosa o en algunos de los intermediarios de su degradación, mediante reacciones de isomerización.
- 61. GLUCOLISIS
- 62. CICLO DE KREBS
- 63. CADENA RESPIRATORIA • Los electrones de los coenzimas reducidos NADH y FADH2 procedentes de las anteriores etapas del catabolismo de los azúcares pueden ser ahora cedidos a una de los varios miles de cadenas de transportadores de electrones que se encuentran distribuidas por toda la superficie de la membrana mitocondrial interna y que reciben el nombre de cadenas respiratorias.
- 64. CATABOLISMO DE LÍPIDOS. • Dado que los lípidos que con más frecuencia degradan las células para obtener energía son los triacilglicéridos o grasas neutras, analizaremos sus rutas degradativas como modelo del catabolismo de los lípidos en general.
- 65. CATABOLISMO DE PROTEÍNAS. • Por lo general las células no utilizan las proteínas como combustible metabólico más que en casos de extrema necesidad. • Sin embargo, las células están renovando constantemente sus proteínas.
- 66. CATABOLISMO DE LOS ÁCIDOS NUCLEICOS • a) Pentosas.- mediante la ruta de las pentosas. • b) Ácido fosfórico.- se excreta como tal por la orina • c) Bases nitrogenadas.- se degradan siguiendo complejas rutas que dan lugar
- 68. ANABOLISMO • Es el conjunto de procesos del metabolismo que tienen como resultado la síntesis de componentes celulares a partir de precursores de baja masa molecular por lo que también recibe el nombre de biosíntesis.
- 69. ANAPLETÓRICOS • Las reacciones anapleróticas son aquellas que proporcionan intermediarios del ciclo de los ácidos tricarboxílicos (TCA, del inglés) o ciclo del ácido cítrico o ciclo de Krebs.
- 70. PRINCIPIOS DE REGULACIÓN METABÓLICA • Ciertas vías metabólicas son comunes a todas las células de un organismo, son las rutas centrales del metabolismo (como la glucólisis).
- 71. PRINCIPIOS DE REGULACIÓN METABÓLICA • Hígado: La actividad metabólica del hígado es esencial para suministrar combustible al cerebro, al músculo y al resto de los tejidos del cuerpo. • Cerebro: La glucosa es prácticamente el único combustible utilizado por el cerebro humano, excepto durante el ayuno prolongado.
- 72. REGULACIÓN DE ACTIVIDAD ENZIMÁTICA • La cantidad de una enzima se puede controlar regulando la velocidad de su síntesis o de su degradación. • Las enzimas reguladoras se pueden clasificar por el método de su modulación: modulación alostérica no covalente o modificación covalente. • Un inhibidor o activador alostérico, que también se llama modulador alostérico o efector alostérico, se une al sitio regulador y causa un cambio de conformación en la enzima reguladora.
- 73. INHIBICIÓN • Los inhibidores son moléculas o iones que interactúan con la enzima y disminuyen su actividad catalítica.
- 74. INHIBICIÓN COMPETITIVA. • La característica más importante de este tipo de inhibición es que el sustrato y el inhibidor son mutuamente excluyentes, por lo que no se forma el complejo ternario IES.
- 76. INHIBICIÓN NO COMPETITIVA • En la inhibición no competitiva clásica, además de formarse los complejos binarios entre la enzima y el inhibidor (EI) y la enzima y el sustrato (ES), se puede también formar el complejo ternario entre enzima, inhibidor y sustrato (EIS).
- 77. INHIBICIÓN ACOMPETITIVA • En la inhibición de tipo acompetitiva, el inhibidor no interactúa con la enzima libre, pero si con el complejo enzima-sustrato (ES).
- 78. INHIBIDORES IRREVERSIBLES • Los inhibidores irreversibles se unen por medio de enlaces covalentes a los grupos funcionales de la enzima, por lo que la actividad de ésta se pierde de manera permanente.
- 79. MODIFICACIÓN COVALENTE • La modificación covalente de las enzimas reguladas es reversible, pero suele requerir enzimas modificadoras adicionales para su activación e inactivación.
- 80. CONCENTRACIÓN DE ENZIMAS • La concentración de enzimas es otro de los factores que afecta la velocidad, cuanto mayor cantidad de enzima este presente, mayor será la velocidad que se alcanzará, debido a que necesito más cantidad de sustrato para alcanzar la saturación.
- 81. REGULACIÓN A NIVEL DNA • La regulación en la dosis del producto de un gen es uno de los mecanismos que actúan a nivel del ADN.
- 82. REGULACIÓN A NIVEL DNA • INDUCCIÓN: capacidad que tienen los organismos para sintetizar ciertas enzimas solo cuando las necesitan. El termino inducción se refiere también a la activación de la trascripción de un gen como consecuencia de un inductor que interactiva con una proteína reguladora. • REPRESOR: proteína que se une a la secuencia del operador de un gen, evitando así la trascripción de dicho gen.
- 84. Desde el punto de vista químico OXIDACIÓN • Ganancia de oxígeno • Pérdida de electrones • Pérdida de hidrógeno REDUCCIÓN • Pérdida de oxígeno • Ganancia de electrones • Ganancia de hidrógeno (en compuestos orgánicos) El uso principal del OXÍGENO es en la RESPIRACIÓN Y ESTE ES EL PROCESO POR EL CUAL LAS CÉLULAS OBTIENEN ENERGÍA EN FORMA DE ATP Este principio de OXIDO- REDUCCIÓN se aplica a los sistemas bioquímicos y es un concepto importante para la comprensión de la naturaleza de las oxidaciones biológicas.
- 85. EN LOS SISTEMAS REDOX LOS CAMBIOS DE ENERGÍA LIBRE PUEDEN EXPRESARSE EN TÉRMINOS DEL POTENCIAL DE OXIDACIÓN – REDUCCIÓN LAS ENZIMAS QUE INTERVIENEN EN LOS PROCESOS REDOX SE DENOMINAN OXIDORREDUCTASAS
- 86. Oxidorreductasas Catalizan reacciones de oxido- reducción Ared + Box Aox + Bred A : es el reductor o dador electrónico; en el curso de la reacción se oxida (pierde electrones) B : es el oxidante o aceptor electrónico; en el curso de la reacción se reduce (gana electrones) En las reacciones redox, siempre tienen que estar presentes a la vez el aceptor y el dador electrónico
- 87. Estas reacciones son fuertemente exergónicas, en las cuales para evitar una liberación brusca de energía, no aprovechable por la célula, se libera en forma fraccionada.
- 88. DISTINTAS FORMAS EN QUE LA CELULA PUEDE TRANSFERIR ELECTRONES 1.- Transferencia de 1 e-: Fe +++ Fe++ 2.- Transferencia de un átomo de hidrógeno: (H+ + e-): AH2 + B A + BH2 3.- Transferencia de un ion Hidruro (:H-) AH2 + NAD+ → A + NADH + H+ 4.- Transferencia de e- desde un reductor orgánico al oxígeno: R-CH3 + ½ O2 RCH2-OH
- 89. • Gran parte de los sustratos oxidados en el organismo sufren deshidrogenación. • Las reacciones de deshidrogenación son catalizadas por las ENZIMAS DESHIDROGENASAS. • En estas reacciones el hidrógeno es captado por una coenzima. • Las coenzimas pueden ser: - Nicotinamida (NAD o NADP) - Flavina (FAD).
- 90. Flujo de electrones en la oxido-reducciones biológicas
- 91. RESPIRACIÓN CELULAR Es el conjunto de reacciones en las cuales el ác. pirúvico producido por la glucólisis se desdobla a CO2 y H2O y se producen 30 ATP. En las células eucariontes la respiración se realiza en la mitocondria.
- 93. LA MITOCONDRIA FÁBRICA DE ENERGÍA CELULAR ES EL SITIO DONDE TIENEN LUGAR EL TRANSPORTE ELECTRÓNICO Y LA FOSFORILACIÓN OXIDATIVA
- 96. La cadena transportadora de electrones • El NADH+H y el FADH2, obtenidos en el ciclo de Krebs, van a entrar en una cadena transportadora de electrones o cadena respiratoria, donde pasan los electrones, de una molécula reducida a otra oxidada, hasta el aceptor final que será el oxígeno molecular, que al reducirse formará agua.
- 97. CADENA DE TRANSPORTE ELECTRONICO • Los componentes de la cadena se encuentran en la membrana mitocondrial interna. • Reciben equivalentes de reducción de NADH Y FADH2 producidos en la matriz. • Los componentes actúan secuencialmente en orden creciente según sus potenciales de reducción. • La energía que se libera durante la transferencia electrónica está acoplada a varios procesos endergónicos entre los que se destaca la síntesis de ATP.
- 99. Reacciones de la cadena de transporte de electrones Con excepción de la coenzima Q, todos los miembros de esta cadena son proteínas. Pueden funcionar como enzimas como en el caso de varias deshidrogenasas. Pueden contener hierro como parte de su centro hierro-azufre . Los citocromos a y a3 contienen cobre.
- 100. Componentes de la cadena respiratoria Transportadores de electrones -Coenzimas hidrosolubles: NAD+ coenzimas de las deshidrogenasas NADP+ FMN se unen covalentemente a flavoproteínas FAD (grupo prostético), transportan 2 e- y 2 H+ - Quinonas: Coenzima Q – Ubiquinona, transportadores en medio no acuoso (membrana), transporta 1 e- y libera 2 H+ a la matriz - Citocromos b, c, c1, a y a3 : proteínas con grupo prostético hemo, transportan 1 e- - Proteínas ferro-sulfuradas: proteínas con Fe asociado a átomos de S, transfieren 1 e- por oxidación o reducción del Fe
Notas del editor
- Químicamente la oxidación se define como la pérdida de electrones y la reducción como la ganancia de ellos. En consecuencia la oxidación está siempre acompañada por la reducción de un aceptor de electrones. Este principio de OXIDO- REDUCCIÓN se aplica a los sistemas bioquímicos y es un concepto importante para la comprensión de la naturaleza de las oxidaciones biológicas. La vida de los animales superiores depende en forma absoluta del suministro de oxígeno.