Ing.quimica trabajo final para cargar
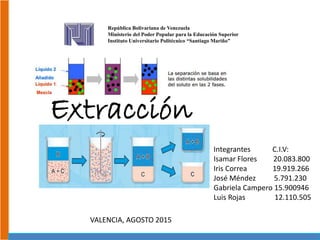
- 1. República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación Superior Instituto Universitario Politécnico “Santiago Mariño” Extracción Integrantes C.I.V: Isamar Flores 20.083.800 Iris Correa 19.919.266 José Méndez 5.791.230 Gabriela Campero 15.900946 Luis Rojas 12.110.505 VALENCIA, AGOSTO 2015
- 2. DEFINICIÓN OPERACIONES UNITARIAS Las Operaciones Unitarias estudian principalmente la transferencia y los cambios de energía, transferencias y cambios de materiales que se llevan a cabo por medios físicos, pero también por medios fisicoquímicos. El Proceso es el conjunto de operaciones unitarias. Así, el concepto esencial es por lo tanto dividir los procesos físicos de alimentos en operaciones unitarias básicas cada uno de los cuales pueden encontrarse en forma independiente y los cuales dependen de principios físicos coherentes. Dos Leyes muy importantes que todas las Operaciones Unitarias obedecen son las “Leyes de la conservación de masa y energía”
- 3. EXTRACCIÓN Proceso en el cual una mezcla líquida de dos especies (el soluto y el portador de la alimentación) se pone en contacto en un mezclador con un tercer líquido (el solvente), el cual es inmiscible con el portador de la alimentación. Cuando los líquidos entran en contacto, se transfiere soluto del portador de la alimentación al solvente, y se permite la mezcla combinada se divida en dos fases, las cuales se separan por gravedad en un decantador. Extracción líquido-líquido Extracción líquido-líquido simple: Es un método para separar componentes de una mezcla, depende de la diferencia de solubilidad del compuesto a extraer en dos disolventes diferentes. Cuando se agita un compuesto con dos disolventes inmiscibles, el compuesto se distribuye entre los dos disolventes. Extracción líquido-líquido continua: La solubilidad del compuesto a extraer en los disolventes de extracción habituales no es elevada se y se utilizar otro procedimiento que implica una extracción continua de la fase inicial en fase acuosa con porciones nuevas del disolvente orgánico de extracción. Extracción sólido-líquido Extracción sólido-líquido discontinua: La separación de una mezcla de compuestos sólidos también se puede llevar a cabo aprovechando diferencias de solubilidad de los mismos en un determinado disolvente. Extracción sólido-líquido continua: Es eficiente cuando se hace de manera continua con el disolvente de extracción caliente en un sistema cerrado, basada en un disolvente orgánico, previamente vaporizado.
- 4. EQUIPOS •Mezcladores-sedimentadores: Para lograr una transferencia de masa eficiente, con frecuencia se usa un mezclador mecánico que permite un contacto íntimo entre las dos fases líquidas EXTRACCIÓN POR ETAPAS Mezcladores- sedimentadores separado y combinado Torres de platos perforados: Varias etapas en contracorriente de alta capacidad, eficacia para sistemas de baja tensión superficial trabaja en fase continua pesada y dispersa ligera.
- 5. EQUIPOS Columnas de bandejas: Este tipo de columna trabaja en contracorriente con fase continua y pesada, baja tensión. Extracción por contacto continuo diferencial Columna pulsada: Una bomba pulsa el contenido de la columna a intervalos frecuentes la torre puede ser de platos perforados o de relleno utilizada en el tratamiento de líquidos corrosivos o radiactivos. Columna pulsada
- 6. EQUIPOS Extractor centrífugo: Aumentan la turbulencia y el grado de contacto empleando altas velocidades de rotación para líquidos de muy pequeña diferencia de densidad.
- 7. Ecuaciones de Balance de Materia y Energía BALANCE DE MATERIA Cuando se lleva a cabo una reacción química en determinado proceso, los procedimientos aplicados en balance de materia se complican. Además de los balances por componentes y global que se siguen formulando para las unidades en las que no ocurren transformaciones químicas, hay que tomar la información concerniente a la reacción química dada que se lleva a cabo en una reacción. Ecuación. ENTRADA + GENERACIÓN= SALIDA + CONSUMO REACTOR SEPARADOR F=75 mol a/min E=100 mol a/min 25 MOL A/MIN 75 mol B/min R= 25 mol A/min
- 8. Ecuaciones de Balance de Materia y Energía BALANCE DE ENERGÍA El balance de energía al igual que el balance de materia es una derivación matemática de la "Ley de la conservación de la energía" (Primera Ley de La Termodinámica), es decir "La energía no se crea ni se destruye, solo se transforma". El balance de energía es un principio físico fundamental al igual que la conservación de masa, que es aplicado para determinar las cantidades de energía que es intercambiada y acumulada dentro de un sistema.
- 9. Balance de Materia y Energía Descripción esquemática del balance de materia y energía (descripción gráfica incluyendo el volumen de control) Un volumen de control es un espacio arbitrario que se instituye con el objeto de estudio. Formado por el espacio delimitado por una superficie de control (SC) cerrada, real o virtualmente, donde una de sus características, será la permanencia de la forma y el tamaño del volumen delimitado. Es También un sistema termodinámico con la propiedad añadida que se admite a la posibilidad de entradas y salida de masa. El volumen de control intercambia calor con una fuente térmica y trabajo con una o varias fuentes de trabajo, el cambio de la masa dentro del volumen está dada por la diferencia entre el flujo másico de entrada y el flujo másico de salida. Para un único flujo que entra al volumen de control y un único flujo de salida.
- 10. CONDICIONES El estado estacionario es aquel en el que no existen cambios de variables de proceso. Por ejemplo, en un intercambiador de calor, puede entrar agua a 25 C y salir a 80 C. Claro que el agua ha cambiado su temperatura, pero en el estado estacionario, la temperatura del agua a la entrada y a la salida siempre será la misma. En la práctica el estado estacionario es más flexible, las variables cambian dentro de un rango de tolerancia. ESTADO ESTACIONARIO
- 11. LIXIVIACIÓN Extracción sólido-líquido, es un proceso en el que un disolvente líquido pasa a través de un sólido pulverizado para que se produzca la elución de uno o más de los componentes solubles del sólido. Difiere poco del lavado o filtrado de sólidos. Algunos ejemplos: - El azúcar se separa de la remolacha con agua caliente. - Los aceites vegetales se recuperan a partir de semillas mediante la lixiviación con disolventes orgánicos. - La extracción de colorantes se realiza a partir de materias sólidas por lixiviación con alcohol o sosa. LIXIVIACIÓN
- 12. CRISTALIZACIÓN CRISTALIZACIÓN La cristalización es una operación de transferencia de materia en la que se produce la formación de un sólido (cristal o precipitado) a partir de una fase homogénea (soluto en disolución o en un fundido). Destaca sobre otros procesos de separación por su potencial para combinar purificación y producción de partículas en un solo proceso. Comparado con otras operaciones de separación la cristalización en disolución presenta:
- 13. CRISTALIZACIÓN Ventajas • El factor de separación es elevado (producto casi sin impurezas). En bastantes ocasiones se puede recuperar un producto con una pureza mayor del 99% en una única etapa de cristalización, separación y lavado. • Controlando las condiciones del proceso se obtiene un producto sólido constituido por partículas discretas de tamaño y forma adecuados para ser directamente empaquetado y vendido (el mercado actual reclama productos con propiedades específicas). • Precisa menos energía para la separación que la destilación u otros métodos empleados habitualmente y puede realizarse a temperaturas relativamente bajas.
- 14. CRISTALIZACIÓN Desventajas • En general, ni se puede purificar más de un componente ni recuperar todo el soluto en una única etapa. Es necesario equipo adicional para retirar el soluto restante de las aguas madres. • La operación implica el manejo de sólidos, con los inconvenientes tecnológicos que esto conlleva. En la práctica supone una secuencia de procesado de sólidos, que incluye equipos de cristalización junto con otros de separación sólido-líquido y de secado. La cristalización es una operación de transferencia de materia que depende de la superficie del cristal. Cada factor cinético de cristalización está relacionado con los demás, con la velocidad de crecimiento y con el tiempo de residencia de cada partícula (balance de población). Existe una fuerte relación entre la sobresaturación (fuerza impulsora) y el área superficial de los cristales (relacionada con la CSD). Estas interacciones cristalizador/CSD pueden influir profundamente en la operación en estado estacionario de un cristalizador en continuo.
- 15. CRISTALIZACIÓN Los Siete Sistemas Cristalinos Existen siete clases de cristales, dependiendo de la distribución de los ejes a los que se refieren los ángulos: 1. Sistema cúbico. Tres ejes iguales que forman ángulos rectos entre sí.
- 16. CRISTALIZACIÓN 2. Sistema tetragonal. Tres ejes que forman ángulos rectos entre sí, con uno de los ejes más largo que los otros dos.
- 17. CRISTALIZACIÓN 3. Sistema ortorrómbico. Tres ejes a ángulos rectos entre sí, todos de tamaño diferente.
- 18. CRISTALIZACIÓN 4. Sistema hexagonal. Tres ejes iguales en un plano formando ángulos de 60” entre sí y un cuarto eje formando un ángulo recto con este plano y ‘ no necesariamente de la misma longitud.
- 19. CRISTALIZACIÓN 5. Sistema monoclínico. Tres ejes desiguales, dos a ángulos rectos en un plano y el tercero formando cierto ángulo con dicho plano.
- 20. CRISTALIZACIÓN 6. Sistema triclínico. Tres ejes desiguales que forman ángulos desiguales entre sí que no son de 60” ni de 90”.
- 21. CRISTALIZACIÓN 7. Sistema trigonal. Tres ejes iguales con la misma inclinación.
- 22. EJERCICIOS 1- Una pulpa de madera húmeda contiene 68% en peso de agua. Después de secarla se determina que se ha eliminado el 55% de agua original de la pulpa. Calcule la composición de la pulpa seca y su peso para una alimentación de 1000kg/min de pulpa húmeda SECADOR 1000 kg/min purga húmeda 68% Agua C, agua B, purga seca 45% agua 1000 = B + C – C=1000- B…….. (1) 0.68 (1000) = 0.45(B) + C…….. (2) Reemplazando en (1) en (2) 380=0.45(B) + 1000-B 581.81 kg/h de purpa seca La composición de purpa seca es el 45% de agua y el 55% de agua.
- 23. EJERCICIOS
- 24. EJERCICIOS
- 25. EJERCICIOS
- 26. EJERCICIOS
- 27. EJERCICIOS
- 28. CONCLUCIÓN CONCLUSIONES: La ingeniería química es una rama de la ingeniería que tiene una sólida formación en ciencias básicas, ingeniería y gestión. Esta especialidad desempeña un papel fundamental en el diseño, mantenimiento, evaluación, optimización, simulación, planificación, construcción y operación de plantas para la producción de compuestos y productos cuya elaboración requiere de transformaciones físicas y químicas de la materia. El proceso químico llevado a cabo puede descomponerse en una serie ordenada llamada Operaciones Unitarias. Los procesos químicos en general y cada operación unitaria en particular tienen como objetivo modificar las condiciones de una determinada cantidad de materia en forma más útil a nuestros fines.