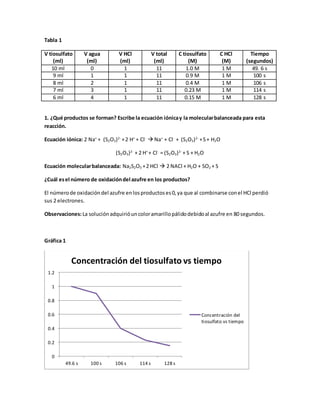
Efecto de la concentración y temperatura en la velocidad de reacción del tiosulfato de sodio y ácido clorhídrico
- 1. Tabla 1 V tiosulfato (ml) V agua (ml) V HCl (ml) V total (ml) C tiosulfato (M) C HCl (M) Tiempo (segundos) 10 ml 0 1 11 1.0 M 1 M 49. 6 s 9 ml 1 1 11 0.9 M 1 M 100 s 8 ml 2 1 11 0.4 M 1 M 106 s 7 ml 3 1 11 0.23 M 1 M 114 s 6 ml 4 1 11 0.15 M 1 M 128 s 1. ¿Qué productos se forman? Escribe la ecuación iónicay la molecularbalanceada para esta reacción. Ecuación iónica: 2 Na+ + (S2O3)2- +2 H+ + Cl- Na+ + Cl- + (S2O3)2- +S+ H2O (S2O3)2- + 2 H+ + Cl- = (S2O3)2- + S + H2O Ecuación molecularbalanceada: Na2S2O3 +2 HCl 2 NACl + H2O + SO2 + S ¿Cuál esel número de oxidacióndel azufre en los productos? El númerode oxidacióndel azufre enlosproductoses0,ya que al combinarse conel HCl perdió sus 2 electrones. Observaciones:La soluciónadquirióuncoloramarillopálidodebidoal azufre en 80 segundos. Gráfica 1 0 0.2 0.4 0.6 0.8 1 1.2 49.6 s 100 s 106 s 114 s 128 s Concentración del tiosulfato vs tiempo Concentración del tiosulfato vs tiempo
- 2. Tabla 2 Temperatura (°C) Tiempo(s) Velocidadde reacción 10 °C 1414 s 7.07X10-4 M/s 20 °C 170 s 5.88X10-3 M/s 35 °C 60 s 1.66X10-2 M/s 50 °C 45 s 2.22X10-2 M/s 80 °C 19 s 5.26X10-2 M/s Gráfica 2 Cuestionario 1. ¿Por qué la soluciónse enturbiaa medidaque pasa el tiempo? La soluciónse enturbiaamedidaque pasael tiempoporel precipitadoque se formaal reaccionar el ácidoclorhídrico con el tiosulfatode sodio. 2. ¿Para qué se detiene el cronómetro,cada vez,cuando se forma el precipitado? El cronómetrose detiene cadavezque se formael precipitado parapodermedirque tantoha variadola concentraciónde productosoreactivosen un determinadotiempo. 0 200 400 600 800 1000 1200 1400 1600 10 °C 20 °C 35 °C 50 °C 80 °C Temperatura vs tiempo Temperatura vs tiempo
- 3. 3. ¿Por qué se mantiene constante el volumende la disoluciónresultante de la mezcla? El volumende ladisoluciónresultante de lamezcla se mantieneconstante yaque de estaformase pudocomprobar comoafectabala concentraciónde tiosulfatoalareacción.El volumende la disoluciónresultantede lamezcla se mantuvoconstante graciasa que al disminuirla concentracióndel tiosulfato, aumentamosel volumendel agua. 4. ¿Por qué se varía sólola concentración inicial de tiosulfatoy no tambiénla de ácido clorhídrico? Porque al variar solamente ladel tiosulfatopudimosobservarcomolasdiferentesconcentraciones del mismoafectaronala reacción,ademásel HCl actúo como un descomponedordel mismo. 5. ¿Por qué es necesarioseguirtemperandola solucióncuando ocurre la reacción? Es necesarioseguirtemperandolasolucióncuandoocurre lareacción paradeterminarsi a éstale afectoun cambiode temperaturanuevo. 6. ¿Qué efectotiene la temperatura sobre la velocidadcon que ocurre la reacción para las mismas concentracionesiniciales? La temperaturaactúacomo uncatalizadorque aumentalavelocidadde lareacción,ya que permite el aumentode lascolisionesentre laspartículasde lasolución,razónporla cual el incrementode latemperaturasignificóunaumentoenlavelocidadde lareacción. 7. Calcular las velocidadesobtenidasdurante todo el experimentoexpresándolasen 𝒎𝒐𝒍𝒆𝒔 𝒍∗𝒔 Tabla 1: Velocidad de Reacción Tabla 2: Velocidad de Reacción 2.01 X 10-2 𝑴 𝒔 7.07X10-4 𝑴 𝒔 9.0X10-3 𝑴 𝒔 5.88X 10-3 𝑴 𝒔 3.77X10-3 𝑴 𝒔 1.66X10-2 𝑴 𝒔 2.04X10-3 𝑴 𝒔 2.22X10-2 𝑴 𝒔 1.17X10-3 𝑴 𝒔 5.26X10-2 𝑴 𝒔 Velocidadesde la tabla 1 Velocidad= 𝑪𝒐𝒏𝒄𝒆𝒏𝒕𝒓𝒂𝒄𝒊ó𝒏 𝑻𝒊𝒆𝒎𝒑𝒐 Velocidad= 𝟏 𝑴 𝟒𝟗.𝟔 𝒔 = 2.01 X 10-2 𝑴 𝒔 Velocidad= 𝟎.𝟗 𝑴 𝟏𝟎𝟎 𝒔 = 9.0X10-3 𝑴 𝒔
- 4. Velocidad= 𝟎.𝟒 𝑴 𝟏𝟎𝟔 𝒔 = 3.77X10-3 𝑴 𝒔 Velocidad= 𝟎.𝟐𝟑 𝑴 𝟏𝟏𝟒 𝒔 = 2.04X10-3 𝑴 𝒔 Velocidad= 𝟎.𝟏𝟓 𝑴 𝟏𝟐𝟖 𝒔 = 1.17X10-3 𝑴 𝒔 Velocidadesde la tabla 2 Velocidad= 𝑪𝒐𝒏𝒄𝒆𝒏𝒕𝒓𝒂𝒄𝒊ó𝒏 𝑻𝒊𝒆𝒎𝒑𝒐 Velocidad= 𝟏 𝑴 𝟏𝟒𝟏𝟒 𝒔 = 7.07X10-4 𝑴 𝒔 Velocidad= 𝟏 𝑴 𝟏𝟕𝟎 𝒔 = 5.88X 10-3 𝑴 𝒔 Velocidad= 𝟏 𝑴 𝟔𝟎 𝒔 = 1.66X10-2 𝑴 𝒔 Velocidad= 𝟏 𝑴 𝟒𝟓 𝒔 = 2.22X10-2 𝑴 𝒔 Velocidad= 𝟏 𝑴 𝟏𝟗 𝒔 = 5.26X10-2 𝑴 𝒔 Discusión Dependenciadel tiempode avance de una reacción entérminos de la concentración de los reactivos: A medidaque disminuíamoslaconcentracióndel tiosulfato,lavelocidadde reacción disminuíatambién, porqueal disminuir la concentracióndel tiosulfato, el equilibrio se desplazó hacia la derecha, en el sentido de formación de los productos, razón por la cual la velocidad disminuía. Dependenciadel tiempode avance de una reacción entérminos de la temperatura de los reactivos: A medidade que aumentábamoslatemperaturade losreactivos,lavelocidadde la reacciónaumentabayaque al aumentarla temperatura,aumentael númerode moléculascon una energíaigual o mayorque la energíade activación,conlo que aumentael númerode choques efectivos.
- 5. Conclusiones De acuerdocon lateoría cinético-molecularde lamateria,lasmoléculasconstituyentesde cualquiertipode sustanciase hallanencontinuaagitaciónvibrandoodesplazándose conuna energíacinética,que esdirectamenteproporcionalalatemperaturaabsolutaT a la que se encuentre dichasustancia.Experimentalmente se observóque lavelocidadde unareacción aumentóconforme se aumentólatemperatura,yaque al aumentarlatemperatura,laenergía cinéticade lasmoléculasde losreactivosaumentó,conloque loschoquessonmásviolentos poniéndoseenjuegoenunmayornúmerode elloslaenergíasuficiente comoparasuperaresa barrera que constituye laenergíade activación.El efectoconjuntode estos procesosindividuales se tradujoen que una mayorcantidadde reactivosse transformóenla unidadde tiempo,esdecir, la velocidadde reacciónaumentó notablemente. -BeatrizCedeño8-909-595 Por lamismarazón que son másfrecuenteslosaccidentesde tráficoenlas,«horas pico»,cuanto mayor seael númerode moléculasde losreactivospresentesenunmismovolumenmás fácilmente podráncolisionar.Asimismo,cuantomayorseael númerode colisionesque se producenenla unidadde tiempo,tantomásprobable serálarealizaciónde unchoque eficaz,esto es,de un choque que dé lugar a la transformaciónde lasmoléculas.De estaformase explicael hechoexperimentalmenteobservado,de que al aumentarlaconcentraciónde losreactivos aumente lavelocidadde lareacciónquímica. -ElíasÁvila8-920-1944
