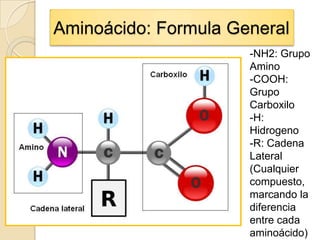
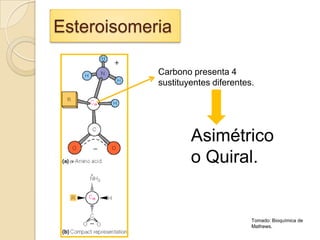
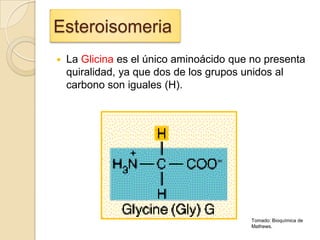
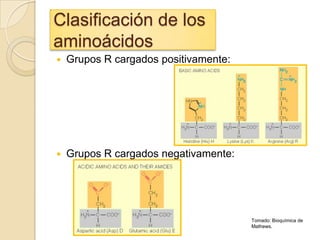
Los aminoácidos que forman proteínas contienen un grupo carboxilo, amino y cadena lateral unida al carbono alfa. Todos los aminoácidos excepto la glicina son asimétricos y existen en formas estereoisoméricas. Los aminoácidos se clasifican en 5 tipos según la polaridad de su grupo R a pH 7. Un zwitterion es la forma de un aminoácido en agua, pudiendo actuar como ácido o base.