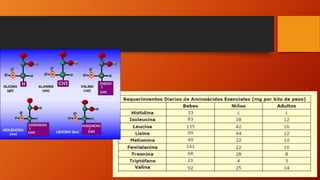
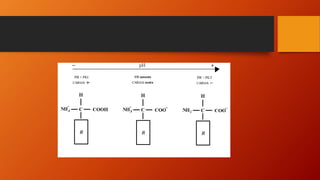
Los aminoácidos son las unidades básicas de las proteínas. Se componen de un grupo carboxilo, un grupo amino y una cadena lateral unidos a un carbono asimétrico. Existen 20 aminoácidos proteicos, de los cuales 8 son esenciales y deben obtenerse de la dieta. Los aminoácidos tienen propiedades anfóteras que les permiten actuar como sistemas tampón y regular el pH.