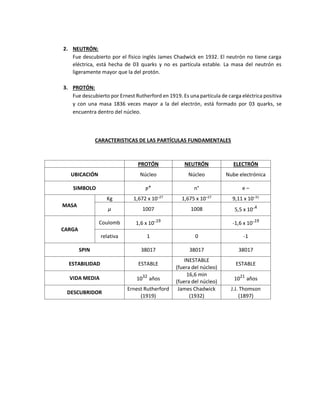
El átomo es la partícula más pequeña de un elemento químico que conserva sus propiedades. Está compuesto por un núcleo central con carga positiva que contiene protones y neutrones, y una zona extranuclear donde orbitan electrones con carga negativa. El núcleo concentra casi toda la masa del átomo y está compuesto principalmente por protones y neutrones. Los electrones se mueven alrededor del núcleo en órbitas.