Determinación de Entropía por método de conteo y pesada
•
0 recomendaciones•556 vistas
Determinación de Entropía molar de Plata y Cobre a 298.15K haciendo uso de los métodos de pesada, conteo y aproximación polinómica de Excel.
Denunciar
Compartir
Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
2020 ley de hess

El documento explica la Ley de Hess, que establece que la entalpía de una reacción química es la suma de las entalpías de las reacciones individuales que la componen. Proporciona un ejemplo de cómo calcular la entalpía de una reacción a partir de las entalpías de otras reacciones relacionadas, manipulando las ecuaciones químicas para cancelar los términos e identificar la reacción neta.
Proceso de electrolisis

Este documento resume los principales conceptos de la electrolisis. Explica que la electrolisis es un proceso en el que se utiliza la energía eléctrica para provocar una reacción química no espontánea. Describe varios ejemplos de electrolisis como la del NaCl fundido, el agua y disoluciones acuosas. También explica las leyes de Faraday que relacionan la corriente eléctrica, la carga y la masa de sustancias producidas o consumidas.
Informe propiedades term de una celda

Este documento describe un experimento para determinar las propiedades termodinámicas de una celda electroquímica de Daniell. Se construyó la celda y se midió su fuerza electromotriz a diferentes temperaturas. Los datos se usaron para calcular cambios en la energía libre de Gibbs, entalpía y entropía para la reacción de la celda. Los resultados experimentales se compararon con valores teóricos y se encontraron errores del 49.82% y 56.21% para la energía libre de Gibbs y la entalpía, respectivamente.
transferencia de calor 2

Este documento describe un curso de Transferencia de Calor II que incluye cinco temas: 1) Intercambiadores de calor, 2) Flujo laminar y convección libre, 3) Cálculos para condiciones de proceso, 4) Evaporación, y 5) Transferencia de calor por contacto directo y torres de enfriamiento. El objetivo es estudiar técnicas de diseño y evaluación de equipos de transferencia de calor usados en ingeniería química y aplicar conceptos fundamentales a sistemas térmicos industriales.
Tecnicas instrumentales ejercicios numericos - 3.4 - contenido de calcio y ...

Este documento describe un experimento para determinar el contenido de calcio (Ca) y magnesio (Mg) en una muestra de alfalfa mediante espectrofotometría de absorción atómica. La muestra se mineralizó y disolvió en una solución acuosa, de la cual se tomaron alícuotas para realizar dos experimentos de calibración, uno normal y otro por adición de patrones, a fin de comprobar posibles efectos de matriz. Los resultados de los experimentos permitieron calcular la concentración de Ca y Mg en la muestra original de
solucionario cap 3 treybal

El documento presenta varios problemas resueltos relacionados con el capítulo 3 de un libro sobre operaciones de transferencia de masa. El Problema 3.1 calcula el coeficiente de transferencia de masa y el espesor de la película para la absorción de amoniaco en ácido sulfúrico. El Problema 3.2 transforma una ecuación empírica para la evaporación de agua en cilindros a una forma basada en el número de Reynolds. El Problema 3.3 calcula la presión parcial promedio de vapor de agua en aire que
Laboratorio Reacciones químicas 

Este documento presenta las instrucciones para realizar 5 experimentos químicos en el laboratorio escolar. Los experimentos incluyen reacciones de sodio, magnesio, clorato de potasio con y sin dióxido de manganeso, nitrato de plata con cloruro de sodio, y zinc con ácido clorhídrico. El objetivo es clasificar los tipos de reacciones químicas que ocurren y escribir las ecuaciones químicas balanceadas correspondientes. El documento proporciona los materiales, reactivos, procedim
Experimento De Clement Y Desormes

Determinaremos la relación γ entre los calores específicos de un gas sometiéndolo a una expansión adiabática en un recipiente a temperatura ambiente y baja presión. Midiendo las diferencias de nivel del líquido en un manómetro antes y después de la expansión, calcularemos γ para varias repeticiones del experimento y determinaremos su valor promedio.
Recomendados
2020 ley de hess

El documento explica la Ley de Hess, que establece que la entalpía de una reacción química es la suma de las entalpías de las reacciones individuales que la componen. Proporciona un ejemplo de cómo calcular la entalpía de una reacción a partir de las entalpías de otras reacciones relacionadas, manipulando las ecuaciones químicas para cancelar los términos e identificar la reacción neta.
Proceso de electrolisis

Este documento resume los principales conceptos de la electrolisis. Explica que la electrolisis es un proceso en el que se utiliza la energía eléctrica para provocar una reacción química no espontánea. Describe varios ejemplos de electrolisis como la del NaCl fundido, el agua y disoluciones acuosas. También explica las leyes de Faraday que relacionan la corriente eléctrica, la carga y la masa de sustancias producidas o consumidas.
Informe propiedades term de una celda

Este documento describe un experimento para determinar las propiedades termodinámicas de una celda electroquímica de Daniell. Se construyó la celda y se midió su fuerza electromotriz a diferentes temperaturas. Los datos se usaron para calcular cambios en la energía libre de Gibbs, entalpía y entropía para la reacción de la celda. Los resultados experimentales se compararon con valores teóricos y se encontraron errores del 49.82% y 56.21% para la energía libre de Gibbs y la entalpía, respectivamente.
transferencia de calor 2

Este documento describe un curso de Transferencia de Calor II que incluye cinco temas: 1) Intercambiadores de calor, 2) Flujo laminar y convección libre, 3) Cálculos para condiciones de proceso, 4) Evaporación, y 5) Transferencia de calor por contacto directo y torres de enfriamiento. El objetivo es estudiar técnicas de diseño y evaluación de equipos de transferencia de calor usados en ingeniería química y aplicar conceptos fundamentales a sistemas térmicos industriales.
Tecnicas instrumentales ejercicios numericos - 3.4 - contenido de calcio y ...

Este documento describe un experimento para determinar el contenido de calcio (Ca) y magnesio (Mg) en una muestra de alfalfa mediante espectrofotometría de absorción atómica. La muestra se mineralizó y disolvió en una solución acuosa, de la cual se tomaron alícuotas para realizar dos experimentos de calibración, uno normal y otro por adición de patrones, a fin de comprobar posibles efectos de matriz. Los resultados de los experimentos permitieron calcular la concentración de Ca y Mg en la muestra original de
solucionario cap 3 treybal

El documento presenta varios problemas resueltos relacionados con el capítulo 3 de un libro sobre operaciones de transferencia de masa. El Problema 3.1 calcula el coeficiente de transferencia de masa y el espesor de la película para la absorción de amoniaco en ácido sulfúrico. El Problema 3.2 transforma una ecuación empírica para la evaporación de agua en cilindros a una forma basada en el número de Reynolds. El Problema 3.3 calcula la presión parcial promedio de vapor de agua en aire que
Laboratorio Reacciones químicas 

Este documento presenta las instrucciones para realizar 5 experimentos químicos en el laboratorio escolar. Los experimentos incluyen reacciones de sodio, magnesio, clorato de potasio con y sin dióxido de manganeso, nitrato de plata con cloruro de sodio, y zinc con ácido clorhídrico. El objetivo es clasificar los tipos de reacciones químicas que ocurren y escribir las ecuaciones químicas balanceadas correspondientes. El documento proporciona los materiales, reactivos, procedim
Experimento De Clement Y Desormes

Determinaremos la relación γ entre los calores específicos de un gas sometiéndolo a una expansión adiabática en un recipiente a temperatura ambiente y baja presión. Midiendo las diferencias de nivel del líquido en un manómetro antes y después de la expansión, calcularemos γ para varias repeticiones del experimento y determinaremos su valor promedio.
Practica 1.-ley-de-boyle

La práctica demostró que el volumen de un gas varía inversamente con la presión cuando se mantiene constante la temperatura. Al aumentar la presión sobre un gas atrapado en una jeringa, su volumen disminuyó. La gráfica de presión vs volumen mostró una relación inversa, confirmando la Ley de Boyle.
Transiciones electronicas

El documento describe los tipos de transiciones electrónicas que pueden ocurrir en moléculas dependiendo de su estructura. Menciona que las transiciones σ→σ*, n→σ*, n→π* y π→π* son posibles, y que las energías requeridas para las transiciones n→π* y π→π* conducen a absorción en el rango de 200-700 nm. También explica que la presencia de grupos funcionales específicos ("cromóforos") es necesaria para proporcionar orbitales que permitan la absorción
Química2 bach 8.5 grado de disociación

El documento habla sobre el grado de disociación, definido como la fracción de moléculas disociadas en equilibrio. Explica que la relación entre la constante de equilibrio Kc y el grado de disociación α depende del proceso químico específico. Proporciona dos ejemplos de cálculos de Kc y α para reacciones de descomposición de N2O4 y NH3.
TERMOQUÍMICA

Este documento presenta los conceptos fundamentales de la termoquímica en 12 puntos. Introduce sistemas, estados y funciones de estado, así como el primer principio de la termodinámica. Explica las relaciones entre energía interna, entalpía, calor y trabajo, y cómo calcular las entalpías estándar de reacción y formación usando la ley de Hess.
2013 2 taller transf masa int

1) El documento presenta varios problemas relacionados con la transferencia de masa interfacial en operaciones unitarias. Incluye cálculos de coeficientes de transferencia de masa, flujos y porcentajes de resistencia en películas para absorción de gases en torres de paredes mojadas.
2) Presenta ejercicios adicionales sobre absorción de ácido clorhídrico en aire y CO2 en soda cáustica, así como difusión de gases a través de membranas y evaporación en torres. Se piden cálculos de
Mecanismos.de.reaccion.en.quimica.organica.(problemas.selectos.y.soluciones)....

Este documento describe los pasos para configurar una nueva cuenta de correo electrónico en Gmail. Explica cómo iniciar sesión en Gmail, completar la configuración del perfil y agregar una dirección de correo electrónico.
Cálculo de la entalpía

El documento calcula las entalpías estándar de formación del FeO(s) y Fe2O3(s) utilizando la ley de Hess. Para el FeO(s), invierte y suma las reacciones (2) y (3), luego invierte y suma (4), obteniendo una reacción de formación cuya entalpía es -63.72 kcal. Para el Fe2O3(s), invierte y multiplica (1) por 3, luego suma (3) también multiplicada por 3, obteniendo una reacción de formación cuya entalpía es -196.
Catalisis

Este documento trata sobre los conceptos básicos de la catálisis, incluyendo definiciones de catalizador, tipos de catalizadores (homogéneos y heterogéneos), propiedades de los catalizadores, mecanismos de reacción catalítica, y tipos de catálisis como la catálisis ácida, básica, enzimática y heterogénea. También discute conceptos como la energía de activación, ecuación de Arrhenius, y ejemplos de reacciones catalizadas como la descomposición del per
39368106 7-6-punto-triple-so2

Este documento presenta la resolución de varios ejercicios relacionados con el equilibrio de fases en sistemas simples utilizando la ecuación de Clapeyron. Se calculan propiedades como puntos de ebullición, entalpías y entropías de vaporización para diferentes sustancias como éter etílico, agua, sodio y yodo. También se estiman cambios en los puntos de fusión y ebullición del agua y benceno al variar la presión.
Joule thomson

El experimento de Joule-Thompson mide cómo la temperatura de un gas cambia cuando se expande adiabáticamente. Para la mayoría de los gases, la temperatura disminuye durante la expansión, lo que significa que tienen un coeficiente de Joule-Thompson positivo. La expansión adiabática se utiliza en aplicaciones como extintores de incendios, refrigeración y para explicar la formación de nubes. El coeficiente de Joule-Thompson ayuda a determinar cómo varía la entalpía de un gas con respecto a los cambios de presión.
Equilibrio fisico

Este documento describe un experimento sobre el equilibrio físico entre las fases líquida y gaseosa de sustancias. Los estudiantes prepararon soluciones acuosas de NaCl y sacarosa a diferentes concentraciones y midieron cómo cambiaba su temperatura de ebullición en comparación con el agua pura, para determinar el aumento ebulloscópico y la molalidad de cada solución. Los resultados mostraron que una mayor concentración de soluto requiere una temperatura más alta para que la solución hierva.
Estimación de coeficientes de transporte

Historia y ecuaciones utilizadas para estimar coeficientes de transporte o para "reajustar" los coeficientes a condiciones físicas distintas de las experimentadas.
Calculo de la conductividad termica liquido y gases

Experimento del alambre caliento de platino y método pa calcular la conductividad termica de gases y liquido
Calorimetria Presion Constante (1).pptx

Este documento describe los principios de la calorimetría a presión constante y presenta varios casos de estudio para calcular cantidades de calor involucradas en reacciones químicas como la fusión, disolución y neutralización. También calcula el calor de combustión del ácido benzoico usando una bomba calorimétrica.
Fisica antologia fenómenos de transporte

Este documento presenta conceptos básicos sobre fenómenos de transporte. Explica que un sistema termodinámico está caracterizado por variables como presión, volumen y temperatura. Describe los tres tipos de sistemas: aislados, cerrados y abiertos. También distingue entre sistemas homogéneos y heterogéneos. Presenta información sobre transferencia de cantidad de movimiento, clasificación de fluidos newtonianos y no newtonianos, y la ley de Newton de la viscosidad.
Determinacion de las cantidades molares parciales

Este documento describe tres métodos (directo, analítico y gráfico) para determinar las propiedades molares parciales de una mezcla de dos componentes. Explica que el método gráfico involucra trazar una curva de la propiedad extensiva frente al número de moles de un componente y calcular la pendiente a diferentes composiciones. También describe cómo el método analítico usa ecuaciones diferenciales de la propiedad y fracciones molares para calcular las propiedades molares parciales.
TRIÁNGULO DE GIBBS: ENFOQUE GENERAL A REPRESENTACIÓN DE SISTEMAS TERNARIOS.

TRIÁNGULO DE GIBBS: ENFOQUE GENERAL A REPRESENTACIÓN DE SISTEMAS TERNARIOS.Irvin de Jesús Rodríguez Martínez
Este PDF, es la versión de una presentación realizada para dar un enfoque general de los diagramas triangulares (Triángulo de Gibbs) para sistemas ternarios.respuestas-ejercicios-exsamen 2.pdf

Este documento contiene tres ejercicios de cálculo relacionados con intercambiadores de calor. El primero calcula el área requerida para enfriar aceite usando agua en un intercambiador tubular. El segundo calcula la velocidad de flujo de agua y el coeficiente de transferencia de calor para enfriar aceite en un intercambiador contracorriente. El tercero calcula la cantidad de calor transferida, la temperatura de salida del agua y el número de placas necesarias para enfriar aceite en un interc
Termoquimica

Este documento trata sobre la termoquímica y resume sus principales conceptos y leyes. Explica que la termoquímica estudia los cambios energéticos en las reacciones químicas mediante la aplicación de la primera ley de la termodinámica. Define conceptos como la entalpía de reacción, las reacciones exotérmicas y endotérmicas, y expone leyes como la ley de Hess sobre la constancia del calor de reacción.
Problemas y cuestiones olimpiadas de quimica

Este documento presenta una colección de problemas y cuestiones de las Olimpiadas de Química de España entre 1996 y 2011. Explica que el objetivo es ofrecer material de apoyo para la enseñanza de la Química en bachillerato y primeros cursos universitarios. Además, incluye las soluciones a los problemas y cuestiones propuestos.
datos experimentales

laboratorio graficamos un conjunto de datos experimentales en el sistema de coordenadas cartesianas rectangulares, en papel milimetrado, papel logarítmico y semilogaritmico. Aplicamos el método de mínimos cuadrados para poder convertir nuestra curva en rectas
Ejercicios de analisis de graficas

1. El decaimiento de isótopos radiativos en el tiempo sigue una relación exponencial negativa.
2. Se observan dos móviles cuyos movimientos siguen relaciones lineales y exponenciales respectivamente.
3. El volumen de un gas varía inversamente con la temperatura siguiendo una relación exponencial.
Más contenido relacionado
La actualidad más candente
Practica 1.-ley-de-boyle

La práctica demostró que el volumen de un gas varía inversamente con la presión cuando se mantiene constante la temperatura. Al aumentar la presión sobre un gas atrapado en una jeringa, su volumen disminuyó. La gráfica de presión vs volumen mostró una relación inversa, confirmando la Ley de Boyle.
Transiciones electronicas

El documento describe los tipos de transiciones electrónicas que pueden ocurrir en moléculas dependiendo de su estructura. Menciona que las transiciones σ→σ*, n→σ*, n→π* y π→π* son posibles, y que las energías requeridas para las transiciones n→π* y π→π* conducen a absorción en el rango de 200-700 nm. También explica que la presencia de grupos funcionales específicos ("cromóforos") es necesaria para proporcionar orbitales que permitan la absorción
Química2 bach 8.5 grado de disociación

El documento habla sobre el grado de disociación, definido como la fracción de moléculas disociadas en equilibrio. Explica que la relación entre la constante de equilibrio Kc y el grado de disociación α depende del proceso químico específico. Proporciona dos ejemplos de cálculos de Kc y α para reacciones de descomposición de N2O4 y NH3.
TERMOQUÍMICA

Este documento presenta los conceptos fundamentales de la termoquímica en 12 puntos. Introduce sistemas, estados y funciones de estado, así como el primer principio de la termodinámica. Explica las relaciones entre energía interna, entalpía, calor y trabajo, y cómo calcular las entalpías estándar de reacción y formación usando la ley de Hess.
2013 2 taller transf masa int

1) El documento presenta varios problemas relacionados con la transferencia de masa interfacial en operaciones unitarias. Incluye cálculos de coeficientes de transferencia de masa, flujos y porcentajes de resistencia en películas para absorción de gases en torres de paredes mojadas.
2) Presenta ejercicios adicionales sobre absorción de ácido clorhídrico en aire y CO2 en soda cáustica, así como difusión de gases a través de membranas y evaporación en torres. Se piden cálculos de
Mecanismos.de.reaccion.en.quimica.organica.(problemas.selectos.y.soluciones)....

Este documento describe los pasos para configurar una nueva cuenta de correo electrónico en Gmail. Explica cómo iniciar sesión en Gmail, completar la configuración del perfil y agregar una dirección de correo electrónico.
Cálculo de la entalpía

El documento calcula las entalpías estándar de formación del FeO(s) y Fe2O3(s) utilizando la ley de Hess. Para el FeO(s), invierte y suma las reacciones (2) y (3), luego invierte y suma (4), obteniendo una reacción de formación cuya entalpía es -63.72 kcal. Para el Fe2O3(s), invierte y multiplica (1) por 3, luego suma (3) también multiplicada por 3, obteniendo una reacción de formación cuya entalpía es -196.
Catalisis

Este documento trata sobre los conceptos básicos de la catálisis, incluyendo definiciones de catalizador, tipos de catalizadores (homogéneos y heterogéneos), propiedades de los catalizadores, mecanismos de reacción catalítica, y tipos de catálisis como la catálisis ácida, básica, enzimática y heterogénea. También discute conceptos como la energía de activación, ecuación de Arrhenius, y ejemplos de reacciones catalizadas como la descomposición del per
39368106 7-6-punto-triple-so2

Este documento presenta la resolución de varios ejercicios relacionados con el equilibrio de fases en sistemas simples utilizando la ecuación de Clapeyron. Se calculan propiedades como puntos de ebullición, entalpías y entropías de vaporización para diferentes sustancias como éter etílico, agua, sodio y yodo. También se estiman cambios en los puntos de fusión y ebullición del agua y benceno al variar la presión.
Joule thomson

El experimento de Joule-Thompson mide cómo la temperatura de un gas cambia cuando se expande adiabáticamente. Para la mayoría de los gases, la temperatura disminuye durante la expansión, lo que significa que tienen un coeficiente de Joule-Thompson positivo. La expansión adiabática se utiliza en aplicaciones como extintores de incendios, refrigeración y para explicar la formación de nubes. El coeficiente de Joule-Thompson ayuda a determinar cómo varía la entalpía de un gas con respecto a los cambios de presión.
Equilibrio fisico

Este documento describe un experimento sobre el equilibrio físico entre las fases líquida y gaseosa de sustancias. Los estudiantes prepararon soluciones acuosas de NaCl y sacarosa a diferentes concentraciones y midieron cómo cambiaba su temperatura de ebullición en comparación con el agua pura, para determinar el aumento ebulloscópico y la molalidad de cada solución. Los resultados mostraron que una mayor concentración de soluto requiere una temperatura más alta para que la solución hierva.
Estimación de coeficientes de transporte

Historia y ecuaciones utilizadas para estimar coeficientes de transporte o para "reajustar" los coeficientes a condiciones físicas distintas de las experimentadas.
Calculo de la conductividad termica liquido y gases

Experimento del alambre caliento de platino y método pa calcular la conductividad termica de gases y liquido
Calorimetria Presion Constante (1).pptx

Este documento describe los principios de la calorimetría a presión constante y presenta varios casos de estudio para calcular cantidades de calor involucradas en reacciones químicas como la fusión, disolución y neutralización. También calcula el calor de combustión del ácido benzoico usando una bomba calorimétrica.
Fisica antologia fenómenos de transporte

Este documento presenta conceptos básicos sobre fenómenos de transporte. Explica que un sistema termodinámico está caracterizado por variables como presión, volumen y temperatura. Describe los tres tipos de sistemas: aislados, cerrados y abiertos. También distingue entre sistemas homogéneos y heterogéneos. Presenta información sobre transferencia de cantidad de movimiento, clasificación de fluidos newtonianos y no newtonianos, y la ley de Newton de la viscosidad.
Determinacion de las cantidades molares parciales

Este documento describe tres métodos (directo, analítico y gráfico) para determinar las propiedades molares parciales de una mezcla de dos componentes. Explica que el método gráfico involucra trazar una curva de la propiedad extensiva frente al número de moles de un componente y calcular la pendiente a diferentes composiciones. También describe cómo el método analítico usa ecuaciones diferenciales de la propiedad y fracciones molares para calcular las propiedades molares parciales.
TRIÁNGULO DE GIBBS: ENFOQUE GENERAL A REPRESENTACIÓN DE SISTEMAS TERNARIOS.

TRIÁNGULO DE GIBBS: ENFOQUE GENERAL A REPRESENTACIÓN DE SISTEMAS TERNARIOS.Irvin de Jesús Rodríguez Martínez
Este PDF, es la versión de una presentación realizada para dar un enfoque general de los diagramas triangulares (Triángulo de Gibbs) para sistemas ternarios.respuestas-ejercicios-exsamen 2.pdf

Este documento contiene tres ejercicios de cálculo relacionados con intercambiadores de calor. El primero calcula el área requerida para enfriar aceite usando agua en un intercambiador tubular. El segundo calcula la velocidad de flujo de agua y el coeficiente de transferencia de calor para enfriar aceite en un intercambiador contracorriente. El tercero calcula la cantidad de calor transferida, la temperatura de salida del agua y el número de placas necesarias para enfriar aceite en un interc
Termoquimica

Este documento trata sobre la termoquímica y resume sus principales conceptos y leyes. Explica que la termoquímica estudia los cambios energéticos en las reacciones químicas mediante la aplicación de la primera ley de la termodinámica. Define conceptos como la entalpía de reacción, las reacciones exotérmicas y endotérmicas, y expone leyes como la ley de Hess sobre la constancia del calor de reacción.
Problemas y cuestiones olimpiadas de quimica

Este documento presenta una colección de problemas y cuestiones de las Olimpiadas de Química de España entre 1996 y 2011. Explica que el objetivo es ofrecer material de apoyo para la enseñanza de la Química en bachillerato y primeros cursos universitarios. Además, incluye las soluciones a los problemas y cuestiones propuestos.
La actualidad más candente (20)
Mecanismos.de.reaccion.en.quimica.organica.(problemas.selectos.y.soluciones)....

Mecanismos.de.reaccion.en.quimica.organica.(problemas.selectos.y.soluciones)....
Calculo de la conductividad termica liquido y gases

Calculo de la conductividad termica liquido y gases
TRIÁNGULO DE GIBBS: ENFOQUE GENERAL A REPRESENTACIÓN DE SISTEMAS TERNARIOS.

TRIÁNGULO DE GIBBS: ENFOQUE GENERAL A REPRESENTACIÓN DE SISTEMAS TERNARIOS.
Similar a Determinación de Entropía por método de conteo y pesada
datos experimentales

laboratorio graficamos un conjunto de datos experimentales en el sistema de coordenadas cartesianas rectangulares, en papel milimetrado, papel logarítmico y semilogaritmico. Aplicamos el método de mínimos cuadrados para poder convertir nuestra curva en rectas
Ejercicios de analisis de graficas

1. El decaimiento de isótopos radiativos en el tiempo sigue una relación exponencial negativa.
2. Se observan dos móviles cuyos movimientos siguen relaciones lineales y exponenciales respectivamente.
3. El volumen de un gas varía inversamente con la temperatura siguiendo una relación exponencial.
359757087 viscosidad-cinematica-de-aire-y-agua-pdf

Este documento contiene 5 tablas que proporcionan información sobre prefijos, propiedades físicas del aire y líquidos comunes, propiedades físicas del agua, la tabla periódica de elementos y una tabla sintética de unidades. La información incluye factores de prefijos, densidades, viscosidades, módulos de elasticidad, tensiones superficiales y presiones de vapor para diferentes temperaturas.
Tablas graficos

Este documento contiene 5 tablas que proporcionan información sobre prefijos, propiedades físicas del aire y líquidos comunes, propiedades físicas del agua, la tabla periódica de elementos y una tabla sintética de unidades. La información incluye factores de prefijos, densidades, viscosidades, módulos de elasticidad, tensiones superficiales y presiones de vapor para diferentes temperaturas.
Memoria de practicas física uned 2011

Este documento presenta la metodología para dos prácticas de física sobre la determinación de la aceleración de la gravedad mediante un péndulo simple y la constante elástica de un muelle. En la primera práctica, los estudiantes medirán el período de oscilación de un péndulo para diferentes longitudes y usarán esos datos para calcular g. En la segunda práctica, determinarán la constante elástica de un muelle usando métodos estático y dinámico, midiendo el alargamiento bajo diferentes cargas
Ejercicio de Sedimentación 

Se llevó a cabo una prueba de sedimentación por lotes con una suspensión de cal. La interfase entre el líquido y los sólidos en suspensión en función del tiempo se muestran en la siguiente tabla. La prueba utilizada es de 236 g de cal por litro de suspensión. Determinar:
a) Un perfil de velocidad versus concentración de sólidos.
b) El área mínima si la alimentación es de 50 ton / h de sólidos secos y una suspensión de 600 g / L es producido
c) Profundidad del espesante (ρS = 2090 Kg / m3).
practica de perdidas menores

El documento describe tres experimentos realizados para determinar las longitudes equivalentes en metros y diámetros de diferentes accesorios de tuberías. Se midieron las pérdidas de carga en tres trayectorias con diferentes configuraciones de tuberías y accesorios. Luego, se calculó la longitud equivalente de cada configuración y se compararon los resultados con valores bibliográficos.
1 mer examen

Este documento presenta la solución a dos preguntas relacionadas con el análisis de datos de precipitación. La primera pregunta involucra completar registros mensuales de precipitación faltantes utilizando información histórica y evaluar la homogeneidad de los datos. La segunda pregunta trata sobre el cálculo de precipitaciones máximas en 24 horas para diferentes periodos de retorno y la construcción de curvas de intensidad-duración-frecuencia.
Conversión de unidades

Este documento explica cómo convertir unidades de medida de diferentes cantidades físicas como longitud, masa, volumen, temperatura, entre otras. Describe los factores de conversión que se usan para expresar cantidades medidas en unidades diferentes y proporciona ejemplos numéricos de conversiones entre unidades como centímetros a metros, gramos a kilogramos, y grados Celsius a grados Fahrenheit. Finalmente, incluye tablas de equivalencia de unidades para diferentes magnitudes físicas.
Trabajo dinamica logistico

Este documento presenta los resultados de 4 modelos del juego frijolero con diferentes condiciones iniciales de número de individuos (N1=100, N2=200, N3=300, N4=400). En cada modelo se muestra la evolución de la población (Nt) a lo largo del tiempo, así como los parámetros K, r, a y b. Las gráficas muestran oscilaciones de Nt cercanas a K, indicando que la población se estabiliza cerca de su capacidad de carga. Los valores de K y r varían entre modelos,
Metodo dinamico plano 3 2011

Este documento presenta los pasos para calcular las fuerzas sísmicas en un edificio de 8 niveles utilizando el método dinámico con un grado de libertad por planta de acuerdo a la norma sismorresistente COVENIN 1756-2001. Se obtienen los datos modales del edificio y se aplican los parámetros de la norma para determinar los factores de participación modal y los espectros de diseño. Luego se calculan las fuerzas laterales y cortantes en cada modo y se comprueba que el cortante basal acumulado
Metodo dinamico plano 3 2011

Este documento presenta los pasos para calcular las fuerzas sísmicas en un edificio de 8 niveles utilizando el método dinámico con un grado de libertad por planta de acuerdo a la norma sismorresistente COVENIN 1756-2001. Se obtienen los datos modales del edificio y se aplican los parámetros de la norma para determinar los factores de participación modal y los espectros de diseño. Luego se calculan las fuerzas laterales y cortantes en cada modo y se comprueba que el cortante basal acumulado
Informe final topografia 2

Este informe presenta los resultados de un levantamiento topográfico realizado mediante el método de trilateración. Se midieron ángulos y distancias entre puntos de referencia para calcular las coordenadas de cada punto. Luego de corregir errores, se generó una poligonal y se calcularon las coordenadas de todos los puntos. Finalmente, se creó un plano topográfico del área mediante software.
Informe de-consolidacion

Este informe presenta los resultados de una prueba de consolidación de una muestra de suelo. La prueba determinó el índice de compresión (Cc) de 0,283 y el índice de expansión (Cs) de 0,0465. También se midieron las deformaciones de la muestra bajo diferentes cargas de 20kg a 320kg y se graficaron las curvas de consolidación.
Presentacion Caceres de obras hidraulicas.pptx

El documento presenta el proyecto de una presa de gravedad. Los objetivos del proyecto son ubicar la presa de manera técnica y económica, dimensionar el embalse mediante los métodos RIPL y de simulación, y diseñar el cuerpo de la presa. Se realizan cálculos topográficos, de volumen del embalse, evaporación y sedimentos para determinar las dimensiones de la presa, con un volumen útil de 3.15 millones de metros cúbicos y un volumen total de 33.85 millones de metros c
Corte directo

Este documento describe el procedimiento para realizar una prueba de corte directo en una muestra de suelo para determinar su resistencia al corte y ángulo de fricción interno. Se somete la muestra a diferentes cargas normales mientras se mide la fuerza de cizalladura y deformación. Los resultados incluyen gráficas de esfuerzo cortante contra deformación y esfuerzo normal contra esfuerzo cortante máximo para cada carga.
Analisis granulometrico por sedimentacion

Este documento presenta el procedimiento para realizar un análisis granulométrico por sedimentación de suelos utilizando un hidrómetro. El método implica mezclar una muestra de suelo con un agente dispersivo, agitar la mezcla y tomar lecturas del hidrómetro en diferentes tiempos para determinar el porcentaje de partículas que permanecen en suspensión y así estimar la distribución de tamaños de partícula en la muestra. El procedimiento incluye correcciones por temperatura, gravedad específica y otros factores para obt
Separata iii integración numerica terry

Este documento presenta la regla de Simpson para la integración numérica y su aplicación en diferentes casos. Explica cómo usar la regla para integrar funciones, funciones entre límites diferentes y datos experimentales. También presenta ejemplos de integración de funciones y cálculo del volumen de un cilindro y masa de efluentes vertidos. Finaliza con problemas propuestos para integrar funciones usando la regla de Simpson.
Curvas de remanso-tramo fijos

El documento presenta 8 problemas resueltos sobre flujo gradualmente variado y el método de tramos fijos. El Problema 1 calcula la altura de remanso a 500 m aguas arriba de una sección dada. El Problema 2 calcula la longitud requerida para revestir una rápida en un canal. El Problema 3 analiza el flujo a través de una compuerta en un canal rectangular.
Cambio de unidades

Este documento trata sobre cambios de unidades y escalas de unidades. Explica las escalas de unidades lineales, cuadráticas y cúbicas, así como las conversiones entre unidades de longitud, masa, volumen, superficie y otras cantidades físicas usando factores de conversión. También incluye ejemplos numéricos de cómo realizar dichas conversiones.
Similar a Determinación de Entropía por método de conteo y pesada (20)
359757087 viscosidad-cinematica-de-aire-y-agua-pdf

359757087 viscosidad-cinematica-de-aire-y-agua-pdf
Más de Fabián Andrés Cruz González
Experimento de pendulo simple

Este documento presenta el informe de un experimento para medir la gravedad usando un péndulo simple. Se midió el período del péndulo variando la longitud del hilo y el ángulo de inicio de las oscilaciones. Los datos se usaron para calcular la gravedad indirectamente y comparar con valores oficiales. Los resultados encontraron que la gravedad medida fue de 996,93 cm/s2 para un ángulo de 30° y 977,19 cm/s2 para 20°, con errores de ±2% y ±0,02% respectivamente en comparación con
Hidroxiprolina en productos cárnicos y sus derivados

Este documento describe un método colorimétrico para determinar la hidroxiprolina en carnes y productos cárnicos. La muestra se hidroliza en ácido sulfúrico para liberar la hidroxiprolina. Luego se oxida y se desarrolla un color rojo-morado que se mide fotométricamente. Se prepara una curva de calibración con patrones de hidroxiprolina y se usa para calcular la cantidad en la muestra. La hidroxiprolina se usa para estimar el contenido de tejido conect
Isolation of Artemisinin (Qinghaosu) from Artemisia Annua Growing in the Unit...

Isolation of Artemisinin (Qinghaosu) from Artemisia Annua Growing in the Unit...Fabián Andrés Cruz González
Traducción al Español del articulo "Isolation of Artemisinin (Qinghaosu) from Artemisia Annua Growing in the United States", de los siguientes autores; Daniel l. Klayman,* Aij. Lin. Nancy Acton, John P. Scovill, James m. Hoch, Wilbur k. Milhous, Anthony D. Theoharide and Arthur S. Dobek
If It's Resonance, What is Resonating? - Si Es Resonancia, ¿Qué Está Resonando?

If It's Resonance, What is Resonating? - Si Es Resonancia, ¿Qué Está Resonando?Fabián Andrés Cruz González
Traducción al español del artículo "If It’s Resonance, What Is Resonating?" del profesor Robert C. Kerber.Termogravimetría

Es una presentación sobre la termogravimetría TG y este mismo método acoplado a otras técnicas para tener máxima eficiencia de resultados
CARACTERIZACIÓN DE ACELGA FRESCA DE SANTIAGO DEL ESTERO (ARGENTINA). COMPARAC...

CARACTERIZACIÓN DE ACELGA FRESCA DE SANTIAGO DEL ESTERO (ARGENTINA). COMPARAC...Fabián Andrés Cruz González
El documento presenta los resultados de un estudio de caracterización integral de la acelga (Beta vulgaris, var. cycla) cultivada en la provincia de Santiago del Estero, Argentina. Se analizaron y compararon la hoja y el tallo con respecto a su contenido de nutrientes, minerales, proteínas, fibra y carotenoides. Se encontraron diferencias significativas entre la hoja y el tallo en estos componentes. Específicamente, la hoja contenía mayores niveles de carotenoides, lo que indica un mayor valor provitamínico A.Medición de la entropía

Este documento describe diferentes métodos para medir la entropía de una sustancia. La tercera ley de la termodinámica establece que la entropía de una sustancia perfectamente cristalina es cero a 0 K. Se pueden medir las capacidades caloríficas a diferentes temperaturas y extrapolar los datos a bajas temperaturas usando la aproximación de Debye. La entropía se puede calcular mediante la integración numérica de los datos experimentales usando la definición de la integral definida. Como ejemplo, se muestra el cálculo
Más de Fabián Andrés Cruz González (7)
Hidroxiprolina en productos cárnicos y sus derivados

Hidroxiprolina en productos cárnicos y sus derivados
Isolation of Artemisinin (Qinghaosu) from Artemisia Annua Growing in the Unit...

Isolation of Artemisinin (Qinghaosu) from Artemisia Annua Growing in the Unit...
If It's Resonance, What is Resonating? - Si Es Resonancia, ¿Qué Está Resonando?

If It's Resonance, What is Resonating? - Si Es Resonancia, ¿Qué Está Resonando?
CARACTERIZACIÓN DE ACELGA FRESCA DE SANTIAGO DEL ESTERO (ARGENTINA). COMPARAC...

CARACTERIZACIÓN DE ACELGA FRESCA DE SANTIAGO DEL ESTERO (ARGENTINA). COMPARAC...
Último
DESARROLLO DE LAS RELACIONES CON LOS STAKEHOLDERS.pdf

DESARROLLO DE LAS RELACIONES CON LOS STAKEHOLDERS
CALCULO DE AMORTIZACION DE UN PRESTAMO.pdf

Se ha realizado este trabajo con la finalidad de explicar como se realiza el cálculo de la amortización de un préstamo descrita en una serie de pasos.
MATERIAL ESCOLAR 2024-2025 3 AÑOS CEIP SAN CRISTÓBAL

MATERIAL ESCOLAR 2024-2025 3 AÑOS CEIP SAN CRISTÓBAL
Gracias papá voz mujer_letra y acordes de guitarra.pdf

Puedes encontrar el video y el archivo para descargar en mi blog:
https://labitacoradeann.blogspot.com/2024/06/gracias-papa.html
Business Plan -rAIces - Agro Business Tech

Innovación y transparencia se unen en un nuevo modelo de negocio para transformar la economia popular agraria en una agroindustria. Facilitamos el acceso a recursos crediticios, mejoramos la calidad de los productos y cultivamos un futuro agrícola eficiente y sostenible con tecnología inteligente.
ANALISIS CRITICO DEL PENSAMIENTO COLONIAL Y DESCOLONIZACION

ES UN ANALISIS DE LA REALIDAD BOLIVIANA EN LA ETAPA DE DESCOLONIZACION DE BOLIVIA, QUE SE DA MEDIANTE INSURGENCIAS INDIGENAS HASTA EL SIGLO XXI
La necesidad de bienestar y el uso de la naturaleza.pdf

La necesidad de bienestar y el uso de la naturaleza
Papel histórico de los niños, jóvenes y adultos mayores en la historia nacional

es un cuestionario sbre el Papel histórico de los niños, jóvenes y adultos mayores en la historia nacional
La filosofía presocrática y los filosofos más relvantes del periodo.

clase de la filosofía presocrática.
Gracias papá hombre_letra y acordes de guitarra.pdf

Puedes encontrar el video y el archivo para descargar en mi blog:
https://labitacoradeann.blogspot.com/2024/06/gracias-papa.html
Mapa Mental documentos que rigen el sistema de evaluación

APORTES DE LOS DOCUMENTOS QUE RIGEN EL SISTEMA DE EVALUACIÓN.
Último (20)
DESARROLLO DE LAS RELACIONES CON LOS STAKEHOLDERS.pdf

DESARROLLO DE LAS RELACIONES CON LOS STAKEHOLDERS.pdf
Presentación de proyecto en acuarela moderna verde.pdf

Presentación de proyecto en acuarela moderna verde.pdf
MATERIAL ESCOLAR 2024-2025 3 AÑOS CEIP SAN CRISTÓBAL

MATERIAL ESCOLAR 2024-2025 3 AÑOS CEIP SAN CRISTÓBAL
Gracias papá voz mujer_letra y acordes de guitarra.pdf

Gracias papá voz mujer_letra y acordes de guitarra.pdf
ANALISIS CRITICO DEL PENSAMIENTO COLONIAL Y DESCOLONIZACION

ANALISIS CRITICO DEL PENSAMIENTO COLONIAL Y DESCOLONIZACION
La necesidad de bienestar y el uso de la naturaleza.pdf

La necesidad de bienestar y el uso de la naturaleza.pdf
Papel histórico de los niños, jóvenes y adultos mayores en la historia nacional

Papel histórico de los niños, jóvenes y adultos mayores en la historia nacional
La filosofía presocrática y los filosofos más relvantes del periodo.

La filosofía presocrática y los filosofos más relvantes del periodo.
2024 planificacion microcurricular 7mo A matutino..docx

2024 planificacion microcurricular 7mo A matutino..docx
Gracias papá hombre_letra y acordes de guitarra.pdf

Gracias papá hombre_letra y acordes de guitarra.pdf
Mapa Mental documentos que rigen el sistema de evaluación

Mapa Mental documentos que rigen el sistema de evaluación
Determinación de Entropía por método de conteo y pesada
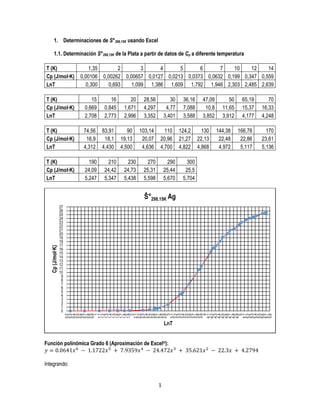
- 1. 1 1. Determinaciones de S°298,15K usando Excel 1.1. Determinación S°298,15K de la Plata a partir de datos de Cp a diferente temperatura T (K) 1,35 2 3 4 5 6 7 10 12 14 Cp (J/mol∙K) 0,00106 0,00262 0,00657 0,0127 0,0213 0,0373 0,0632 0,199 0,347 0,559 LnT 0,300 0,693 1,099 1,386 1,609 1,792 1,946 2,303 2,485 2,639 T (K) 15 16 20 28,56 30 36,16 47,09 50 65,19 70 Cp (J/mol∙K) 0,669 0,845 1,671 4,297 4,77 7,088 10,8 11,65 15,37 16,33 LnT 2,708 2,773 2,996 3,352 3,401 3,588 3,852 3,912 4,177 4,248 T (K) 74,56 83,91 90 103,14 110 124,2 130 144,38 166,78 170 Cp (J/mol∙K) 16,9 18,1 19,13 20,07 20,96 21,27 22,13 22,48 22,86 23,61 LnT 4,312 4,430 4,500 4,636 4,700 4,822 4,868 4,972 5,117 5,136 T (K) 190 210 230 270 290 300 Cp (J/mol∙K) 24,09 24,42 24,73 25,31 25,44 25,5 LnT 5,247 5,347 5,438 5,598 5,670 5,704 Función polinómica Grado 6 (Aproximación de Excel®): 𝑦 = 0.0641𝑥6 − 1.1722𝑥5 + 7.9359𝑥4 − 24.472𝑥3 + 35.621𝑥2 − 22.3𝑥 + 4.2794 Integrando: 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1 1,1 1,2 1,3 1,4 1,5 1,6 1,7 1,8 1,9 2 2,1 2,2 2,3 2,4 2,5 2,6 2,7 2,8 2,9 3 3,1 3,2 3,3 3,4 3,5 3,6 3,7 3,8 3,9 4 4,1 4,2 4,3 4,4 4,5 4,6 4,7 4,8 4,9 5 5,1 5,2 5,3 5,4 5,5 5,6 5,7 5,8 Cp(J/mol∙K) LnT Ŝ°298,15K Ag
- 2. 2 ∫ 0.0641𝑥6 − 1.1722𝑥5 + 7.9359𝑥4 − 24.472𝑥3 + 35.621𝑥2 − 22.3𝑥 + 4.2794 5.698 0.300 𝑑𝑥 = 41.96 𝐸𝑟𝑟𝑜𝑟 𝑎𝑏𝑠𝑜𝑙𝑢𝑡𝑜 = |41.96 − 42.55| = 0.590 𝐸𝑟𝑟𝑜𝑟 𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = (| 41.96 − 42.55 42.55 |) = 0.01387 %𝐸𝑟𝑟𝑜𝑟 𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = (| 41.96 − 42.55 42.55 |) ∗ 100 = 1.387% 1.2. Determinación S°298,15K del Cobre a partir de datos de Cp a diferente temperatura Cp (J/mol∙K) 0,056 0,094 0,149 0,225 0,328 0,462 0,963 1,690 2,640 3,740 T (K) 10 12 14 16 18 20 25 30 35 40 LnT 2,303 2,485 2,639 2,773 2,890 2,996 3,219 3,401 3,555 3,689 Cp (J/mol∙K) 6,150 8,600 10,86 12,85 14,56 16,01 18,25 19,87 21,05 21,94 T (K) 50 60 70 80 90 100 120 140 160 180 LnT 3,912 4,094 4,248 4,382 4,500 4,605 4,787 4,942 5,075 5,193 Cp (J/mol∙K) 22,63 23,17 23,60 23,94 24,22 24,45 T (K) 200 220 240 260 280 300 LnT 5,298 5,394 5,481 5,561 5,635 5,704 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 2,2 2,3 2,4 2,5 2,6 2,7 2,8 2,9 3 3,1 3,2 3,3 3,4 3,5 3,6 3,7 3,8 3,9 4 4,1 4,2 4,3 4,4 4,5 4,6 4,7 4,8 4,9 5 5,1 5,2 5,3 5,4 5,5 5,6 5,7 5,8 5,9 Cp(J/mol∙K) LnT Ŝ°298,15K Cu
- 3. 3 Función polinómica Grado 6 (Aproximación de Excel®): 𝑦 = 0.2045𝑥6 − 4.4231𝑥5 + 37.851𝑥4 − 163.08𝑥3 + 373.12𝑥2 − 429.11𝑥 + 192.46 Integrando: ∫ 0.2045𝑥6 − 4.4231𝑥5 + 37.851𝑥4 − 163.08𝑥3 + 373.12𝑥2 − 429.11𝑥 + 192.46 5.698 2.303 𝑑𝑥 = 31.892 𝐸𝑟𝑟𝑜𝑟 𝑎𝑏𝑠𝑜𝑙𝑢𝑡𝑜 = 33.15 − 31.892 = 1.258 𝐸𝑟𝑟𝑜𝑟 𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = ( 33.15 − 31.892 33.15 ) = 0.03795 %𝐸𝑟𝑟𝑜𝑟 𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = ( 33.15 − 31.892 33.15 ) ∗ 100 = 3.795% 2. Determinaciones de S°298.15K por método de pesada 2.1. Determinación de S°298.15K de Plata por método de pesada Ilustración 1. Gráfico en papel milimetrado - Plata
- 4. 4 Peso del gráfico: 515mg Peso del área conocida (0.7 unidades de área): 8mg Á𝑟𝑒𝑎 𝑏𝑎𝑗𝑜 𝑙𝑎 𝑐𝑢𝑟𝑣𝑎 = (515𝑚𝑔 ∗ 0.7 𝑢. 𝑎 8𝑚𝑔 ) = 45.06 𝑢. 𝑎 𝐸𝑟𝑟𝑜𝑟 𝑎𝑏𝑠𝑜𝑙𝑢𝑡𝑜 = 45.06 − 42.55 = 2.51 𝐸𝑟𝑟𝑜𝑟 𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = 45.06 − 42.55 42.55 = 0.0589 𝑃𝑜𝑟𝑐𝑒𝑛𝑡𝑎𝑗𝑒 𝐸𝑟𝑟𝑜𝑟 𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = ( 45.06 − 42.55 42.55 ) ∗ 100% = 5.899% 𝑃𝑜𝑟𝑐𝑒𝑛𝑡𝑎𝑗𝑒 𝐸𝑥𝑎𝑐𝑡𝑖𝑡𝑢𝑑 = ( 45.06 ∗ 100% 42.55 ) = 105.89% 2.2. Determinación de S°298.15K de Cobre por método de pesada Ilustración 2. Gráfico en papel milimetrado - Cobre Peso del gráfico: 416mg Peso del área conocida (0.925 unidades de área): 11mg
- 5. 5 Á𝑟𝑒𝑎 𝑏𝑎𝑗𝑜 𝑙𝑎 𝑐𝑢𝑟𝑣𝑎 = (416𝑚𝑔 ∗ 0.925 𝑢. 𝑎 11𝑚𝑔 ) = 34.98 𝑢. 𝑎 𝐸𝑟𝑟𝑜𝑟 𝑎𝑏𝑠𝑜𝑙𝑢𝑡𝑜 = 34.98 − 33.15 = 1.83 𝐸𝑟𝑟𝑜𝑟 𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = 34.98 − 33.15 33.15 = 0.0552 𝑃𝑜𝑟𝑐𝑒𝑛𝑡𝑎𝑗𝑒 𝐸𝑟𝑟𝑜𝑟 𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = ( 34.98 − 33.15 33.15 ) ∗ 100% = 5.520% 𝑃𝑜𝑟𝑐𝑒𝑛𝑡𝑎𝑗𝑒 𝐸𝑥𝑎𝑐𝑡𝑖𝑡𝑢𝑑 = ( 34.98 ∗ 100% 33.15 ) = 105.52% 3. Determinaciones de S°298.15K por método de Conteo 3.1. Determinación de S°298.15K de Cobre por conteo de unidades de área (Ver anexo) Unidad de área (área de cuadrado del papel milimetrado): 0.1 u.a Conteo total: 32.48 u.a 𝐸𝑟𝑟𝑜𝑟 𝑎𝑏𝑠𝑜𝑙𝑢𝑡𝑜 = 33.15 − 33.06 = 0.09 𝐸𝑟𝑟𝑜𝑟 𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = 33.15 − 33.06 33.15 = 0.002714 𝑃𝑜𝑟𝑐𝑒𝑛𝑡𝑎𝑗𝑒 𝐸𝑟𝑟𝑜𝑟 𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = ( 33.15 − 33.06 33.15 ) ∗ 100% = 0.2714% 𝑃𝑜𝑟𝑐𝑒𝑛𝑡𝑎𝑗𝑒 𝐸𝑥𝑎𝑐𝑡𝑖𝑡𝑢𝑑 = ( 33.06 ∗ 100% 33.15 ) = 99.72% 3.2. Determinación de S°298.15K de Plata por conteo de unidades de área (Ver anexo) Unidad de área (área de cuadrado del papel milimetrado): 0.1 u.a Conteo total: 45.08 u.a 𝐸𝑟𝑟𝑜𝑟 𝑎𝑏𝑠𝑜𝑙𝑢𝑡𝑜 = 42.70 − 42.55 = 0.15 𝐸𝑟𝑟𝑜𝑟 𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = 42.70 − 42.55 42.55 = 0.003525 𝑃𝑜𝑟𝑐𝑒𝑛𝑡𝑎𝑗𝑒 𝐸𝑟𝑟𝑜𝑟 𝑟𝑒𝑙𝑎𝑡𝑖𝑣𝑜 = ( 42.70 − 42.55 42.55 ) ∗ 100% = 0.3525% 𝑃𝑜𝑟𝑐𝑒𝑛𝑡𝑎𝑗𝑒 𝐸𝑥𝑎𝑐𝑡𝑖𝑡𝑢𝑑 = ( 42.70 ∗ 100% 42.55 ) = 100.35%
- 6. 6 Ilustración 3. Gráfico en papel milimetrado; Conteo – Cobre
- 7. 7 Ilustración 4. Gráfico en papel milimetrado; Conteo – Plata
- 8. 8 4. Descripción de métodos 4.1. Método de pesada Se dibuja la línea de tendencia, según los datos de las tablas, en papel milimetrado Se recorta el área gajo la curva en el papel milimetrado Se pesa el área bajo la curva Se determina el área de un segmento del área bajo la curva Se recorta dicho segmento Se pesa el segmento Se hace un factor de conversión para calcular el área total bajo la curva 4.2. Método de conteo Se dibuja la línea de tendencia, según los datos de las tablas, en papel milimetrado Se establece una base para los rectángulos Se delimita la altura de cada rectángulo cuando se intersecta con la línea de tendencia del gráfico Después de hacer los rectángulos, de se puede observar que resultan unos triángulos que colindan con la línea de tendencia del gráfico. Se procede a calcular el área de cada figura. Se hace usa sumatoria de las áreas para calcular el área bajo la curva. 4.3. Método de tendencia polinómica usando Excel® Se hace una tabla con datos de Cp(J/mol∙K) y LnT Se hace un gráfico de dispersión de estos datos Se selecciona tendencia polinómica, en “opciones de línea de tendencia”, en orden 6 Se selecciona la opción “presentar ecuación del gráfico” Se integra la función que aparece entre LnT “mínimo” y “máximo”, usando otro programa como WolframAlpha™.
