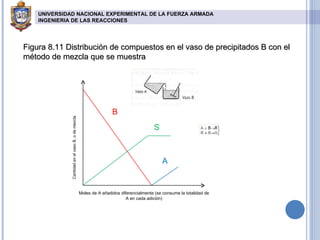
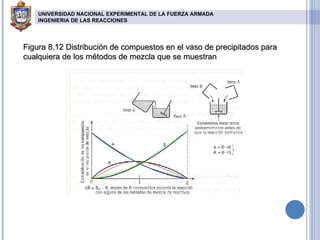
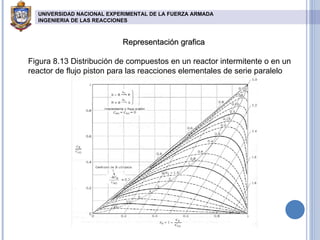
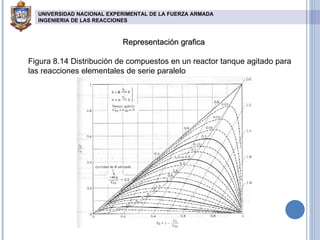
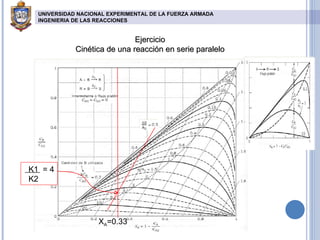
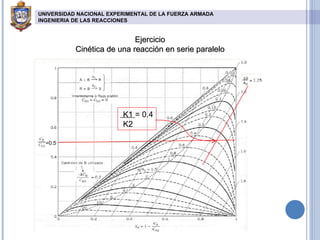
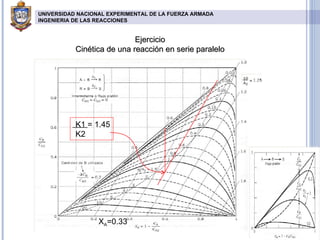
El documento describe reacciones químicas en serie y paralelo. Explica cómo analizar la distribución de productos en este tipo de reacciones y presenta ecuaciones para calcular concentraciones máximas de intermedios y productos finales en reactores de flujo pistón y tanque agitado. También incluye gráficos de la distribución de compuestos y resuelve ejercicios cinéticos para determinar constantes de velocidad de reacciones múltiples.