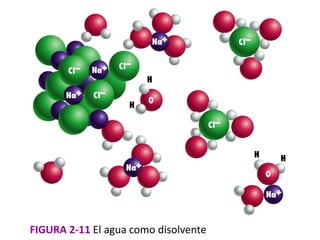
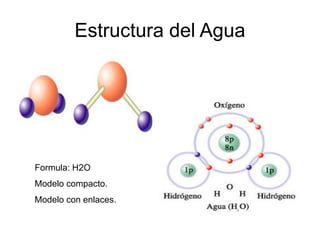
El documento proporciona información sobre las propiedades del agua. Explica que el agua está formada por moléculas de H2O y es esencial para la vida. Sus propiedades físicas como la tensión superficial, calor específico y capacidad de moderar la temperatura la hacen ideal para soportar la vida. También describe las propiedades químicas del agua como su pH, reacciones y dureza. En general, el documento ofrece una introducción a las características fundamentales del agua y por qué es tan importante para los sist











































![• Se denomina dureza del agua a la concentración de
compuestos minerales que hay en una determinada
cantidad de agua.
• Se calcula, genéricamente, a partir de la suma de las
concentraciones de calcio y magnesio existentes
(miligramos) por cada litro de agua; que puede ser
expresado en concentraciones de CaCO3.
• Los coeficientes se obtienen de las proporciones entre
el peso molecular del CaCO3 y los pesos moleculares
respectivos: 100/40 (para el Ca++); y 100/24 (para el
[Mg++]).
DUREZA](https://image.slidesharecdn.com/2-160625030356/85/EL-AGUA-49-320.jpg)