Incrustar presentación
Descargado 12 veces

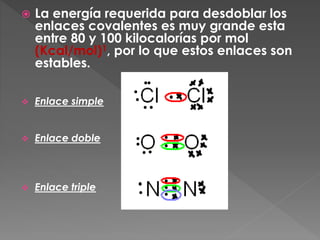




Los enlaces covalentes requieren gran energía para romperse y son estables. La fuerza de un enlace depende del número de cargas positivas en el núcleo atómico y la distancia entre el núcleo y los electrones externos. Las moléculas polares contienen átomos electronegativos como O, N, S o P y sus enlaces polares afectan la reactividad molecular.




