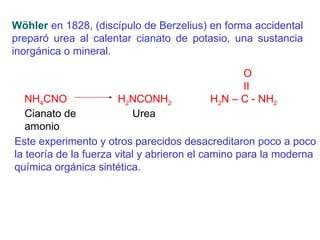
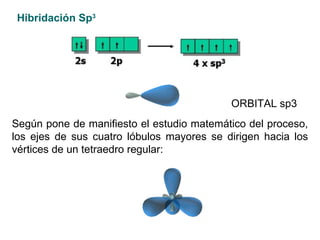
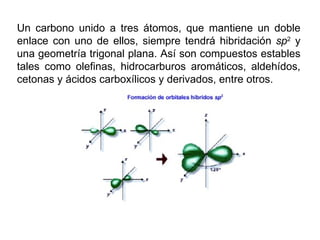
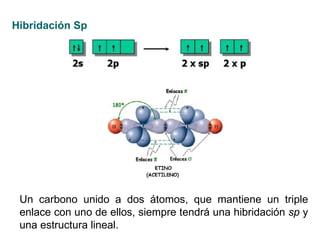
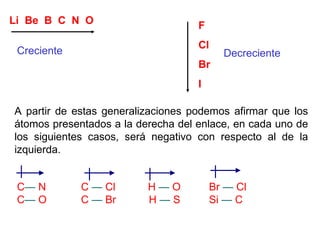
Este documento trata sobre química orgánica. Explica que la química orgánica estudia los compuestos de carbono encontrados en organismos vivos, mientras que la química inorgánica estudia otros compuestos. También describe los experimentos de Wöhler en 1828 que demostraron que los compuestos orgánicos pueden sintetizarse en el laboratorio, desacreditando la teoría de la "fuerza vital". Además, explica conceptos como la hibridación del carbono, los diferentes tipos de enlaces qu