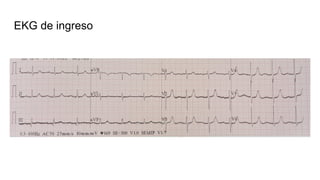
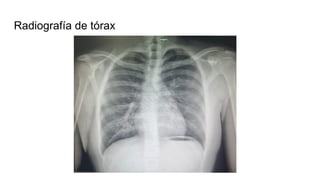
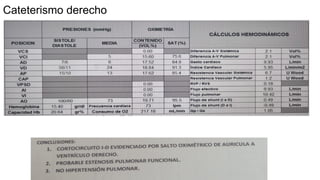
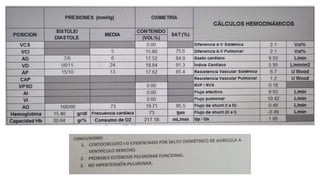
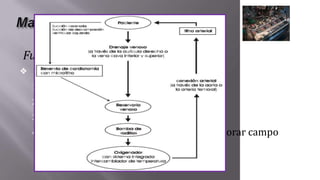
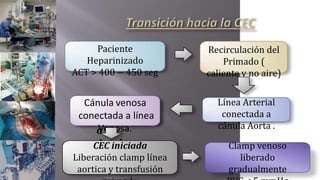
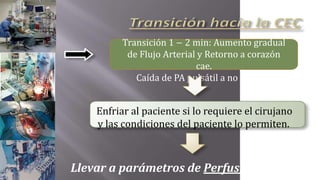
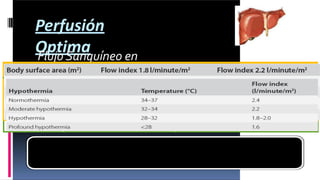
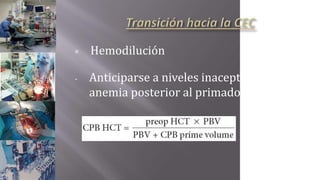
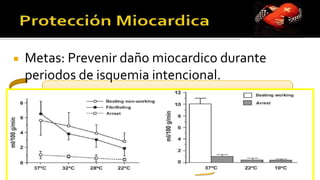
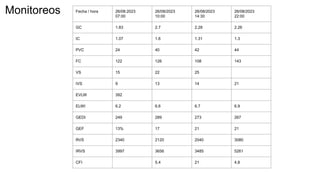
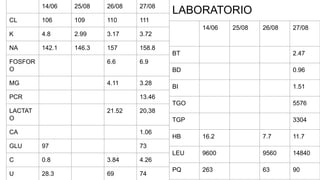
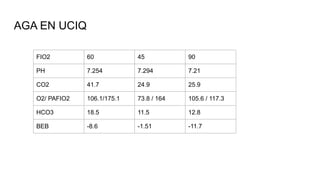
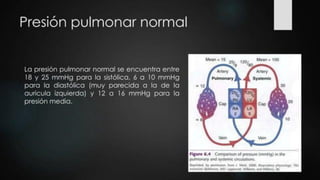
Este documento presenta el caso clínico de un paciente de 22 años con comunicación interventricular desde el nacimiento. El paciente experimentó episodios de dolor torácico y cianosis que mejoraron con el reposo. Los exámenes mostraron una comunicación interventricular de 11 mm. El paciente fue sometido a una hemicorrección del defecto septal ventricular y colocación de un conducto de descarga, pero falleció después de la cirugía.