FASES CICATRIZACION.................pptx
- 2. Como lo señaló John Hunter (1728-1793), un observador perspicaz de fenómenos biológicos “…la lesión tiene en todos los casos una tendencia a producir la disposición y los medios para su curación sola ”. Por definición, una herida altera la integridad tisular y tiene como resultado el corte de vasos sanguíneos y la exposición directa de la matriz extracelular a las plaquetas. La cicatrización normal de una herida sigue un patrón predecible que puede dividirse en fases superpuestas definidas por las poblaciones celulares y las actividades bioquímicas:
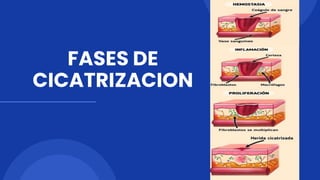
- 3. HEMOSTASIA Fase de hemostasia: inmediato (segundos, minutos) a la lesión. Al ocurrir un episodio lesivo, éste destruye, además de epitelio y matriz extracelular, capilares y vasos sanguíneos. ● Vasoconstricción; ésta sucede en microsegundos como un reflejo a la lesión. Al dañarse la pared vascular, deja expuesta la membrana basal que sostiene a las células endoteliales y da lugar a la activación del factor de la coagulación (XII) y el inicio de la cascada de la coagulación por su vía intrínseca para posibilitar la hemostasia en el vaso dañado. ● Coágulo de fibrina
- 6. Reacción vascular: caracterizada por una vasodilatación que permite un aumento del flujo sanguíneo hacia la zona dañada y con ello elevación de la presión hidrostática intravascular. En seguida ocurren cambios estructurales de las células endoteliales que le permiten contraerse en su mismo sitio y llenar el defecto ocasionado por la lesión tisular. La traducción clínica de este paso es la rubefacción y el edema o hinchazón. Reacción celular. FASE DE INFLAMACION
- 8. Reacción vascular Reacción celular: Sucede la extravasación de leucocitos hacia la zona dañada, junto con fibrina y otras proteínas. Así se obtiene la formación de la costra. Y a su vez la función microbicida de los leucocitos en esta fase es primordial para mantenerla estéril y facilitar la progresión de la reparación. NEUTROFILOS MACROFAGOS FASE DE INFLAMACION
- 10. Después de 48 h lesión, los macrófagos se desplazan a la zona para coordinar los procesos de re-epitelización y angiogénesis mediante la secreción de factores de crecimiento epidérmico (EGF) y vascular endotelial(VEGF). FASE DE PRODUCCIÓN DE TEJIDO DE GRANULACIÓN Y RE- EPITELIZACIÓN
- 11. Para el final del tercer día, los macrófagos han reemplazado en mayor parte a los neutrófilos y las fibras de colágeno comienzan a depositarse, aunque en escasa cantidad y paralelas al borde de la herida sin formar puentes. FASE DE PRODUCCIÓN DE TEJIDO DE GRANULACIÓN Y RE- EPITELIZACIÓN
- 12. FASE DE PRODUCCIÓN DE TEJIDO DE GRANULACIÓN Y RE- EPITELIZACIÓN Dia 5 a 7 Tejido de granulación abundante. Fibras de colágeno orientadas perpendicular a la herida con la formación de puentes. 10% de la fuerza original en este momento.
- 13. Al final de la primera semana y principio de la segunda, el proceso de blanqueamiento o empalidecimiento de la herida comienza a hacerse notorio, lo cual se debe a la producción progresiva de fibras de colágeno. Hay disminución de la densidad de los vasos sanguíneos. En este punto se recupera hasta 70% de la fuerza tensional de la herida.
- 14. FASE DE CONTRACCIÓN DE LA HERIDA Y REMODELADO. Después del primer mes inicia el proceso de contracción de heridas. La célula protagonista miofibroblasto. Este fibroblasto tiene la capacidad de reorganizar su citoesqueleto, alineando filamentos de actina de músculo liso. Esto le permite adherirse a ambos extremos de la herida y contraerse, de tal modo que se obtiene la disminución del espacio entre los bordes de la herida y la remodelación de la cicatriz.
- 15. La fibrilina, una glucoproteína secretada por los fibroblastos, es esencial para la formación de fibras elásticas que están en el tejido conjuntivo. La remodelación de la cicatriz continúa durante muchos meses (seis a 12) después de la lesión y tiene como resultado la formación gradual de una cicatriz madura, avascular y acelular.
- 16. Es posible agruparlos en tres categorías: 1. Formación deficiente de la cicatriz. Es secundaria a las causas locales o sistémicas. 2. Formación excesiva de la cicatriz. Pueden mencionarse la cicatriz hipertrófica en la cual se forma un depósito excesivo de colágeno y ello tiene como resultado una cicatriz abultada o en relieve; la queloide, que es parecida a la cicatriz hipertrófica, con la diferencia de que la formación de la cicatriz rebasa los bordes de la herida; esta última, aunque su mecanismo no se conoce, puede ser muy problemática porque puede crecer aún si se estimula de manera quirúrgica. También puede incluirse la producción de tejido de granulación excesivo (la llamada carnosidad). 3. Contracturas. Corresponden a un proceso excesivo de la contracción de la herida, la cual provoca deformidades e incluso pérdida de la función. Por lo general se identifica en palmas y plantas del pie o incluso en quemaduras graves.
- 21. La segunda población de células inflamatorias que invade la herida la constituyen macrófagos, y se ha reconocido que son esenciales para la cicatrización satisfactoria. Los macrófagos, que se derivan de monocitos circulantes, alcanzan concentraciones importantes en la herida cerca de 48 a 96 h después de la lesión y permanecen en la misma hasta que la cicatrización de la herida termina. La principal función de los macrófagos es la activación e incorporación de otras células por la vía de mediadores, como citocinas y factores de crecimiento, los macrófagos desempeñan una función importante en la regulación de la angiogénesis y el depósito y la remodelación de la matriz.
- 22. PRLIFERACION La fase proliferativa es la segunda fase de la cicatrización de heridas y en general abarca de los días cuatro a 12 (fig. 9-2C). Durante ella la continuidad del tejido se restablece. Los fibroblastos y las células endoteliales son las últimas poblaciones celulares que infiltran la herida en cicatrización y el factor quimiotáctico más potente para fibroblastos es el PDGF. Tras penetrar en el ambiente de la herida, los fibroblastos reclutados necesitan proliferar primero y luego activarse para realizar su principal función de síntesis y remodelación de la matriz. Esta acción es mediada en especial por las citocinas y los factores de crecimiento que los macrófagos de la herida liberan
- 23. SINTESIS DE MATRIZ/COLAGENO El colágeno, la proteína más abundante en el cuerpo, tiene una función crítica en la conclusión satisfactoria de la cicatrización de heridas en adultos. Su depósito, maduración y remodelación subsecuente son esenciales para la integridad funcional de la herida. Los de mayor interés para la reparación de la herida son los tipos I y III. El colágeno tipo I es el principal componente de la matriz extracelular en la piel. El tipo III, que también suele encontrarse en la piel, se torna más prominente e importante durante el proceso de reparación. Los principales glucosaminoglucanos que se encuentran en heridas son el dermatán y el sulfato de condroitina. Estos compuestos son sintetizados por los fibroblastos y su concentración aumenta mucho durante las tres primeras semanas de la cicatrización
- 24. MADURACION Y REMODELACION La maduración y la remodelación de la cicatriz inician durante la fase fibroplástica y se caracterizan por una reorganización del colágeno sintetizado Tanto la cantidad como la calidad del colágeno recién depositado determinan la fuerza y la integridad mecánica de una herida reciente. El depósito de matriz en el sitio de la herida sigue un patrón característico: la fibronectina y el colágeno tipo III constituyen la estructura inicial de la matriz; los glucosaminoglucanos y los proteoglucanos representan los siguientes componentes importantes de la matriz, y el colágeno tipo I es la matriz final. La cantidad de colágeno en la herida llega a una meseta varias semanas después de la lesión, pero la fuerza de tensión continúa en aumento durante varios meses más.
- 25. EPITELIZACION En tanto la integridad y la fuerza del tejido se restablecen, también la barrera externa debe hacerlo. Este proceso se caracteriza en particular por la proliferación y la migración de células epiteliales adyacentes a la herida. El proceso inicia en el transcurso de un día de la lesión y se observa como un engrosamiento de la epidermis en el borde de la herida. Las células marginales del borde de la herida pierden sus inserciones firmes a la dermis subyacente, crecen y comienzan a migrar a través de la superficie de la matriz provisional. Las células basales fijas en una zona cercana al borde del corte experimentan una serie de divisiones mitóticas rápidas y parecen migrar moviéndose una sobre otra en forma de saltos hasta recubrir el defecto. Una vez que el defecto se cubre, las células epiteliales en migración pierden su aspecto aplanado, adquieren una forma más cilíndrica e incrementan su actividad mitótica. Las capas del epitelio se restablecen y al final la capa superficial se queratiniza
- 26. Bibliografía 1. SCHWARTZ PRINCIPIOS DE CIRUGIA. (2010). MC GRAW HILL. PAG 241-246 2. TRATADO DE CIRUGÍA GENERAL. TERCERA EDICIÓN. (2017). EL MANUAL MODERNO. PAG 573-588 3. SENET, P. (2016). FISIOLOGIA DE LA CICATRIZACION CUTÁNEA. ELSEVIER . HTTPS://DOI.ORG/98-040-A-10