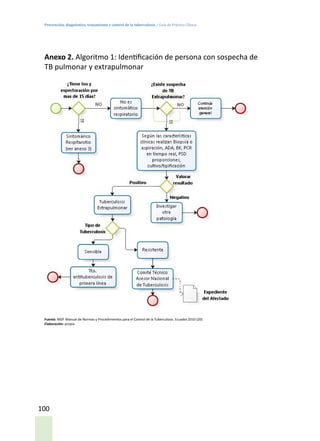
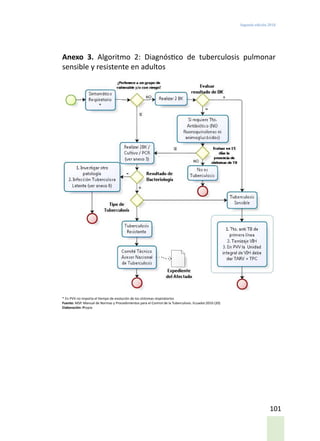
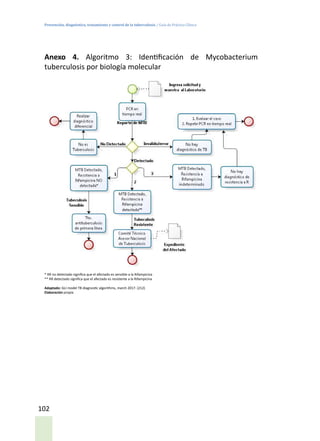
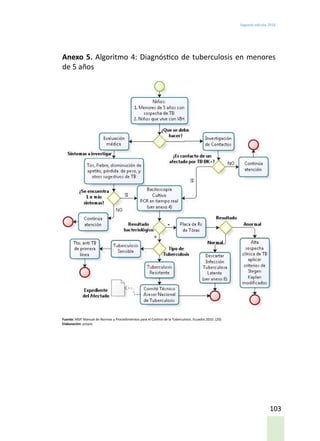
Este documento presenta las guías de práctica clínica para la prevención, diagnóstico, tratamiento y control de la tuberculosis en Ecuador. Incluye definiciones de casos de tuberculosis, resultados de tratamiento, clasificaciones, historia natural de la enfermedad, evidencias y recomendaciones para la prevención, diagnóstico, tratamiento y seguimiento. El objetivo es proveer orientación basada en evidencia científica para profesionales de la salud en la atención de personas con tuberculosis.

































































![Segunda edición 2018
81
la infección tuberculosa latente. Ginebra, Suiza: Organización Mundial de la
Salud; 40.
18. World Health Organization. (2014). Companion handbook to thwe WHO
guidelines of the programmatic management of drug-resistant tuberculosis.
19. Ministerio de Salud Pública del Ecuador. (2017). Manual de procedimientos
para la prevención y control de la Tuberculosis. Quito, Ecuador: MSP;238.
20. Ministerio de Salud Pública. (2010). Manual de normas y procedimientos para
el control de la tuberculosis, 336.
21. Centers for Disease Control and Prevention. (2013). Core Curriculum on
Tuberculosis: What the Clinician Should Know. Centers for Disease Control
and Prevention National Center for HIV/AIDS, Viral Hepatitis, STD, and TB
Prevention Division of Tuberculosis Elimination; 1-320. Disponible en: http://
www.cdc.gov/tb.
22. Houben, RMGJ, Dodd PJ. (Cited 2017 Aug 28). The Global Burden of Latent
Tuberculosis Infection: A Re- estimation Using Mathematical Modelling.
Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5079585/
pdf/pmed.1002152.pdf
23. Blas, E., Kurup Sivasankara A, editors. (2010). Equity, social determinants
and public health programmes. World Health Organization.
Geneva, Switzerland. . Disponible en: http://apps.who.int/iris/
bitstream/10665/44289/1/9789241563970_eng.pdf
24. Pai, M., Behr, MA., Dowdy, D., Dheda, K., Divangahi, M., Boehme, CC., et al.
(2016) Tuberculosis. Nat Rev Dis Prim. (Cited 2017 May 3); 2:16076. Disponible
en: http://www.nature.com/articles/nrdp201676
25. Ministerio de Salud de la Nación. República Argentina. (2014). Enfermedades
infecciosas, tuberculosis. Diagnóstico de tuberculosis. Guía para el equipo de
salud Nro. 3. 2da. Edición. Beltrame, S., Latorraca, M., Moral, M., editores.
Ciudad Autónoma de Buenos Aires, República Argentina; (cited 2017
Aug 29). 27. Disponible en: http://www.msal.gob.ar/images/stories/bes/
graficos/0000000049cnt- guia_de_diagnostico_tratamiento_y_prevencion_
de_la_tuberculosis_2015.pdf
26. Dharmadhikari, AS., Mphahlele, M., Stoltz, A., Venter, K., Mathebula, R.,
Masotla, T., et al. (2012). Surgical Face Masks Worn by Patients with Multidrug-
Resistant Tuberculosis. Am J Respir Crit Care Med.; 185(10):1104–9.
27. Punjabi, CD., Perloff, SR., Zuckerman, JM.. (2016). Preventing Transmission of
Mycobacterium tuberculosis in Health Care Settings. Infect Dis Clin North Am.
30(4):1013–22. Disponible en: http://dx.doi.org/10.1016/j.idc.2016.07.003
28. Minnesota Department of Health. Isolating Potentially Infectious Tuberculosis
(TB ) Patients Recommendations from the Minnesota Department of Health
[Internet]. Disponible en: http://www.health.state.mn.us/divs/idepc/
diseases/tb/isolatingpat.pdf
29. Subbaraman, R., Nathavitharana, RR., Satyanarayana, S., Pai, M., Thomas, BE.,
Chadha, VK., et al. (2016). The Tuberculosis Cascade of Care in India’s Public
Sector: A Systematic Review and Meta-analysis. PLoS Med. 13(10):1–38.](https://image.slidesharecdn.com/gptuberculosis-1-190309145008/85/Gp-tuberculosis-1-81-320.jpg)



![Segunda edición 2018
85
tuberculosis infection in close contacts of people with pulmonary tuberculosis
in low-income and middle- income countries : a systematic review and meta-
analysis. (June 2008):359– 68.
62. Grupo de Estudio de Contactos de la Unidad de Investigación en Tuberculosis
de Barcelona. Documento de consenso sobre el estudio de contactos en los
pacientes tuberculosos. Med Clin. 1999; 112:151–6.
63. OregonHealthAuthorities.(2017).PublicHealthDivision.TuberculosisProgram
Tuberculosis Investigative Guidelines (Cited 2017 Aug 30). Disponible en:
http://www.oregon.gov/oha/ph/DiseasesConditions/CommunicableDisease/
Tubercul osis/Documents/investigativeguide.pdf
64. Dara, M., Grzemska, M., Kimerling, M., Reyes, H., Zagorskiy, A. (2009).
Guidelines for control of Tuberculosis in Prisons. Tuberculosis Coalition for
Technical Assistance and International Committee of the Red Cross;151.
65. Dara, M., Acosta, CD., Vinkeles Melchers, NVS., Al-Darraji, HAA,, Chorgoliani D,
Reyes, H., et al. (2015). Tuberculosis control in prisons: current situation and
research gaps. Int J Infect Dis. (Cited 2017 Aug 30);32:111–7. Disponible en:
http://ac.els-cdn.com/S1201971214017470/1-s2.0-S1201971214017470-
main.pdf?_tid=71e8828a-8dbd-11e7-97aa00000aacb360&acdnat=15041232
25_78e73f4f43cf9bce8c3232a712b9f6ef
66. Lancella, L., Vecchio, A Lo., Chiappini, E., Tadolini, M., Cirillo, D., Tortoli, E., et
al. (2015). How to manage children who have come into contact with patients
affected by tuberculosis. J Clin Tuberc Other Mycobact Dis; 1:1–12. Disponible
en: http://dx.doi.org/10.1016/j.jctube.2015.07.002
67. Tsai, K-S., Chang, H-L., Chien, S-T., Chen, K-L., Chen, K-H., Mai, M-H., et al.
(2013). Childhood Tuberculosis: Epidemiology, Diagnosis, Treatment, and
Vaccination. Pediatr Neonatol (Cited 2017 Aug 30); 54:295–302. Disponible
en: http://dx.doi.org/10.1016/j.pedneo.2013.01.019
68. Wysocki, A., Arakawa, T., et al. Latent Tuberculosis Infection Diagnostic and
Treatment Cascade among Contacts in Primary Health Care in a City of Sao
Paulo State, Brazil: Cross-Sectional Study. [cited 2017 Sep 1]; Disponible
en: http://journals.plos.org/plosone/article/file?id=10.1371/journal.
pone.0155348&type= printable
69. World Health Organization. (2014). Infection prevention and control of
epidemic-and pandemic-prone acute respiratory infections in health care
WHO Guidelines. Geneva, Switzerland. (Cited 2017 Sep 1).156 p. Disponible
en: www.who.int/about/licensing/copyright_form/en/index.html
70. Aït-Khaled, N., Alarcón, E., Armengol, R., Bissell, K., Boillot, F., Caminero, JA.,
et al. (2010). Manejo de la Tuberculosis una Guía Esencial de Buenas Prácticas.
6ta Edición. Unión Internacional contra la Tuberculosis y Enfermedades
Respiratorias, editor. París, Francia; 130.
71. Jordan, R., Valledor, A. (2014). Guías de recomendaciones de prevención de
infecciones en pacientes que reciben modificadores de la respuesta biológica.
Rev Argent Reumatol; 25(2):08–26.](https://image.slidesharecdn.com/gptuberculosis-1-190309145008/85/Gp-tuberculosis-1-85-320.jpg)