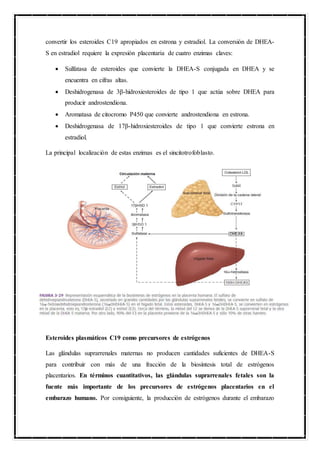
Este documento describe varias hormonas producidas por la placenta humana, incluyendo la gonadotropina coriónica humana (hCG), el lactógeno placentario humano (hPL), la corticotropina coriónica y la relaxina. La hCG se sintetiza principalmente en el sincitiotrofoblasto y desempeña un papel importante en el mantenimiento del cuerpo lúteo durante el embarazo temprano. El hPL estimula la lipólisis y gluconeogénesis maternas y promueve el crecimiento fetal