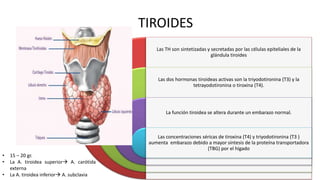
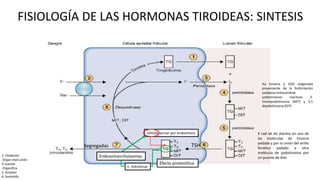
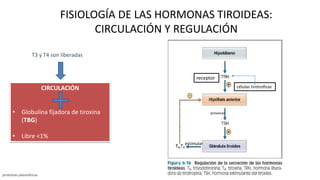
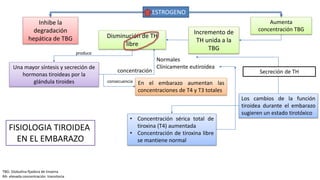
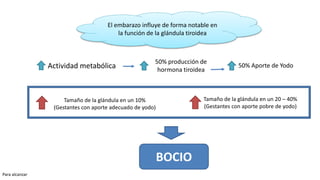
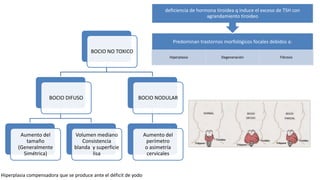
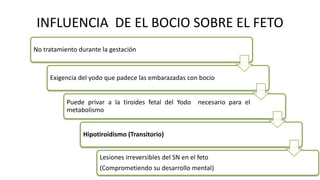
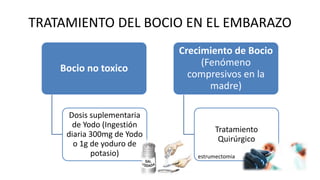
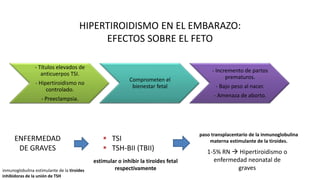
Las hormonas tiroideas experimentan cambios fisiológicos durante el embarazo. La glándula tiroides aumenta su tamaño y producción hormonal para satisfacer las mayores demandas del embarazo. Pueden presentarse alteraciones como hipotiroidismo o hipertiroidismo, las cuales deben diagnosticarse y tratarse para prevenir complicaciones en la madre y el feto.