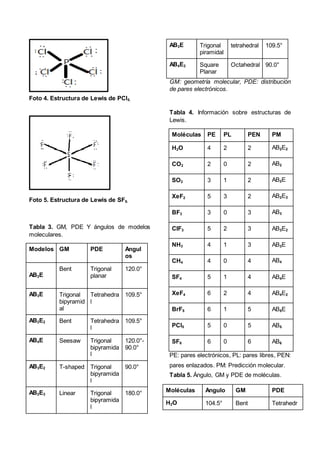
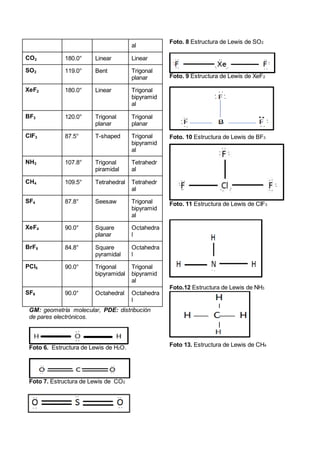
Este informe de laboratorio tuvo como objetivo predecir la geometría molecular y ángulos de diferentes moléculas utilizando la plataforma Phet. Se determinó la geometría y ángulos de moléculas con enlaces sencillos, dobles y triples. Luego, se realizaron estructuras de Lewis y se predijo la geometría de moléculas como BeCl2, BF3, CH4, PCl5, SF6. Finalmente, se predijeron las geometrías de H2O, CO2, SO2 y otras moléculas, coinc