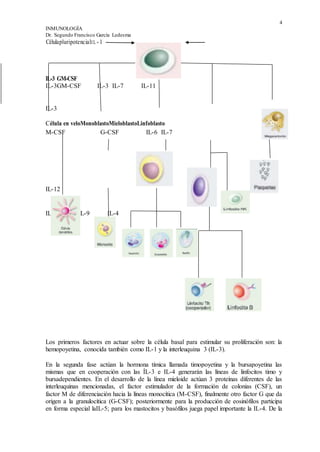
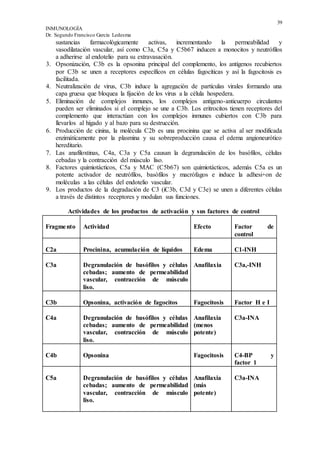
Este documento presenta una introducción general a la inmunología. Explica que el sistema inmunológico está compuesto por mecanismos de defensa innatos y adquiridos que protegen al organismo de agentes nocivos. Describe las principales células y moléculas involucradas, incluyendo linfocitos, macrófagos y citoquinas. También distingue entre la inmunidad innata general y la inmunidad adquirida específica mediada por linfocitos.