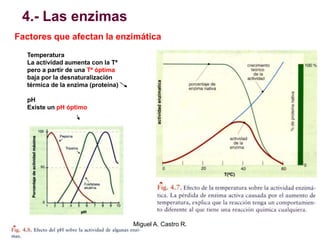
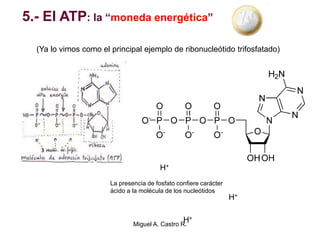
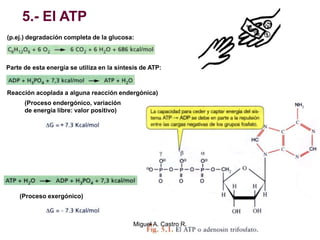
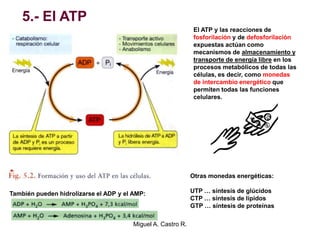
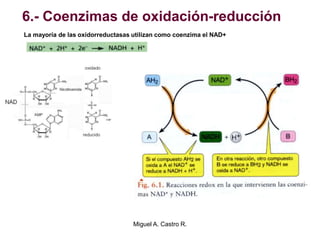
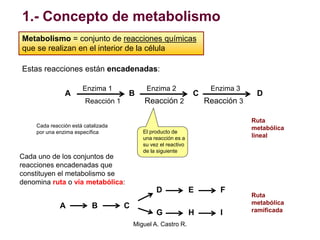
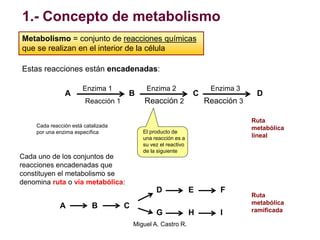
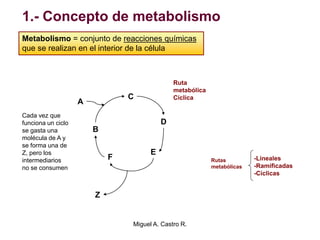
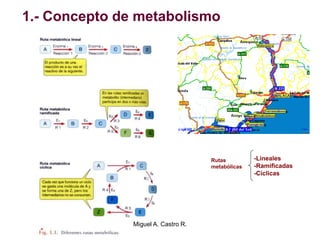
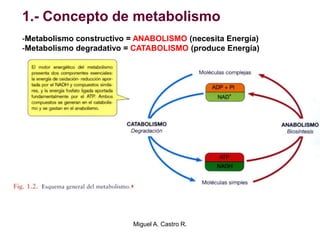
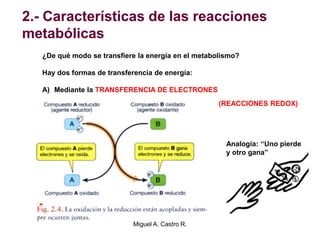
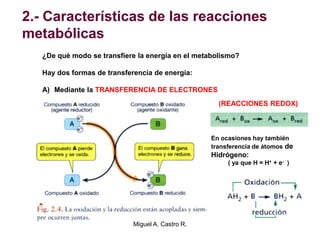
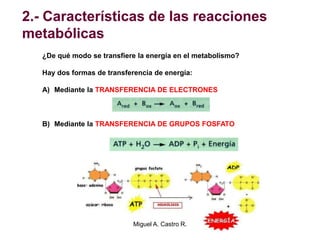
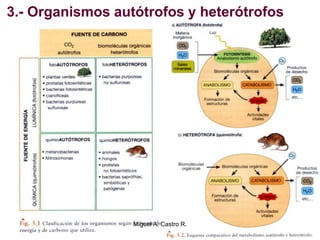
El documento resume los conceptos fundamentales del metabolismo, incluyendo: 1) el metabolismo consiste en reacciones químicas encadenadas en la célula, 2) las reacciones metabólicas son catalizadas por enzimas y transferencia de energía a través de electrones o grupos fosfato, y 3) el ATP sirve como moneda energética almacenando y transfiriendo energía en las reacciones celulares.







![4.- Las enzimas
Cinética enzimática
-No se consumen => vuelven a actuar
=> entre 100 y 1000 moléculas de
sustrato / segundo
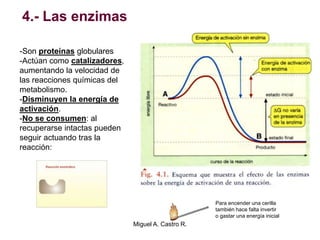
-Saturación por el sustrato: se alcanza
una velocidad máxima
Km = [S] correspondiente a ½ Vmax
La Km es una medida de la afinidad
de la enzima por el sustrato
Miguel A. Castro R.](https://image.slidesharecdn.com/introduccionalmetabolismo-160410050405/85/Introduccion-al-Metabolismo-26-320.jpg)