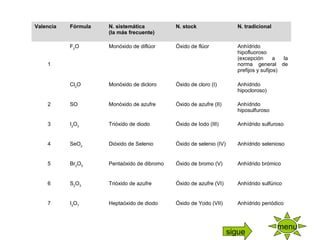
Este documento proporciona información sobre la formulación de química inorgánica, incluyendo la valencia de los elementos, nomenclaturas, óxidos, hidruros, ácidos y sales. Cubre temas como la valencia de metales y no metales importantes, diferentes sistemas de nomenclatura, tipos de óxidos, hidruros, ácidos hidrácidos y oxácidos, e hidróxidos.