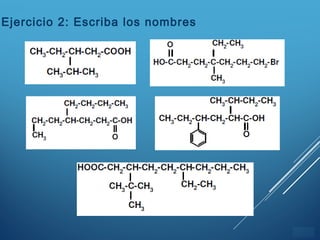
Este documento describe las funciones oxigenadas, incluyendo alcoholes, éteres, aldehídos y cetonas. Explica las propiedades, nomenclatura y usos de estos compuestos orgánicos. También incluye ejemplos y ejercicios para practicar la escritura de nombres y fórmulas.