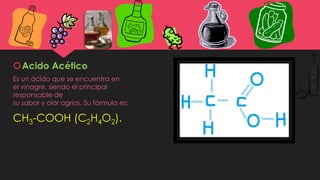
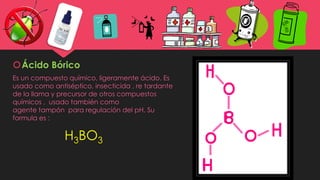
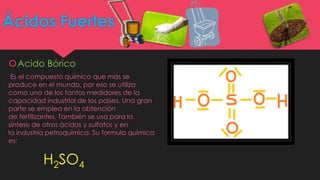
Este documento resume los conceptos básicos de ácidos y bases. Explica que los ácidos tienen sabor agrio y son corrosivos, mientras que las bases tienen sabor amargo y son jabonosas. Luego describe varios ácidos débiles como el cítrico, acético y bórico, así como ácidos fuertes como el sulfúrico, nítrico, bromhídrico. También cubre bases como la sosa caustica, hidróxido de potasio y amoniaco, detallando sus fórmulas