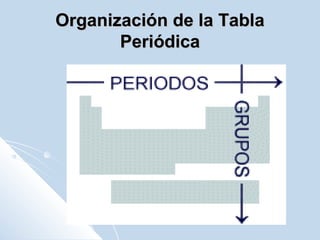
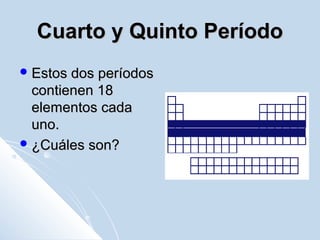
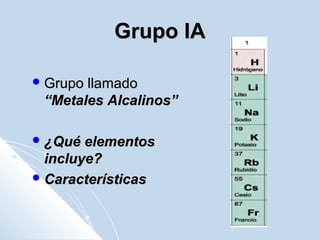
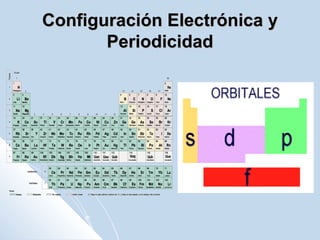
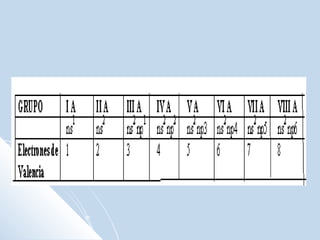
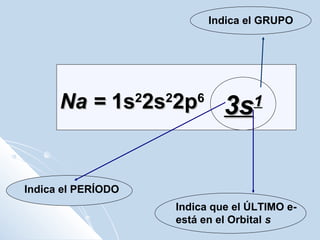
El documento describe la tabla periódica de los elementos químicos. Explica que la IUPAC organiza la tabla, la cual contiene 7 períodos con diferentes números de elementos en cada uno. También describe las características de algunos grupos específicos como los metales alcalinos, los metales alcalinotérreos, los halógenos y los gases nobles. Finalmente, explica que la configuración electrónica de los elementos indica su grupo y período en la tabla, así como sus propiedades químicas.